
【题目】向仅含 Fe2+、I-、Br -的溶液通入适量氯气,溶液中这三种离子的物质的量的变化如下图所示。下列说 法中正确的是
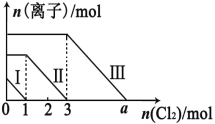
A. 线段Ⅲ代表 Fe2+的变化情况
B. 线段Ⅰ代表 Br -的变化情况
C. 原混合溶液中 n(FeBr2)=4mol
D. a 数值等于 6
【答案】C
【解析】
试题向仅含Fe2+、I-、Br-的溶液中通入适量氯气,还原性I->Fe2+>Br-,首先发生反应2I-+Cl2=I2+2Cl-,I-反应完毕,再反应反应2Fe2++Cl2=2Fe3++2Cl-,Fe2+反应完毕,最后发生反应2Br-+Cl2=Br2+2Cl-,故线段I代表I-的变化情况,线段Ⅱ代表Fe2+的变化情况,线段Ⅲ代表Br-的变化情况.由通入氯气可知,根据反应离子方程式可知溶液中n(I-)=2n(Cl2)=2mol,溶液中n(Fe2+)=2n(Cl2)=2×(3mol-1mol)=4mol,Fe2+反应完毕,根据电荷守恒可知n(I-)+n(Br-)=2n(Fe2+),故n(Br-)=2n(Fe2+)-n(I-)=2×4mol-2mol=6mol.A、由上述分析可知,线段Ⅲ代表Br-的变化情况,A项错误;B、由上述分析可知,线段I代表I-的变化情况,B项错误;C、由上述分析可知,溶液中n(Br-)=2n(Fe2+)-n(I-)=2×4mol-2mol=6mol,根据2Br-+Cl2=Br2+2Cl-可知,溴离子反应需要的氯气的物质的量为3mol,故a=3+3=6,C项正确;D、溶液中n(Br-)=6mol,所以原混合溶液中n(FeBr2)=3mol,c(FeBr2)=3mol·L-1,D项错误;答案选C。


科目:高中化学 来源: 题型:
【题目】实验室中某些气体的制取、收集及尾气处理装置如图所示(省略夹持和净化装置)。仅用此装置和表中提供的物质完成相关实验,最合理的选项是

选项 | a中的物质 | b中的物质 | c中收集的气体 | d中的物质 |
A | 浓氨水 | CaO | NH3 | H2O |
B | 浓硫酸 | Na2SO3 | SO2 | NaOH溶液 |
C | 稀硝酸 | Cu | NO2 | H2O |
D | 浓盐酸 | MnO2 | Cl2 | NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】BHT是一种常用的食品抗氧化剂,从![]() 出发合成BHT的方法有如下两种。下列说法不正确的是
出发合成BHT的方法有如下两种。下列说法不正确的是

A. 推测BHT微溶或难溶于水
B. BHT与![]() 都能与溴水反应产生白色沉淀
都能与溴水反应产生白色沉淀
C. 方法一和方法二的反应类型分别是加成反应和取代反应
D. BHT与![]() 具有的官能团的种类和个数均相等
具有的官能团的种类和个数均相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家最近研究出一种环保、安全的储氢方法,其原理可表示为:NaHCO3+H2 ![]() HCOONa+H2O下列有关说法正确的是( )
HCOONa+H2O下列有关说法正确的是( )
A. 储氢、释氢过程均无能量变化
B. 释氢过程中,每消耗0.1molH2O放出2.24L的H2
C. 上述储氢原理和钢瓶储氢原理相同
D. 1mol固体NaHCO3 中含有2NA个离子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某无色透明的强酸性溶液中,能大量共存的一组离子是
A. Mg2+、A13+、SO42-、NO3- B. Na+、HCO3-、K+、SO42-
C. MnO4-、K+、SO42-、Na+ D. NH4+、Fe2+、Cl-、NO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.按照要求将相应序号填入空白中:
①![]() ②金刚石 ③CO ④CO2 ⑤37Cl ⑥
②金刚石 ③CO ④CO2 ⑤37Cl ⑥![]() ⑦SO2 ⑧
⑦SO2 ⑧![]() ⑨石墨 ⑩C60
⑨石墨 ⑩C60
(1)_______________互为同位素
(2)________________为酸性氧化物
(3)________________的质量数相等,但不能互为同位素
(4)________________互称同素异形体
Ⅱ.已知微粒间的相互作用有以下几种:
①离子键 ②极性共价键 ③非极性共价键 ④氢键 ⑤分子间作用力(范德华力)
下面是某同学对一些变化过程破坏的微粒间的相互作用的判断:
A.干冰熔化②⑤
B.氢氧化钠溶于水①
C.氯化氢气体溶于水②④
D.冰熔化④⑤
E.Na2O2溶于水①②
其中判断正确选项的是_____
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:将Cl2通入适量NaOH溶液,产物中可能有NaCl、NaClO、NaClO3,且![]() 的值仅与温度高低有关,当n(NaOH)=6a mol时,下列有关说法正确的是
的值仅与温度高低有关,当n(NaOH)=6a mol时,下列有关说法正确的是
A. 改变温度,反应中转移电子的物质的量n的范围:3a mol≤n≤5a mol
B. 改变温度,产物中NaCl的最小理论产量为4a mol
C. 参加反应的氯气的物质的量为6a mol
D. 某温度下,若反应后![]() =6,则溶液中
=6,则溶液中![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com