
【题目】已知铅蓄电池的工作原理为Pb+PbO2+2H2SO4![]() 2PbSO4+2H2O,现用如图装置进行电解(电解液足量),测得当铅蓄电池中转移0.4 mol电子时铁电极的质量减少11.2 g。请回答下列问题。
2PbSO4+2H2O,现用如图装置进行电解(电解液足量),测得当铅蓄电池中转移0.4 mol电子时铁电极的质量减少11.2 g。请回答下列问题。

(1)A是铅蓄电池的___________极,铅蓄电池正极反应式为___________,放电过程中电解液的密度___________ (填“减小”、“增大”或“不变”)。
(2)Ag电极的电极反应式是___________,该电极的电极产物共____________g。
(3)Cu电极的电极反应式是____________,CuSO4溶液的浓度____________(填“减小”、“增大”或“不变”)
(4)如图表示电解进行过程中某个量(纵坐标x)随时间的变化曲线,则x表示___________。

a.各U形管中产生的气体的体积
b.各U形管中阳极质量的减少量
c.各U形管中阴极质量的增加量
【答案】 负 PbO2+4H++SO42-+2e-=PbSO4+2H2O 减小 2H++2e-=H2↑ 0.4 Cu-2e-=Cu2+ 不变 B
【解析】试题分析:(1)当铅蓄电池中转移0.4mol电子时铁电极的质量减小11.2g,说明铁作阳极,银作阴极,阴极连接原电池负极,所以A是负极,B是正极,正极上二氧化铅得电子发生还原反应,电极反应式为PbO2+4H++SO42-+2e-═PbSO4+2H2O,放电过程中消耗硫酸,硫酸溶液的密度随浓度减小而减小,故电解的密度减小;
(2)银作阴极,电解稀硫酸时,阴极上氢离子放电生成氢气,电极反应式为2H++2e-═H2↑,生成氢气的质量=0.4mol/2×2g/mol=0.4g;
(3)铜作阳极,阳极上铜失电子发生氧化反应,电极反应式为Cu-2e-═Cu2+,阴极上析出铜,所以该装置是电镀池,电解质溶液中铜离子浓度不变;
(4)右边U形管不析出气体,左边U形管析出气体,所以稀硫酸析出气体体积大于硫酸铜溶液,a错误;当转移相等电子时,溶解金属的物质的量相等,铜的摩尔质量大于铁,所以右边U形管阳极减少的质量大于左边U形管阳极减少的质量,b正确;当转移相等电子时,析出物质的物质的量相等,但铜的摩尔质量大于氢气,所以左边U形管析出氢气的质量小于右边U形管析出铜的质量,c错误。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】工业上由黄铜矿(主要成分为CuFeS2)冶炼铜的主要流程如图所示:
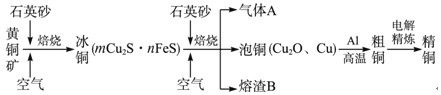
下列说法正确的是( )
A.由黄铜矿到冰铜的反应中,氧化剂是空气,还原剂是CuFeS2
B.气体A中的大气污染物可以用NaOH溶液或氨水吸收
C.将熔渣B用稀硫酸浸泡,取少量所得溶液,滴加KSCN溶液后呈红色,说明熔渣B 中的铁元素显+3价
D.由泡铜到粗铜的反应为吸热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙烯直接氧化法制乙醛的总反应方程式为![]() 。现有人将该反应设计成如图所示的燃料电池,下列有关说法正确的是
。现有人将该反应设计成如图所示的燃料电池,下列有关说法正确的是![]()
![]()

A.该电池可实现化学能与电能之间的相互转化
B.电子移动方向:电极![]() 磷酸溶液
磷酸溶液![]() 电极b
电极b
C.放电时,电路中每转移1mol电子,溶液中就有1molH+向负极迁移
D.电池负极反应式:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】使用新型电极材料,以N2、H2为电极反应物,以HC1-NH4C1为电解质溶液,可制造出一种既能提供电能,又能实现氮固定的新型燃料电池,原理如下图所示。下列有关分析正确的是( )

A. 通入H2—极为正极 B. 分离出的物质X为HC1
C. 电池工作一段时间后,溶液pH减小 D. 通入N2一极的电极反应式为:N2+6e-+8H+=2NH4+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.常温下,将某一元酸HA(甲、乙、丙、丁代表不同的一元酸)和NaOH溶液等体积混合,两种溶液的物质的量的浓度和混合液的pH如下表所示:
实验编号 | HA的物质的量浓度(mol·L-1) | NaOH的物质的量浓度(mol·L-1) | 混合后溶液的pH |
甲 | 0.1 | 0.1 | pH=a |
乙 | 0.12 | 0.1 | pH=7 |
丙 | 0.2 | 0.1 | pH>7 |
丁 | 0.1 | 0.1 | pH=10 |
(1)从甲组情况分析,如何判断HA是强酸还弱酸? 。
(2)乙组混合溶液中离子浓度c(A-)和c(Na+)的大小关系是 。
A.前者大 B.后者大 C.二者相等 D.无法判断
(3)从丙组实验结果分析,该混合溶液中离子浓度由大到小的顺序是 。
(4)分析丁组实验数据,写出该混合溶液中下列算式的精确结果(列式):c(Na+)-c(A-)= mol/L。
Ⅱ.某二元酸(分子式用H2B表示)在水中的电离方程式是:H2B=H++HB-;HB-![]() H++B2-
H++B2-
回答下列问题:
(5)在0.1 mol/L的Na2B溶液中,下列粒子浓度关系式正确的是 。
A.c(B2-)+c(HB-)=0.1mol/L
B.c(B2-)+c(HB-)+c(H2B)=0.1mol/L
C.c(OH-)=c(H+)+c(HB-)
D.c(Na+)+c(OH-)=c(H+)+c(HB-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】依据下列甲、乙、丙三图判断,下列叙述不正确的是
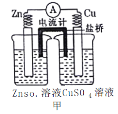
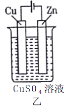
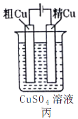
A.甲是原电池,乙是电镀装置
B.甲、乙装置中,锌极上均发生氧化反应
C.乙、丙装置中,阳极均发生氧化反应而溶解
D.丙装置中,若粗铜中含有Au、Ag、Fe、Zn等杂质,电解后Au、Ag形成阳极泥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 时,下列有关电解质溶液说法正确的是
时,下列有关电解质溶液说法正确的是![]()
![]()
A.稀醋酸中加入冰醋酸,醋酸电离平衡右移,电离度增大
B.向NaF溶液中滴加硫酸至中性时,![]()
C.向氨水中加入![]() 固体,溶液中
固体,溶液中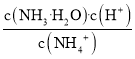 增大
增大
D.AgCl在水和NaCl溶液中的溶度积分别为![]() 、
、![]() ,则
,则![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示原电池的总反应为Cu(s)+2Ag+(aq)===Cu2+(aq)+2Ag(s),下列叙述正确的是

A.电子从银电极经导线流向铜电极
B.盐桥中的阳离子向硝酸银溶液中迁移
C.电池工作时,铜电极发生还原反应
D.将AgNO3溶液更换为Fe(NO3)3溶液,电流表指针反向偏转
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如下图所示,X、Y、Q、W 都是惰性电极,将电源接通后,W极附近颜色逐渐加深。下列说法中不正确的是

A.电源的M 极为正极
B.甲装置中溶液的pH 减小
C.甲装置的两个电极上都有单质生成且物质的量之比为1︰1
D.欲用乙装置给铜镀银,U 极应该是Ag,电镀液选择AgNO3溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com