
����Ŀ���¶�ΪTʱ����4L�����ܱ������г���2molPCl5����ӦPCl5��g��PCl3��g��+Cl2��g������һ��ʱ���ﵽƽ�⣮��Ӧ�����вⶨ�IJ������ݼ��±�������˵����ȷ���ǣ� ��
t/s | 0 | 50 | 150 | 250 | 350 |
n��PCl3��/mol | 0 | 0.32 | 0.38 | 0.40 | 0.40 |
A.��Ӧ��ǰ50s��ƽ������Ϊv��PCl3��=0.0064mol/��Ls��
B.���������������䣬�����¶ȣ�ƽ��ʱc��PCl3��=0.11mol/L����Ӧ�ġ�H��0
C.��ͬ�¶��£���ʼʱ�������г���4molPCl3��4molCl2 �� �ﵽƽ��ʱ����˷�Ӧ�Ļ�ѧƽ�ⳣ��Ϊ0.025mol/L
D.��ͬ�¶��£���ʼʱ���������г���2molPCl5��0.40molPCl3��0.40molCl2 �� �ﵽƽ��ǰv��������v���棩
���𰸡�C
���������⣺A����Ӧ��ǰ50 s��ƽ������Ϊv��PCl3��= ![]() =0.0016 molL��1s��1 �� ��A����
=0.0016 molL��1s��1 �� ��A����
B�������¶ȣ�ƽ��ʱ��c��PCl3��=0.11 molL��1 �� ����ͼ����PCl3Ũ��= ![]() =0.1mol/L��˵������ƽ��������У�����ӦΪ���ȷ�Ӧ����H��0����B����
=0.1mol/L��˵������ƽ��������У�����ӦΪ���ȷ�Ӧ����H��0����B����
C��ƽ���PCl3���ʵ���Ϊ0.4mol��
PCl5��g�� | PCl3��g�� | + | Cl2��g�� | ||
��ʼ����mol/L�� | 0.5 | 0 | 0 | ||
�仯����mol/L�� | 0.1 | 0.1 | 0.1 | ||
ƽ������mol/L�� | 0.4 | 0.1 | 0.1 |
ƽ�ⳣ��K= ![]() =0.025����C��ȷ��
=0.025����C��ȷ��
D����ͬ�¶��£���ʼʱ�������г���2.0molPCl5��0.40molPCl3��0.40molCl2 �� ����Ũ�ȷֱ�Ϊ0.5mol/L��0.1mol/L��0.1mol/L�����Ũ����Q= ![]() =0.02��K=0.025����Ӧû�дﵽƽ��״̬����Ӧ������У��ﵽƽ��ǰv��������v���棩����D����
=0.02��K=0.025����Ӧû�дﵽƽ��״̬����Ӧ������У��ﵽƽ��ǰv��������v���棩����D����
��ѡC��
�����㾫����������Ĺؼ��������⻯ѧƽ��״̬���ʼ����������֪ʶ�����ջ�ѧƽ��״̬�����������ȡ��� V��=V��>0�����������Ƕ�̬ƽ�⣬ƽ��ʱ��Ӧ���ڽ��У�����������Ӧ������и���ְٷֺ������䣻���䡱�������ı䣬ƽ�ⱻ���ƣ������µ������½����µĻ�ѧƽ�⣻��;���أ�����������䣬���淴Ӧ�����Ǵ�����Ӧ��ʼ�����Ǵ��淴Ӧ��ʼ�����ɽ���ͬһƽ��״̬����Ч�����Լ��Ի�ѧƽ��ļ�������⣬�˽ⷴӦ��ת����=ת��Ũ�ȡ���ʼŨ�ȡ�100%=ת�����ʵ�������ʼ���ʵ�����100%����Ʒ�IJ���=ʵ�����ɲ�������ʵ����������Ͽɵõ���������ʵ�����100%��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1.1 g���������������200 mL 5 mol��L��1�����У���Ӧ�������Ũ�ȱ�Ϊ4.6 mol��L��1(��Һ����仯���Բ���)����
(1)��Ӧ������HCl�����ʵ�����
(2)�û�����������������ʵ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������������ѧ��FuNvio Cacace���˻���˼��������о������N4���ӣ�N4���ӽṹ��ͼ��ʾ����֪����1molN��N����193kJ����������1molN��N�ų�941kJ����������������Ϣ�����ݣ�����˵����ȷ���ǣ� �� 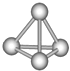
A.N4����һ�����͵Ļ�����
B.N4��N2��ͬϵ��
C.N4ת��ΪN2 �������仯
D.1molN4����ת��ΪN2�ų�724kJ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ƽ��仯������й㷺����;��
��1����ҵ���Ʊ������Ƶij��÷����� �� ��д���Ʊ������ƵĻ�ѧ����ʽ �� �����ƿ����� ��д��Na���۵�ͷ����һ����;����
��2����Na2CO3������������ʣ�CO��O2��CO2Ϊԭ�Ͽ�������͵�أ��õ�صĽṹ��ͼ��ʾ��
�������ĵ缫��ӦʽΪ �� ��ع���ʱ����A��ѭ��ʹ�ã�A���ʵĻ�ѧʽΪ ��
����д������Na2CO3����Ԫ�صķ��� ��
��3�������£�Ũ�Ⱦ�Ϊ0.1molL��1����������������Һ��pH���±���
���� | CH3COONa | NaHCO3 | Na2CO3 | NaCO | NaCN |
pH | 8.8 | 9.7 | .6 | 0.3 | �� |
��������Һ���������У����H+������ǿ���� �� ���ݱ������ݣ�Ũ�Ⱦ�Ϊ0.01molL��1���������������Һ�ֱ�ϡ��100����pH�仯������������ţ���
a��HCN b��HClO c��CH3COOH d��H2CO3
��4��ʵ�����г���NaOH������β��������ϴ�����ᴿ��
�ٳ����£���300mL 1molL��1��NaOH��Һ����4.48L������ɱ�״����SO2ʱ��������ҺpH��7������Һ�и�����Ũ���ɴ�С��˳��Ϊ ��
����֪�������ӿ�ʼ����ʱ��pH���±���
���� | Fe2+ | Cu2+ | Mg2+ |
pH | 7.6 | 5.2 | 10.4 |
������ͬŨ��Cu2+��Mg2+��Fe2+����Һ�еμ�ijŨ�ȵ�NaOH��Һʱ���������ӷ��ţ��ȳ�����Ksp[Fe��OH��2] Ksp[Mg��OH��2]�����������=����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����A��B��C�����ձ��зֱ�ʢ����ͬŨ�ȵ�ϡ���ᣬ��ͼ��ʾ��
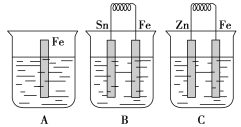
(1)A�з�Ӧ�����ӷ���ʽΪ_____________________________��
(2)B��Sn���ĵ缫��ӦʽΪ____________________________��Sn��������Һ��pH________(���������С�����䡱)��C�б���ʴ�Ľ�����________���ܷ�Ӧ�����ӷ���ʽΪ________________���Ƚ�A��B��C��������ʴ�����ʣ��ɿ쵽����˳����________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ����ʵ���ҽ��а��������Ʊ�������ʵ������װ�ã����̶ֹ�װ��δ������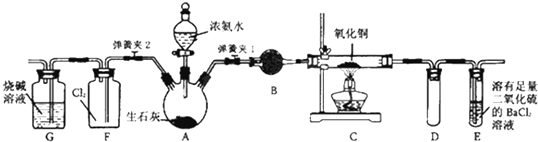
��1������װ��װ�ú���Ҫ����A��Eװ�õ������ԣ����������
�� �� Ȼ����A���쵽E��������ð�����ƿ��ƾ��ƣ�E�е�����ˮ���γ�˵��װ�����������ã�
��2������ƽ���ƶ���ԭ������A����ȡ������ԭ�� ��
��3��װ��B��ʢ���Լ��� ��
��4���رյ��ɼ�2�����ɼ�1���ӷ�Һ©���ų�Ũ��ˮ����û��ƿ�й����رշ�Һ©����������ȼC���ƾ��ƣ�װ��C�к�ɫ������죬װ��E��
����������E���ݳ�Һ����������ֱ�������������д����C�з�����Ӧ�Ļ�ѧ����ʽ ��
��5����C�й���ȫ�����ɫ�رյ��ɼ�1�������ƿ��ƾ��ƣ�����ȴ����C�й�������������Ӧǰ��������Ϊ16g����Ӧ����ع�����������2.4g��ͨ������ȷ���ù������ijɷ��� ��
��6���ڹرյ��ɼ�1���ɼ�2�������������F�У��ܿ췢��װ��F�в������̣�ͬʱ����G����ҺѸ�ٵ�������F�У�д���������̵Ļ�ѧ����ʽ �� Ѹ�ٲ���������ԭ���� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����е��뷽��ʽ��������
A.NaOH��Na++OH-B.H2OH++OH-
C.H2SO4��2H++SO42-D.HClO��H++ClO-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������Ԫ����Ϊ����������������Ϊ������һ��﮵�أ���λ�����ĵ�����ŵ�������ߴ�1675mAh/g��ԶԶ������ҵ�Ϲ㷺Ӧ�õ�����﮵�ص���������150mAh/g������������һ�ֶԻ����Ѻõ�Ԫ�أ��Ի�������û����Ⱦ���������һ�ַdz���ǰ����﮵�أ��乤��ԭ����ͼ��ʾ�����й�������ص�˵������ȷ���ǣ� �� 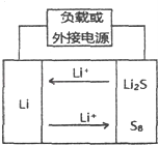
A.�ŵ�ʱ���Ϊ������������ԭ��Ӧ
B.���ʱ������ӦʽΪ��8Li2S��16e���TS8+16Li+
C.����ʿɲ��õ����л������
D.����ص����۵�ѹΪ2.0V����λ�����ĵ�����ı�����Ϊ3.35 kWh/kg
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������������Դ����ѧ��ͨ����ѧ����ʹ��������������������ʽת�����Ӷ������Դ�������ʡ�
��1��������ȼ��ʱ���ų�����������˵���÷�Ӧ��____��Ӧ������ȡ������ȡ������������ڷ�Ӧ���������___�������������������ڡ���С�ڡ������ӻ�ѧ��Ӧ�ı��ʽǶ������������ڶ��ѷ�Ӧ���еĻ�ѧ�����յ�������________�γɲ���Ļ�ѧ���ų���������������ڡ���С�ڡ�����
��2��ͨ��������ȼ�շ�Ӧ�������������̺��Ļ�ѧ��ת��Ϊ���ܣ��������������ԭ��Ӧ��Ƴ�ԭ���װ�ã��Ϳ����������̺��Ļ�ѧ��ת��Ϊ���ܣ���ͼ�����ܹ�ʵ�ָ�ת����װ�ã�����Ϊ����ȼ�ϵ�ء�

�õ�ص�������_____(�a�缫����b�缫��)���ڸ��������ĵ缫��Ӧʽ��_________________����ط�Ӧ���ܷ���ʽ________________________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com