
【题目】据报道,我国拥有完全自主产权的氢氧燃料电池车将在北京奥运会期间为运动员提供服务。某种氢氧燃料电池的电解液为KOH溶液,下列有关该电池的叙述不正确的是( )
A. 正极反应式为:O2+2H2O+4e-====4OH-
B. 工作一段时间后,电解液中KOH的物质的量不变
C. 该燃料电池的总反应方程式为:2H2+O2====2H2O
D. 用该电池电解CuCl2溶液,产生2.24 L Cl2(标准状况)时,有0.1 mol电子转移
【答案】D
【解析】
在碱性条件下,通入O2的一极发生还原反应,该极作原电池的正极,正极反应式为O2+2H2O+4e-====4OH-;通入H2的一极发生氧化反应,该极作原电池的负极,负极反应式为2H2+4OH--4e-====4H2O;两极保证得失电子守恒相加得到总的电极反应:2H2+O2====2H2O,在放电过程中,只是H2、O2参加反应,KOH是电解液不参加反应,物质的量不变,但在整过过程中不断产生水,KOH浓度不断减小。用该电池电解CuCl2溶液,产生2.24 L Cl2。由电解池的原理知道电解方程式为:CuCl2![]() Cu+Cl2↑,产生1 mol Cl2转移2 mol电子,
Cu+Cl2↑,产生1 mol Cl2转移2 mol电子,![]() ,所以D错误,答案选D。
,所以D错误,答案选D。


 同步练习强化拓展系列答案
同步练习强化拓展系列答案科目:高中化学 来源: 题型:
【题目】用脱脂棉包住约0.2g过氧化钠粉末,置于石棉网上,往脱脂棉上滴水,观察到脱脂棉剧烈燃烧。
(1)由上述实验现象所得出的有关过氧化钠跟水反应的结论是:①有氧气生成;②____________。Na2O2跟水反应的化学方程式是____________。
(2)某研究性学习小组拟用如图所示装置(气密性良好)进行实验,以证明上述结论。用以验证第一条结论的实验方法是_________;用以验证第二条结论的实验方法是________。

(3)工业上将氯气通入石灰乳[Ca(OH)2]制取漂白粉,化学方程式为____。
(4)将Cl2制成漂白粉的主要目的是________(填字母)。
A.增强漂白能力和消毒作用
B.使它转化为较稳定物质,便于保存和运输
C.使它转化为较易溶于水的物质
D.提高氯的质量分数,有利于漂白、消毒
(5)将漂白粉溶于适量水中,呈白色浊状物,静置沉降。取少许上层清液,滴加碳酸钠溶液出现白色沉淀,发生反应的化学方程式为_________。
(6)瓶装漂白粉久置空气中会呈稀粥状而失去漂白作用。试用化学方程式表示漂白粉在空气中易失效的原因是①_____________;②__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有金属单质A、B和气体甲、乙(黄绿色气体)、丙及物质C 、D、E、F、G,它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出)。
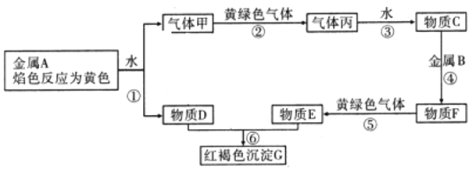
请根据以上信息回答下列问题:
(1)写出下列物质的化学式:A_______、B_______、G ________
(2)写出反应①的化学方程式__________________________________;反应⑤的离子方程式 ____________________________________;
(3)检验物质E的阳离子可以滴加KSCN,现象为_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于Fe(OH)3胶体的叙述中,正确的是( )
A. 制备Fe(OH)3胶体的化学方程式是FeCl3+3H2O![]() Fe(OH)3↓+3HCl
Fe(OH)3↓+3HCl
B. 在制备Fe(OH)3胶体的实验中,加热煮沸时间越长,越有利于胶体的生成
C. Fe(OH)3胶体微粒能吸附阳离子,从而使Fe(OH)3胶体带有一定电荷
D. Fe(OH)3胶体能够吸附水中悬浮的固体颗粒并沉降,达到净水目的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下下列各组离子在指定溶液中能大量共存的是 ( )
A. c(H+)/c(OH-)=1×1012的溶液中:NH、Cl-、NO、Al3+
B. 由水电离出的c(H+)=1×10-14mol/L的溶液中:Ca2+、Cl-、HCO、K+
C. pH=1的溶液中:Fe2+、NO、SO![]() 、Na+
、Na+
D. c(Fe3+)=0.1mol/L的溶液中:K+、ClO-、SO![]() 、SCN-
、SCN-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标准状况下,将a L H2和Cl2的混合气体点燃,充分反应后,将混合气体通入含b mol NaOH的热溶液中,气体恰好被完全吸收,NaOH无剩余,测得反应后溶液中含Cl-、ClO-、![]() ,且三者物质的量之比为8∶1∶1,则原混合气体中H2的物质的量为( )
,且三者物质的量之比为8∶1∶1,则原混合气体中H2的物质的量为( )
A. ![]() mol B.
mol B. ![]() mol C.
mol C. ![]() mol D.
mol D. ![]() mol
mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用化学反应原理研究N、S氧化物有着重要的意义。
(1)已知:
2SO2(g)+O2(g) ![]() 2SO3(g)ΔH1=-196.6kJ/mol
2SO3(g)ΔH1=-196.6kJ/mol
2NO(g)+O2(g) ![]() 2NO2(g)ΔH2=-113.8kJ/mol
2NO2(g)ΔH2=-113.8kJ/mol
NO2(g)+SO2(g)![]() SO3(g)+NO(g)ΔH3
SO3(g)+NO(g)ΔH3
则ΔH3=________,如果上述三个反应方程式的平衡常数分别为K1、K2、K3,则K3=________(用K1、K2表示)。
(2)如下图所示,A是恒容的密闭容器,B是一个体积可变的充气气囊。保持恒温,关闭K2,分别将2 mol NO和1 mol O2通过K1、K3分别充入A、B中,发生的反应为2NO(g)+O2(g)![]() 2NO2(g)[不考虑2NO2(g)
2NO2(g)[不考虑2NO2(g)![]() N2O4(g)],起始时A、B的体积相同均为a L。
N2O4(g)],起始时A、B的体积相同均为a L。

①下列说法和示意图能说明A、B容器均达到平衡状态的是________。
a.A、B容器中气体的颜色均不发生变化
b.A、B容器中NO和O2物质的量浓度比均为2∶1
c.A、B容器中气体的密度不在发生变化
d.A、B容器中气体的平均摩尔质量不再发生变化
e.
②T ℃时,A容器中反应达到平衡时的平衡常数Kp=0.27(kPa)-1。若A容器中反应达到平衡时p(NO2)=200 kPa,则平衡时NO的转化率为________。(Kp是用平衡分压代替平衡浓度计算所得的平衡常数,分压=总压×物质的量分数)
(3)将0.2 mol SO2和0.15 mol O2通入2 L的密闭容器中,测得SO2的物质的量随时间变化如下图实线所示。

①ab段平均反应速率______________(填“大于”“小于”或“等于”)bc段平均反应速率;de段平均反应速率为________。
②仅改变某一个实验条件,测得SO2的物质的量随时间变化如上图中虚线所示,则改变的条件是________。
③如图电解装置可将雾霾中的NO、SO2分别转化为NH4+和SO42-。阴极的电极反应式是_______________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:

(1)从氯化钾溶液中得到氯化钾固体,选择装置________(填代表装置图的字母,下同);除去自来水中的Cl-等杂质,选择装置________。
(2)从碘水中分离出I2,选择装置________,该分离方法的名称为________。
(3)装置A中①的名称是________,进水的方向是从________口进水。装置B在分液时为使液体顺利滴下,除打开活塞外,还应进行的具体操作是____。
(4)海水中蕴藏着丰富的资源,在实验室中取少量海水,进行如下流程的实验:
![]()
![]()
![]()
![]()
![]() ―→
―→![]()
粗盐中含Ca2+、Mg2+、Fe3+、SO42-等杂质,需要提纯后才能综合利用。粗盐提纯的步骤有:
①加入过量的Na2CO3溶液 ②加入过量的BaCl2溶液 ③加入过量的NaOH溶液 ④调节溶液的pH等于7 ⑤溶解 ⑥过滤 ⑦蒸发
正确的操作顺序是________(填选项字母)。
a.⑤②③①⑥④⑦ b.⑤①②③⑥④⑦
c.⑤②①③④⑥⑦ d.⑤③②①⑥④⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.甲、乙、丙三种物质有如图所示的转化关系。

若甲、乙、丙依次是氢气、水、硫酸。
(1)写出甲―→乙的化学方程式:_____。
(2)乙―→丙时所需另一种反应物中,一定含有____和氧元素。
若甲为碳酸钙,丙为氯化钙。
(3)乙可以是______(填名称)。
Ⅱ.N原子的摩尔质量是_____;1molHNO3的质量是____;标准状况下11.2LHCl气体的物质的量是___;2molOH-约含有___个电子。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com