
��14�֣� ������װ�����ⶨ��Ʒ����ĺ����������ձ�A��ʢ������1mol/L Na2SO4��Һ���ձ�B�мӽ������������ڲⶨ��E��ֱ����ѹ��Դ��K�����أ�R���ɱ���裻G�����ƣ�D�����š�
������װ�����ⶨ��Ʒ����ĺ����������ձ�A��ʢ������1mol/L Na2SO4��Һ���ձ�B�мӽ������������ڲⶨ��E��ֱ����ѹ��Դ��K�����أ�R���ɱ���裻G�����ƣ�D�����š�
1����ȡ5.000g������Ʒ���ܽ����뻹ԭ�����黹ԭΪ������As����HAsO32��������ȥ�����Ļ�ԭ����ת�Ƶ�250mL����ƿ�����250mL��Һ��ȡ40mL�ʵ�Ũ�ȵ�KI��NaHCO3�����Һ����B�У�������Һ��ȡ����������Һ10mL����B�У��߽���ߵ�⣬��������I2��As�����١�����������Ϊ As��V������2mA�ĵ������4��1���Ӧ��ȫ���ٶ�����û����ʧ��������Ʒ��Aa2O3�İٷֺ�������1�����ӵĵ���Ϊ1.602��10��19���أ�As2O3��ʽ��Ϊ197.84��
2��װ��A��B�еĵ�ⷴӦֻ��2V���µĵ�ѹ�Ϳ�ʵ�֣�ΪʲôEҪѡ��40V���ϣ�
3����Ӧ�յ����ʲôָʾ����ȷ����
4��HAsO32���Ļ�ԭ����I������ĸ�ǿ�����ʱ����������I2��������As��V����ԭ����ʲô��
5��HAsO32�����Ժ���Һ�е�O2��Ӧ���ܽ�����ʹ�ⶨ���ƫ����ƫ�ͣ�ʵ���������������ܽ�����Ӱ�죿
6����ָʾ���жϷ�Ӧ�յ���2���ʱ�����ɱ��⣬��Ҫ��ⶨ��������������1%������ʱ��Ҫ��ƿ���Ϊ���������ϣ�
1��0.124%��5�֣�
2�����ŵ��Ľ��У������е��跢���仯��Ϊ�˵õ��ȶ��ĵ����������ýϸߵĵ�ѹ�ͽϴ���裬������С��E��R���ƣ�I��E/(R��R��)��R����Խ�С���ɺ��Ե��衣��2�֣�
3�����ۣ�1�֣�
4��HAsO32��ǿ��1�֣� �缫��I���ķ�Ӧ���ʱ�HAsO32���죨1�֣�
5��ƫ�ͣ�1�֣����ȼӹ�����As�����跴Ӧ��Ȼ������۸պñ�ɫΪֹ���ټӴ���Һ���ⶨ��2�֣�
6����Ҫ��ⶨ��������������1%��Ӧ����200�����ϡ���2�֣�


 ͨ��ѧ��Ĭд����ϵ�д�
ͨ��ѧ��Ĭд����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
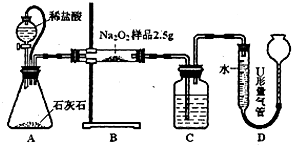 Ϊ�ⶨ����Na2O���ʵ�Na2O2��Ʒ�Ĵ��ȣ��ס��Ҷ�λͬѧ����˶��ֲ�ͬ��ʵ�鷽����
Ϊ�ⶨ����Na2O���ʵ�Na2O2��Ʒ�Ĵ��ȣ��ס��Ҷ�λͬѧ����˶��ֲ�ͬ��ʵ�鷽����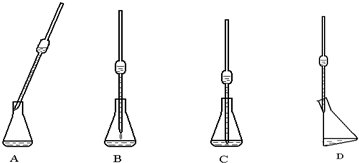
| �ζ����� | ��һ�εζ� | �ڶ��εζ� | �����εζ� |
| ���ı�����������mL�� | 24.98 | 25.00 | 25.02 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��11�֣�Ϊ�ⶨ����Na2O���ʵ�Na2O2��Ʒ�Ĵ��ȣ��ס��Ҷ�λͬѧ����˶��ֲ�ͬ��ʵ�鷽����
��֪��2Na2O2+2CO2===2Na2CO3+O2 2Na2O2+2H2O=== 4NaOH+O2
�ף���ͼl��ʾװ�ã�ͨ���ⶨNa2O2��CO2��Ӧ����O2��������ⶨ��Ʒ�Ĵ��ȡ�
(1)C����ʢ��ҩƷ�ǣ� ��
(2)A����Ƥ�ܵ������ǣ� ��
(3)���ø�ʵ�鷽������Na2O2�Ĵ�������ƫ����ԭ������� (��ѡ����ĸ)��
a��װ��A��B�еĿ����Բⶨ���������Ӱ��
b��װ��C�еĿ����Բⶨ���������Ӱ��
c������ʱU���������е�Һ������ҵ�
d������ʱU���������е�Һ������Ҹ�
�ң���ȡ3��500 g���������1000.00 mL��Һ����0.1000 mol��L-1�ı�����ζ���
(4)ȡ����������Һ25.00 mL����ƿ�У���������ͼ��ʾ���ֲֳ���ʡ�ԣ�����ȷ�IJ�����ͼ ��ȡ��Һ���������������� ��

(5)�ζ�����ƽ��ʵ������ݼ�¼���±���
| �ζ����� | ��һ�εζ� | �ڶ��εζ� | �����εζ� |
| ���ı�����������mL�� | 24.98 | 25.00 | 25.02 |
�ɱ������ݼ�����Ʒ��Na2O2����Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2010�������а�У�߶���ѧ����ĩ������ѧ���� ���ͣ�ʵ����
��11�֣�Ϊ�ⶨ����Na2O���ʵ�Na2O2��Ʒ�Ĵ��ȣ��ס��Ҷ�λͬѧ����˶��ֲ�ͬ��ʵ�鷽����
��֪��2Na2O2+2CO2="==" 2Na2CO3+O2 2Na2O2+2H2O="==" 4NaOH+O2
�ף���ͼl��ʾװ�ã�ͨ���ⶨNa2O2��CO2��Ӧ����O2��������ⶨ��Ʒ�Ĵ��ȡ�
(1)C����ʢ��ҩƷ�ǣ� ��
(2)A����Ƥ�ܵ������ǣ� ��
(3)���ø�ʵ�鷽������Na2O2�Ĵ�������ƫ����ԭ������� (��ѡ����ĸ)��
a��װ��A��B�еĿ����Բⶨ���������Ӱ��
b��װ��C�еĿ����Բⶨ���������Ӱ��
c������ʱU���������е�Һ������ҵ�
d������ʱU���������е�Һ������Ҹ�
�ң���ȡ3��500 g���������1000.00 mL��Һ����0.1000 mol��L-1�ı�����ζ���
(4)ȡ����������Һ25.00 mL����ƿ�У���������ͼ��ʾ���ֲֳ���ʡ�ԣ�����ȷ�IJ�����ͼ ��ȡ��Һ���������������� ��
(5)�ζ�����ƽ��ʵ������ݼ�¼���±���
| �ζ����� | ��һ�εζ� | �ڶ��εζ� | �����εζ� |
| ���ı�����������mL�� | 24.98 | 25.00 | 25.02 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2010�������а�У�߶���ѧ����ĩ������ѧ���� ���ͣ�ʵ����
��11�֣�Ϊ�ⶨ����Na2O���ʵ�Na2O2��Ʒ�Ĵ��ȣ��ס��Ҷ�λͬѧ����˶��ֲ�ͬ��ʵ�鷽����
��֪��2Na2O2+2CO2=== 2Na2CO3+O2 2Na2O2+2H2O=== 4NaOH+O2
�ף���ͼl��ʾװ�ã�ͨ���ⶨNa2O2��CO2��Ӧ����O2��������ⶨ��Ʒ�Ĵ��ȡ�
(1)C����ʢ��ҩƷ�ǣ� ��
(2)A����Ƥ�ܵ������ǣ� ��
(3)���ø�ʵ�鷽������Na2O2�Ĵ�������ƫ����ԭ������� (��ѡ����ĸ)��
a��װ��A��B�еĿ����Բⶨ���������Ӱ��
b��װ��C�еĿ����Բⶨ���������Ӱ��
c������ʱU���������е�Һ������ҵ�
d������ʱU���������е�Һ������Ҹ�
�ң���ȡ3��500 g���������1000.00 mL��Һ����0.1000 mol��L-1�ı�����ζ���
(4)ȡ����������Һ25.00 mL����ƿ�У���������ͼ��ʾ���ֲֳ���ʡ�ԣ�����ȷ�IJ�����ͼ ��ȡ��Һ���������������� ��

(5)�ζ�����ƽ��ʵ������ݼ�¼���±���
|
����� |
��һ�εζ� |
�ڶ��εζ� |
�����εζ� |
|
���ı�����������mL�� |
24.98 |
25.00 |
25.02 |
�ɱ������ݼ�����Ʒ��Na2O2����Ϊ ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com