
在一定容积的密闭容器中发生反应:X(g)+Y(g)  Z(g)+W(s);ΔH>0。若开始投入1 mol X和1 mol Y,在一定条件下达到平衡,改变条件,其变化关系符合甲、乙图像。下列有关判断正确的是
Z(g)+W(s);ΔH>0。若开始投入1 mol X和1 mol Y,在一定条件下达到平衡,改变条件,其变化关系符合甲、乙图像。下列有关判断正确的是
A.甲图表示温度对X转化率的影响,且Ⅰ温度较低
B.乙图一定表示压强对X体积分数的影响,且Ⅳ压强较高
C.甲图一定表示压强对X体积分数的影响,且Ⅰ压强较高
D.甲、乙图都可以表示温度、压强对平衡的影响,且Ⅰ>Ⅱ、Ⅲ<Ⅳ

 巧学巧练系列答案
巧学巧练系列答案科目:高中化学 来源: 题型:
20℃时,在100 g水中溶解11.1 g K2SO4恰好达到饱和,此饱和溶液的密度为1.08 g·cm―3。若将350 mL此温度下K2SO4饱和溶液用水稀释至500 mL。计算稀释后溶液中K2SO4的物质的量浓度。
查看答案和解析>>
科目:高中化学 来源: 题型:
元素X、Y、Z、W均为短周期元素,且原子序数依次增大。已知Y原子最外层电子数
占核外电子总数的3/4,W—、Z+、X+半径逐渐减小,化合物XW常温下为气体,Z是本周
期中除稀有气体元素外,原子半径最大的元素,据此回答下列问题:
(1)Z在元素周期表中的位置 ,工业上生产Z单质的化学方程式为
(2)A、B均为由上述四种元素中的三种组成的强电解质,且常温下两种物质的水溶液pH
均大于7,组成元素的原子数目比均为1∶1∶1。若A能抑制水的电离,而B能促进水的电
离,则A、B的化学式分别为 、 。
(3)C是由上述四种元素的两种组成的相对分子质量为34的化合物,则C的电子式 。
(4)用B在碱性条件下可以处理CN—的工业废水,请将下列6种微粒:CN—、CO32—
N2、OH—、B的阴离子,W的阴离子,分别填入在下对应的横线上,组成一个配平的离子方程式: + + ═ + + + H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
下列事实中,不能用勒夏特列原理解释的是
A.盛有NO2和N2O4 混合气体的烧瓶置于热水中,气体颜色变深
B.工业合成氨选择500oC左右的温度比室温有利
C.实验室中常用排饱和食盐水的方法收集Cl2
D.合成氨时采用循环操作及将氨液化分离,可提高原料的利用率
查看答案和解析>>
科目:高中化学 来源: 题型:
向Ba(OH)2溶液中逐滴滴入稀H2SO4,则溶液的导电能力,下列叙述描述正确的是( )
A.开始时,导电能力肯定最强 B.当沉淀为最大值时,导电性最弱
C.先变强,后变弱 D.逐渐变弱
查看答案和解析>>
科目:高中化学 来源: 题型:
水溶液中能大量共存的一组离子是
A.Na+、Ca2+、Cl-、SO42- B.Fe2+、H+、SO32-、ClO-
C.Mg2+、NH4+、Cl-、SO42- D.K+、Fe3+、NO3-、SCN-
查看答案和解析>>
科目:高中化学 来源: 题型:
化合物Ⅰ(C11H12O3)是制备液晶材料的中间体之一,其分子中含有醛基和酯基。Ⅰ可以用E和H在一定条件下合成:
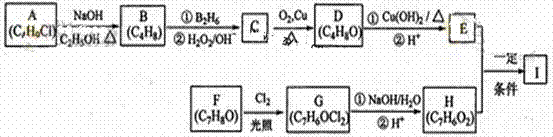
已知以下信息:
A的核磁共振氢谱表明其只有一种化学环境的氢;
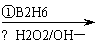 |
RCH=CH2 RCH2CH2OH
化合物F苯环上的一氯代物只有两种;
通常在同一个碳原子上连有两个羟基不稳定,易脱水形成羰基。
回答下列问题:
A的化学名称为_________。
D的结构简式为_________ 。
E的分子式为___________。
(4)F生成G的化学方程式为
________ ,
该反应类型为__________。
(5)I的结构简式为___________。
(6)I的同系物J比I相对分子质量小14,J的同分异构体中能同时满足如下条件:
①苯环上只有两个取代基,
②既能发生银镜反应,又能和饱和NaHCO3溶液反应放出CO2,共有______种(不考虑立体异构)。J的一个同分异构体发生银镜反应并酸化后核磁共振氢谱为三组峰,且峰面积比为2:2:1,写出J的这种同分异构体的结构简式______ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com