
【题目】下列有关钠及其化合物的有关说法中正确的是( )
A.钠与CuSO4溶液反应的离子方程式为2Na+Cu2+═Cu+2Na+
B.7.8 g Na2O2含离子数为0.4NA
C.“侯氏制碱法”中的碱指NaHCO3
D.向Na2CO3饱和溶液中通入足量的CO2,有NaHCO3结晶析出
【答案】D
【解析】
A. 将金属钠放入CuSO4溶液中,钠先与水反应生成NaOH,NaOH再与CuSO4反应;
B. 1molNa2O2中存在2molNa+和1molO22-;
C. “侯氏制碱法”中的碱为Na2CO3
D. 相同条件下NaHCO3的溶解度小于Na2CO3的溶解度。
A. 钠与硫酸铜溶液反应,生成氢氧化铜沉淀、硫酸钠和氢气,离子方程式:Cu2++2Na+2H2O=Cu(OH)2↓+2Na++H2↑,A项错误;
B. 7.8 g Na2O2物质的量为:![]() =0.1mol,含有0.2mol Na+,0.1mol O22-,共含离子数为0.3NA,B项错误;
=0.1mol,含有0.2mol Na+,0.1mol O22-,共含离子数为0.3NA,B项错误;
C. “侯氏制碱法”中的碱为Na2CO3,C项错误;
D. Na2CO3+H2O+CO2=2NaHCO3,相同条件下NaHCO3的溶解度小于Na2CO3的溶解度,因此向Na2CO3饱和溶液中通入CO2,有NaHCO3结晶析出,D项正确;
答案选D。
生成气体型 | 钠与NH4Cl溶液反应生成H2和NH3 |
生成沉淀型 | 钠与铜盐、铁盐等溶液反应生成Cu(OH)2或Fe(OH)3 |
复杂型 | 钠与AlCl3稀溶液反应,如果钠量较多,则先生成Al(OH)3沉淀,后沉淀溶解 |


科目:高中化学 来源: 题型:
【题目】已知三种有机物 ![]() (x)
(x) ![]() (y)
(y)![]() (z),下列说法不正确的是
(z),下列说法不正确的是
A.x、y、z 互为同分异构体,z 的二氯代物有三种
B.x、y 的一氯代物均只有三种,z 的一氯代物有一种
C.x、y 可使溴的四氯化碳溶液因发生加成反应而褪色
D.x、y、z 中只有 x 的所有原子可能处于同一平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、Q、R为原子序数依次增大的短周期元素。25℃时,其最高价氧化物的水化物溶液(浓度均为0.001mol·L-1)的pH和原子半径的关系如图所示。下列说法中正确的是( )
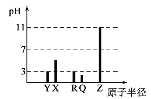
A.Y和Z的简单离子半径:Y<Z
B.R、Q的气态氢化物的稳定性:R>Q
C.R的最高价氧化物对应水化物的化学式为HRO3
D.上述五种元素中有两种元素是金属元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对有机物结构的叙述中不正确的是
A.乙烯、溴苯分子中的所有原子均共平面
B.在有机物分子中,含有的氢原子个数一定是偶数
C.![]() 属于同种物质,说明苯分子中6个碳原子之间的键是完全一样的
属于同种物质,说明苯分子中6个碳原子之间的键是完全一样的
D.CH2Cl2只有一种结构说明甲烷分子是正四面体结构,而不是平面正方形结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素W、X、Y、Z的原子序数依次增大。其中X与Y可形成一种淡黄色物质P,常温下将0.05 mol P溶于水,配成1 L溶液,其中![]() ;Z为金属元素,且Z可在W的一种氧化物中燃烧,生成一种白色的物质和一种黑色的物质。下列说法错误的是()
;Z为金属元素,且Z可在W的一种氧化物中燃烧,生成一种白色的物质和一种黑色的物质。下列说法错误的是()
A. 氢化物的沸点:W<X
B. 简单离子半径:X>Y>Z
C. 化合物P中既含有离子键又含有共价键
D. W、X、Y三种元素形成的物质的水溶液显碱性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】端炔烃在催化剂存在下可发生偶联反应,称为Glaser反应。2R—C≡C—H![]() R—C≡C—C≡C—R+H2。该反应在研究新型发光材料、超分子化学等方面具有重要价值。下面是利用Glaser反应制备化合物E的一种合成路线:
R—C≡C—C≡C—R+H2。该反应在研究新型发光材料、超分子化学等方面具有重要价值。下面是利用Glaser反应制备化合物E的一种合成路线:
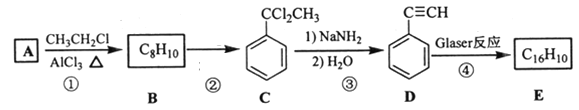
回答下列问题:
(1)B的结构简式为_____,反应②所需的试剂和条件是______,反应③的反应类型为______反应。
(2)1molE理论上最多消耗氢气_____mol。
(3)芳香化合物F是C的同分异构体,其分子中只有两种不同化学环境的氢,数目比为3:1,写出任意一种的结构简式______。
(4)写出用2苯基乙醇![]() )为原料(其他无机试剂任选)制备化合物D的合成路线______。
)为原料(其他无机试剂任选)制备化合物D的合成路线______。
(合成路线常用的表达方式为:A![]() B
B![]() ……目标产物)
……目标产物)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸钴可用于指示剂和催化剂的制备。用水钴矿(主要成分为Co2O3,含少量Fe2O3、A12O3、MnO、MgO、CaO、SiO2等)制取CoC2O4·2H2O工艺流程如下
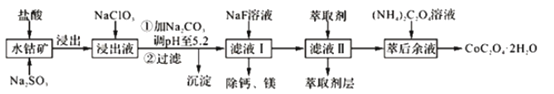
已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Ca2+、Mg2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见表:
沉淀物 | Fe(OH)3 | Al(OH)3 | Co(OH)2 | Fe(OH)2 | Mn(OH)2 |
完全沉淀的pH | 3.7 | 5.2 | 9.2 | 9.6 | 9.8 |
(1)CoC2O4·2H2O中C的化合价是____________________________。
(2)写出浸出过程中Na2SO3与Co2O3发生反应的离子方程式:______________。
(3)浸出液中加入NaClO3的目的是____________________________。
(4)加Na2CO3能使浸出液中某些金属离子转化成氢氧化物沉淀,沉淀除Al(OH)3外,还有的成分是______________(填化学式),试用离子方程式和必要的文字简述其原理:____________________________。
(5)萃取剂对金属离子的萃取率与pH的关系如图,萃取剂的作用是______________;其使用的适宜pH范围是______________。
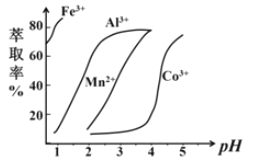
A. 2.02.5
B. 3.03.5
C. 4.04.5
(6)滤液I“除钙、镁”是将其转化为MgF2、CaF2沉淀。己知Ksp(MgF2)=7.35×10-11、Ksp(CaF2)=1.05×10-10,当加入过量 NaF后,所得滤液 c(Mg2+)/c(Ca2+) =______________。
(7)用m1kg水钴矿(含Co2O360%)制备CoC2O4·2H2O,最终得到产品m2kg,产率(实际产量/理论产量×100%)为____________________________。(已知:M(Co2O3)=166, M(CoC2O4·2H2O)=183,仅需列出数字计算式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaCl和NaClO在酸性条件下可发生反应:ClO-+Cl-+2H+=Cl2↑+H2O,某学习小组拟研究消毒液(主要成分为NaCl和NaClO)的变质情况。
(1)此消毒液中NaClO可吸收空气中的CO2生成NaHCO3和HClO。写出化学反应方程式___。
(2)取适量消毒液放在试管中,加入足量一定浓度的硫酸,有气体放出。通过以下装置检验气体的成分可以判断消毒液是否变质。
限选试剂:98%浓硫酸、1%品红溶液、1.0mol·L-1KI淀粉溶液、1.0mol·L-1NaOH溶液、澄清石灰水、饱和NaCl溶液。
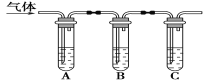
请完成下列实验方案。
所加试剂 | 预期现象和结论 |
试管A中加足量①___; 试管B中加1%品红溶液; 试管C中加②___。 | 若A中溶液变蓝色,B中溶液不褪色,C中溶液变浑浊,则消毒液部分变质;③___,则消毒液未变质;④___,则消毒液完全变质。 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜板上铁铆钉长期暴露在潮湿的空气中,形成一层酸性水膜后铁铆钉会被腐蚀,示意图如下。下列说法不正确的是
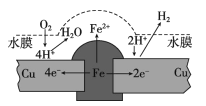
A. 腐蚀过程中铜极上始终只发生: 2H++2e-= H2↑
B. 若水膜中溶有食盐将加快铁铆钉的腐蚀
C. 若在金属表面涂一层油脂能防止铁铆钉被腐蚀
D. 若将该铜板与直流负极相连,则铁铜均难被腐蚀
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com