
| A、硅酸凝胶干燥后可作实验室、袋装食品和瓶装药品的干燥剂 |
| B、硅可做半导体材料 |
| C、二氧化硅是现代光学及光纤制品的基本原料 |
| D、碳化硅是做电子组件的材料 |


 快乐5加2金卷系列答案
快乐5加2金卷系列答案科目:高中化学 来源: 题型:
| 元素编号 | 元素性质或原子结构 |
| T | M层上有3个未成对电子 |
| X | 3p能级上有一个空轨道 |
| Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| Z | 元素最高正价是+7价 |
| W | 3d能级上只有1对成对电子 |

查看答案和解析>>
科目:高中化学 来源: 题型:
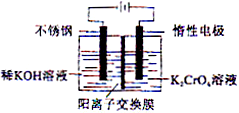 (1)Na2SO3和Na2S是硫元素的两种重要化合物,请回答下列问题:
(1)Na2SO3和Na2S是硫元素的两种重要化合物,请回答下列问题:
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、HNO3 |
| B、NaHSO4 |
| C、H2SO4 |
| D、HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 化学式 | AgCl | AgBr | AgI |
| 颜 色 | 白色 | 浅黄色 | 黄色 |
| Ksp | 2.0×10-10 | 5.4×10-13 | 8.3×10-17 |
| c(Br-) |
| c(Cl-) |
+ 4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
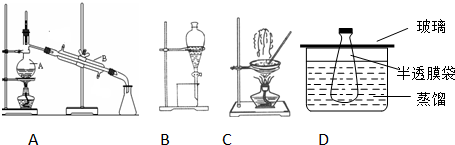
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com