
| A. | 等物质的量浓度的下列溶液:①H2CO3、②Na2CO3、③NaHCO3、④(NH4)2CO3:其中c(CO32-)的大小关系为:②>④>③>① | |
| B. | pH=2 的H2C2O4溶液与pH=12的NaOH溶液等体积混合:c(Na+)+c(H+)=c(OH-)+c(HC2O4-)+c(C2O42-) | |
| C. | 向0.2 mol•L-1NaHCO3 溶液中加入等体积0.1 mol•L-1NaOH 溶液:c(CO32-)>c(HCO3-)>c(OH-)>c(H+) | |
| D. | 常温下,同浓度的CH3COONa与CH3COOH 溶液等体积混合,溶液的pH<7:c(CH3COOH)+c(OH-)>c(Na+)+c(H+) |
分析 A.H2CO3为二元弱酸,不稳定,加热易分解,碳酸为弱电解质,在水溶液中分两步电离,以第一步为主;
B.pH=2 的H2C2O4溶液与pH=12的NaOH溶液等体积混合,溶液中存在电荷守恒;
C.向0.2 mol•L-1NaHCO3 溶液中加入等体积0.1 mol•L-1NaOH 溶液得到等浓度的碳酸钠和碳酸氢钠溶液,溶液中碳酸根离子水解程度大于碳酸氢根离子;
D.常温下,同浓度的CH3COONa与CH3COOH 溶液等体积混合,溶液的pH<7,溶液显酸性,醋酸电离大于醋酸根离子的水解,电荷守恒分析判断.
解答 解:A.②④相比较,④发生互促水解,c(CO32-)的大小为②>④,③以水解为主,c(CO32-)较小,①为二元弱酸,c(CO32-)最小,则c(CO32-)的大小关系为Na2CO3>(NH4)2CO3>NaHCO3>H2CO3,②④③①,故A正确;
B.pH=2 的H2C2O4溶液与pH=12的NaOH溶液等体积混合:c(Na+)+c(H+)=c(OH-)+c(HC2O4-)+2c(C2O42-),故B错误;
C.向0.2 mol•L-1NaHCO3 溶液中加入等体积0.1 mol•L-1NaOH 溶液得到等浓度的碳酸钠和碳酸氢钠溶液,溶液中碳酸根离子水解程度大于碳酸氢根离子,溶液显碱性,离子浓度大小为:c(HCO3-)>c(CO32-)>c(OH-)>c(H+),故C错误;
D.常温下,同浓度的CH3COONa与CH3COOH 溶液等体积混合,溶液的pH<7,溶液显酸性,醋酸电离大于醋酸根离子的水解,离子浓度大小为:c(CH3COOH)<c(CH3COO-),电荷守恒为:c(CH3COO-)+c(OH-)=c(Na+)+c(H+),c(CH3COOH)+c(OH-)<c(Na+)+c(H+),故D错误;
故选A.
点评 本题考查了电解质溶液中离子浓度大小比较、电荷守恒分析,盐类水解的应用,注意混合溶液中电离和水解程度大小的比较判断,题目难度中等.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
| 实验步骤 | 实验目的 |
| (滴定前的所有操作正确,已略去) 步骤1: ①用碱式滴定管量取20.00mL的氨水放入锥形瓶中,滴入2滴甲基橙. ②用酸式滴定管取0.1000mol/L盐酸滴定氨水. ③当锥形瓶中的溶液由黄色变成橙色时,停止滴定,纪录数据. ④重复滴定操作2~3次. | 测定氨水的准确浓度 |
| 步骤2:用pH计测定氨水的pH. | 测定氨水中c(OH-)浓度 |
| 步骤3:通过实验数据计算氨水的电离常数K | |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
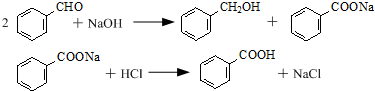
| 名称 | 相对密度 | 熔点(℃) | 沸点(℃) | 溶解度 | |
| 水 | 乙醚 | ||||
| 苯甲醛 | 1.04 | -26 | 179.6 | 微溶 | 易溶 |
| 苯甲酸 | 1.27 | 122.1 | 249 | 25℃微溶,95℃可溶 | 易溶 |
| 苯甲醇 | 1.04 | -15.3 | 205.7 | 微溶 | 易溶 |
| 乙醚 | 0.71 | -116.3 | 34.6 | 不溶 | -- |

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 二氧化硅熔点高,硬度大,存在于水泥、陶瓷中 | |
| B. | 二氧化硅用于制造晶体管、集成电路 | |
| C. | 二氧化硅用于制造石英钟表的压电材料和光导纤维 | |
| D. | 二氧化硅是酸性氧化物,它不溶于任何酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
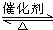 N2+4NH3;为抑制肼的分解,可采取的合理措施有降低反应温度(任写一种).
N2+4NH3;为抑制肼的分解,可采取的合理措施有降低反应温度(任写一种).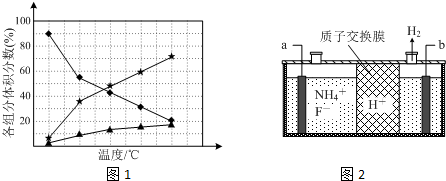
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | “静电除尘”、“汽车尾气的催化净化”都有利于提高空气质量 | |
| B. | 减少化石燃料的使用,有利于降低空气中PM2.5的含量 | |
| C. | 食品包装袋中常放入小袋的生石灰,目的是防止食品氧化变质 | |
| D. | 医用酒精是用淀粉类植物发酵经蒸馏制成,浓度通常是75% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2CH3CH2OH+2Na→2CH3CH2ONa+H2↑(取代反应) | |
| B. | CH2═CH2+H2O$\stackrel{催化剂}{→}$CH3CH2OH(加成反应) | |
| C. | CH3COOH+CH3CH2OH$?_{△}^{浓H_{2}SO_{4}}$CH3COOCH2CH3+H2O(取代反应) | |
| D. | 2CH3CH2OH+O2$→_{△}^{催化剂}$2CH3CHO+2H2O(加成反应) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
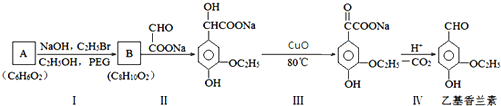
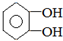 .
.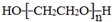 .若PEG的平均相对分子质量为17618,则其平均聚合度约为400.
.若PEG的平均相对分子质量为17618,则其平均聚合度约为400.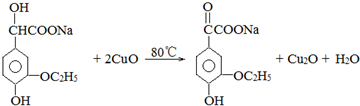 .
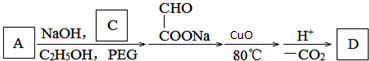
.
 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com