
【题目】现有短周期元素R、X、Y、Z、T,R与T原子最外层电子数均是电子层数的2倍,Y元素能与大多数金属和非金属元素形成化合物;Z+与Y2-电子层结构相同。五种元素的原子半径如图所示,下列推断正确的是

A. Y、Z组成的化合物只含离子键
B. 氢化物的沸点:R<X<Y
C. T的最高价氧化物的水化物酸性比R的强
D. Y和Z分别与T、X组成的二元化合物的水溶液一定呈中性
科目:高中化学 来源: 题型:
【题目】现有反应:
A.CaCO3 ![]() CaO+CO2↑
CaO+CO2↑
B.Zn+H2SO4=ZnSO4+H2↑
C.C+CO2 ![]() 2CO
2CO
D.2KOH+H2SO4═K2SO4+2H2O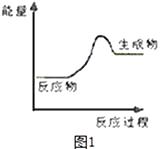
(1)上述四个反应中属于氧化还原反应且反应过程中能量变化符合图1的是(填反应序号).
(2)在常温下,上述四个反应中可用于设计原电池的是(填反应序号),根据该原电池回答下列问题:
①负极材料是 , 负极发生(填“氧化”或“还原”)反应;正极反应式为 .
②当导线中有1mol电子通过时,理论上发生的变化是(填序号). (相对原子质量:H1,Zn65)
a.溶液增重32.5g b.溶液增重31.5g
c.析出1g H2 d.析出11.2LH2
(3)对于反应B,将足量且等量的形状相同的锌块分别加入到等浓度等体积的两份稀硫酸X、Y中,同时向X中加入少量饱和CuSO4溶液,发生反应生成氢气的体积(V)与时间(t)的关系如图2所示. 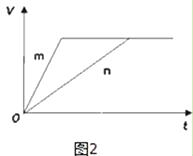
①m曲线表示锌与稀硫酸(填“X”或“Y”)反应.
②锌分别与稀硫酸X、Y反应时,反应速率不同的原因是(填序号).
a.CuSO4作催化剂
b.加入硫酸铜溶液增大了c(SO42﹣)
c.Zn首先与Cu2+反应,生成的Cu与Zn、稀硫酸构成原电池
d.加入硫酸铜溶液增大了溶液体积.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质互为同分异构体的一组是 ( )
A. 35Cl和37Cl B. H2O和H2O2
C. O2和O3 D. CH3CH2OH和CH3OCH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】黄铜矿不仅可用于火法炼铜,也可用于湿法炼铜,湿法可同时生产铜、磁性氧化铁和用于橡胶工业的一种固体物质A,流程如下:
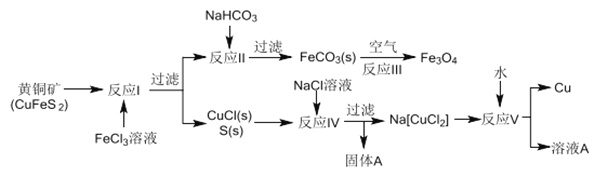
(1)黄铜矿中Cu 的化合价是______,反应I中65gFeC13 可氧化________mol CuFeS2。
(2)工业生产中的过滤操作多采用倾析法分离出固体物质,下列适合用倾析法的有______。
A.沉淀的颗粒较大 B.沉淀容易沉降 C.沉淀呈胶状 D.沉淀呈絮状
(3)在反应Ⅱ中,计算NaHCO3饱和溶液(其中CO32-平衡浓度为1.2×10-3mol/L)可产生FeCO3沉淀时的最小Fe2+浓度是_________(己知FeCO3的Ksp=3.0×10-11)
(4)反应Ⅲ是在设备底部鼓入空气,高温氧化锻烧法来制备磁性氧化铁,写出对应的化学方程式_________________。
(5)固体物质A的成分________(写名称)。
(6)潮湿的FeCO3固体若不及时灼烧处理会在空气中逐渐变红,写出相关的化学方程式:_______________。
(7)本流程中可实现循环使用的物质除了水外,还有_____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Fenton试剂常用于氧化降解有机污染物X。在一定条件下,反应初始时c(X)=2.0×10-3mol·L-1,反应10 min进行测定,得图1和图2。下列说法不正确的是
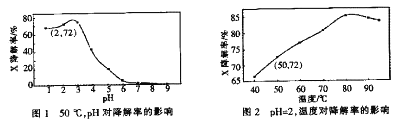
A. 50oC,PH在3~6之间,X降解率随pH增大而减小
B. pH=2,温度在40~80oC,X降解率随温度升高而增大
C. 无需再进行后续实验,就可以判断最佳反应条件是:PH=3、温度为80oC
D. pH=2、温度为50oC,10min内v(X)=1.44x10-4mol·L-1min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用氟硼酸(HBF4,属于强酸)代替硫酸作铅蓄电池的电解质溶液,可使铅蓄电池在低温下工作时的性能更优良,反应方程式为:Pb+PbO2+4HBF4![]() 2Pb(BF4)2+2H2O,Pb(BF4)2为可溶于水的强电解质,下列说法正确的是
2Pb(BF4)2+2H2O,Pb(BF4)2为可溶于水的强电解质,下列说法正确的是
A. 放电时,负极反应为:PbO2+4HBF4-2e-=Pb(BF4)2+2BF4-+2H2O
B. 充电时,当正极质量减少23.9g时转移0.2mol电子
C. 放电时,PbO2电极附近溶液的pH增大
D. 充电时,Pb电极的电极反应式为PbO2+4H++2e-=Pb2++2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化硫酰(SO2C12)主要用作氯化剂。它是一种无色液体,熔点-54.1℃,沸点69.1℃。氯化硫酰可用干燥的二氧化硫和氯气在活性炭催化剂存在下反应制取:SO2(g)+C12(g)![]() SO2C12 (l) △H=-97.3kJ/mol
SO2C12 (l) △H=-97.3kJ/mol
(1)试写出常温常压下化学平衡常数K的表达式:K=____________;若在此条件下,将化学平衡常数K增大,化学反应速率V正也增大,可采取的措施是____________(选填编号)。
a.降低温度 b.移走SO2C12
c.增加反应物浓度 d.以上都不对
(2)为了提高上述反应中Cl2的平衡转化率,下列措施合理的是___________(选选填编号)。
a.缩小容器体积 b.使用催化剂
c.增加SO2浓度 d.升高温度
(3)在100℃时,往上述平衡体系中加入37C12,—段时间后,则平衡体系中含有37C1的物质有_______(选选填编号)。
a.只有37C12 b.只有 SO237Cl2 c. 37C12和SO237Cl2 d.无法判断
(4)下列描述中能说明上述反应己达平衡的是_____________ (选填编号)。
a.v (Cl2) =v (SO2)
b.容器中气体压强不随时间而变化
c.c (Cl2) : c (SO2) =1 : 1
d.容器中气体颜色不随时间而变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有100mL含Cu2+、Al3+、NH4+、H+、Cl-的溶液,向该溶液中逐滴加入2.5mol·L-1NaOH溶液,所加NaOH 溶液的体积(mL)与产生沉淀的物质的量(mol)关系如下图所示:

(1)B点的沉淀物的化学式为______________。
(2)原溶液中Cu2+的物质的量为______,原溶液中Cl-物质的量浓度为__________。
(3)原溶液的pH=__________,x-y= _________。
(4)经过滤得到D点的沉淀物,并多次用蒸馏水洗涤沉淀,判断沉淀是否洗涤干净的方法是_________________________________________________________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com