
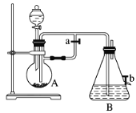
【题目】如图所示装置,可用来制取和观察Fe(OH)2在空气中被氧化过程中的颜色变化。实验时必须使用铁屑和6 mol·L1的硫酸,其他试剂任选。
请回答下列问题:
(1)B中盛有一定量的NaOH溶液,A中应预先加入的物质是__________________,A中反应的离子方程式是____________________________________________________。
(2)实验开始时应先将活塞a________(填“打开”或“关闭”)。其目的是____________________。
(3)简述生成Fe(OH)2的操作过程:__________________________________________。
(4)实验完毕,打开b处活塞,放入一部分空气,此时B中发生反应的化学方程式为_________________。
(5)图中________(填“能”或“不能”)较长时间看到Fe(OH)2白色沉淀。
【答案】铁屑 Fe+2H+===Fe2++H2↑打开排出装置中的空气首先打开a,让分液漏斗中酸液流下,使A中产生的H2通入B中,一段时间后关闭a,烧瓶中压强增大,A中液体沿导管流入B中,产生少量白色沉淀4Fe(OH)2+O2+2H2O===4Fe(OH)3能
【解析】
打开活塞a,先在烧瓶A中加入Fe粉,通过分液漏斗向烧瓶A中滴加无挥发性的稀硫酸,这时发生反应:Fe+2H +=Fe2++H2↑。产生的氢气把锥形瓶B中是NaOH溶液里的空气驱赶掉。使B中处于氢气的环境中。关闭活塞b。再关闭活塞a, 由于A中不断产生氢气,使得A中的压强越来越大。这时A中产生的氢气将A装置中的FeSO 4溶液通过导气管压入B中,发生反应Fe2++2OH -=Fe(OH) 2↓。由于整个装置都处于H 2的还原性环境中,所以可以较长时间的观察的Fe(OH) 2的白色沉淀。当实验完毕,打开b处活塞,空气进入到装置B中,此时B瓶中发生反应的化学方程式为:4Fe(OH) 2+O 2+2H 2O=4Fe(OH) 3。会看到:白色沉淀逐渐变成灰绿色,最后变成红褐色;说明Fe(OH) 2不稳定,容易被空气中的氧气氧化为红褐色的Fe(OH)3。
(1) 打开活塞a,先在烧瓶A中加入Fe粉,通过分液漏斗向烧瓶A中滴加无挥发性的稀硫酸,这时发生反应:Fe+2H+=Fe2++H2↑;
(2) 打开活塞a,先在烧瓶A中加入Fe粉,通过分液漏斗向烧瓶A中滴加无挥发性的稀硫酸,产生的氢气把锥形瓶B中是NaOH溶液里的空气驱赶掉;
(3) 首先打开a,让分液漏斗中酸液流下,使A中产生的H2通入B中,一段时间后关闭a,烧瓶中压强增大,A中液体沿导管流入B中,产生少量白色沉淀;
(4) 当实验完毕,打开b处活塞,空气进入到装置B中,此时B瓶中发生反应的化学方程式为:4Fe(OH) 2+O 2+2H 2O=4Fe(OH) 3;
(5) 首先打开a,让分液漏斗中酸液流下,使A中产生的H2通入B中,一段时间后关闭a,烧瓶中压强增大,A中液体沿导管流入B中,产生少量白色沉淀,此时仪器中不含有氧气,因此能较长时间看到Fe(OH)2白色沉淀。


科目:高中化学 来源: 题型:
【题目】关于氯化镁溶液和氢氧化铁胶体的说法中正确的是( )
A.溶液是电中性的,胶体是带电的
B.两者的分散质微粒均能透过半透膜和滤纸
C.溶液中溶质分子的运动有规律,胶体中分散质粒子的运动无规律,即布朗运动
D.一束光线分别通过溶液和胶体时,后者会出现明显的“光亮的通路”,前者则没有
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一无色溶液,其中可能含有![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 等离子中的几种,为分析其成分,取此溶液分别进行了四个实验,其操作和有关现象如下:
等离子中的几种,为分析其成分,取此溶液分别进行了四个实验,其操作和有关现象如下:

第③个实验中,生成白色沉淀的量与加入![]() 的量有如下图所示的相互关系。据此可知:
的量有如下图所示的相互关系。据此可知:

(1)在原溶液中一定存在的离子有______;一定不存在的离子有______;不能确定是否存在的离子有______。
(2)写出第③个实验中发生反应的离子方程式____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】菲索菲那定(E)可用于减轻季节性过敏鼻炎引起的症状,其合成路线如下(其中R—为![]() ):
):

(1)A的名称是_______。C中含氧官能团的名称是_______。
(2)D的结构简式是_______。
(3)流程图中属于取代反应的是_______(填数字编号)。
(4)反应②的化学方程式是_______。
(5)G是B的同系物,分子式为C8H8O2,G的结构有_______种。其中,核磁共振氢谱吸收峰面积之比为1:2:2:2:1的结构简式是_______。
(6)已知: ,请以丙酮(CH3COCH3)、乙醇为原料制备A,写出相应的合成路线流程图(无机试剂任选)_______。
,请以丙酮(CH3COCH3)、乙醇为原料制备A,写出相应的合成路线流程图(无机试剂任选)_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将NaOH溶液滴加到某一元酸(HA)溶液中,测得混合溶液的pH与离子浓度变化关系如下图所示【已知:P[c(A-)/c(HA)]=-1g[c(A-)/c(HA)]】。下列叙述不正确的是
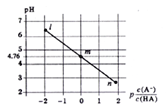
A. Ka(HA)的数量级为10-5
B. 滴加NaOH溶液过程中,c(A-)/[c(HA)×c(OH-)]保持不变
C. m点所示溶液中:c(H+)=c(HA)+c(OH-)-c(Na+)
D. n点所示溶液中:c(Na+)=c(A-)+c(HA)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】若在加入铝粉能放出氢气的溶液中,分别加入下列各组离子,可能共存的是( )
A.NH4+、CO32﹣、K+、Na+
B.Na+、Ba2+、Cl﹣、HCO3﹣
C.NO3﹣、Cu2+、K+、SO42﹣
D.K+ , Na+ , Cl﹣ , NO3﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A.同温同压下,相同体积的物质,其物质的量一定相等
B.任何条件下,等物质的量的甲烷和一氧化碳所含的分子数一定相等
C.1L一氧化碳气体一定比1L氧气的质量小
D.相同条件下的一氧化碳气体和氮气,若物质的量相等则体积相等,但质量不相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A. 0.1 mol·L-1的Na2CO3溶液中:c(OH-)=c(HCO![]() )+c(H+)+c(H2CO3)
)+c(H+)+c(H2CO3)
B. 25 ℃时,用醋酸溶液滴定等浓度NaOH溶液至pH=7,V醋酸<VNaOH
C. 常温下将10mlpH=4的醋酸溶液稀释至100ml,所得溶液4<pH<5
D. 向NaAlO2溶液中滴加NaHCO3溶液相互促进水解,有沉淀和气体生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室需要配制0.1 mol·L-1CuSO4溶液480 mL。按下列操作步骤填上适当的文字,以使整个操作完整。
(1)选择仪器。完成本实验所必需的仪器有:托盘天平(精确到0.1 g)、药匙、烧杯、量筒、玻璃棒、________、________以及等质量的两片滤纸。
(2)计算,应选择下列________。
A.需要CuSO4固体8 g B.需要CuSO4固体7.7 g
C.需要CuSO4·5H2O晶体12.5 g D.需要CuSO4·5H2O晶体12.0 g
(3)称量。所用砝码生锈则所配溶液的浓度会_____(填“偏高”“偏低”或“无影响”。
(4)溶解、冷却,该步实验中需要使用玻璃棒,目的是____________________。
(5)转移、洗涤。在转移时应使用________引流,需要洗涤烧杯2~3次是为了________。
(6)定容,摇匀。
(7)将配好的溶液静置一段时间后,倒入指定的试剂瓶,贴好标签,注明配制的时间、溶液名称及浓度。
(8)在配制过程中,某学生观察定容时液面情况如图所示,所配溶液的浓度会________(填“偏高”“偏低”或“无影响”)。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com