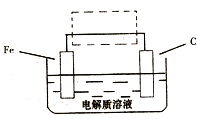
(2010?临沂一模)Fe元素是地壳中最丰富的元素之一,在金属中仅次于铝,铁及其化合物在生活、生产中有广泛应用.请回答下列问题:
(1)磁铁矿是工业上冶炼铁的原料之一,其原理是Fe
30
4+4CO
3Fe+4C0
2,若有1mol Fe
30
4参加反应,转移电子的物质的量是
8
8
mol;
(2)与明矾相似,硫酸铁也可用作净水剂,在使用时发现硫酸铁并不能使酸性废水中的悬浮物沉降除去,其原因是
因酸性废液中,将会Fe3+抑制的水解,无法得到Fe(OH)3胶体,故不能够吸附悬
因酸性废液中,将会Fe3+抑制的水解,无法得到Fe(OH)3胶体,故不能够吸附悬
;
(3)钢铁的电化腐蚀简单示意图如右,将该图稍作修改即可成为钢铁电化学防护的简单示意图,请在下图虚线框内作出修改,并用箭头标出电子流动方向
;
(4)硫酸亚铁晶体(FeS0
4?7H
20)常作医药上的补血剂.课外研究性小组测定该补血剂中铁元素的含量.实验步骤如下:
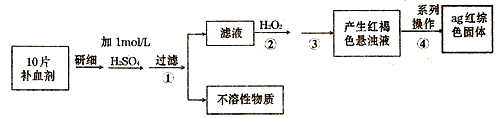
请回答下列问题:
①证明步骤①所得滤液中含有Fe
2+的方法是先滴加KSCN溶液,再滴加H
2O
2,此过程的现象为:
H2O2溶液由浅绿色变为血红色
H2O2溶液由浅绿色变为血红色
;
②若该实验温度下,步骤③中难溶物的溶度积为Ksp=8×l0
-38,试计算该物质沉淀完全所需要的pH=
3.3
3.3
(已知溶液中离子浓度小于10
-5mol时,该离子可看做沉淀完全;lg2=0.3);
③步骤④中一系列的操作步骤为:过滤、
洗涤
洗涤
、灼烧、冷却、称量;
④若实验过程中无损耗,最后称量得到a克红棕色的固体,则每片补血剂中含铁元素的质量为
0.07a
0.07a
g.(用含a的式子表示)

 (2010?临沂一模)Fe元素是地壳中最丰富的元素之一,在金属中仅次于铝,铁及其化合物在生活、生产中有广泛应用.请回答下列问题:
(2010?临沂一模)Fe元素是地壳中最丰富的元素之一,在金属中仅次于铝,铁及其化合物在生活、生产中有广泛应用.请回答下列问题:


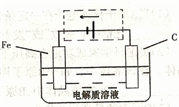 ,故答案为:
,故答案为: ;
;

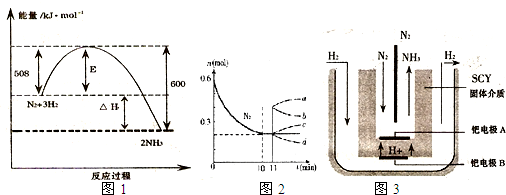
 (2010?临沂一模)某化学学习小组为研究HA、HB和MOH的酸碱性的相对强弱,设计以下实验以下实验:将pH═2的两种酸溶液HA,HB和pH=12的MOH碱溶液各1mL,分别加水稀释到1000mL,其pH的变化与溶液体积的关系如图,根据所给的数据,请回答下列问题:
(2010?临沂一模)某化学学习小组为研究HA、HB和MOH的酸碱性的相对强弱,设计以下实验以下实验:将pH═2的两种酸溶液HA,HB和pH=12的MOH碱溶液各1mL,分别加水稀释到1000mL,其pH的变化与溶液体积的关系如图,根据所给的数据,请回答下列问题: