
【题目】已知:A是石油裂解气的主要产物之一,其产量常用于衡量一个国家石油化工发展水平的标志。下列是有机物A~G 之间的转化关系:
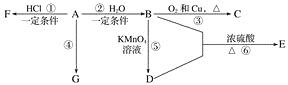
请回答下列问题:
(1)A的官能团的名称是_____;C的结构简式是_____。
(2)E是一种具有香味的液体,由B+D→E的反应方程式为_______,
(3)比赛中,当运动员肌肉挫伤或扭伤时,随队医生即对准受伤部位喷射物质F(沸点12.27℃)进行应急处理。写出由A制F的化学方程式:________。
(4)E的同分异构体能与NaHCO3溶液反应,写出该同分异构体的结构简式:______。
【答案】碳碳双键 CH3CHO CH3CH2OH+CH3COOH![]() CH3COOCH2CH3+H2O CH2=CH2+HCl
CH3COOCH2CH3+H2O CH2=CH2+HCl ![]() CH3CH2Cl CH3CH2CH2COOH、(CH3)2CHCOOH
CH3CH2Cl CH3CH2CH2COOH、(CH3)2CHCOOH
【解析】
A是石油裂解气的主要产物之一,它的产量常用来衡量一个国家石油化工水平,则A是乙烯。乙烯和水发生加成反应生成B,则B是乙醇,乙醇和氧气在铜作催化剂作用下反应生成C,则C是乙醛,乙醇在高锰酸钾作用下生成D,D是乙酸,乙醇和乙酸在浓硫酸作用下发生酯化反应生成E,E是乙酸乙酯;乙烯和氯化氢加成得到F,F为氯乙烷,据此分析解答。
(1)由以上分析可知A为乙烯,结构简式为:CH2=CH2,含有C=C双键;C是乙醛,乙醛的结构简式为CH3CHO,故答案为:碳碳双键;CH3CHO;
(2)E是一种具有香味的液体,为乙酸乙酯,B是乙醇,乙醇在高锰酸钾作用下生成D,D为乙酸,乙醇和乙酸在浓硫酸作用下发生酯化反应CH3CH2OH+CH3COOH ![]() CH3COOCH2CH3+H2O,故答案为:CH3CH2OH+CH3COOH
CH3COOCH2CH3+H2O,故答案为:CH3CH2OH+CH3COOH![]() CH3COOCH2CH3+H2O;
CH3COOCH2CH3+H2O;
(3)F为A乙烯和氯化氢反应的产物,乙烯和氯化氢在一定条件下发生加成反应生成氯乙烷,反应的化学方程式为:CH2=CH2+HCl ![]() CH3CH2Cl,故答案为:CH2=CH2+HCl
CH3CH2Cl,故答案为:CH2=CH2+HCl ![]() CH3CH2Cl;
CH3CH2Cl;
(4)E为CH3COOCH2CH3,E的同分异构体能与NaHCO3反应,应含有羧基,结构简式为CH3CH2CH2COOH或(CH3)2CHCOOH,故答案为:CH3CH2CH2COOH、(CH3)2CHCOOH。


 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案科目:高中化学 来源: 题型:
【题目】已知某反应aA(g)+bB(g)![]() cC(g)△H="Q" 在密闭容器中进行,在不同温度(T1和T2)及压强(P1和P2)下,混合气体中B的质量分数w(B)与反应时间(t)的关系如图所示,下列判断正确的是( )
cC(g)△H="Q" 在密闭容器中进行,在不同温度(T1和T2)及压强(P1和P2)下,混合气体中B的质量分数w(B)与反应时间(t)的关系如图所示,下列判断正确的是( )

A. T1<T2,P1<P2,a+b>c,Q<0
B. T1>T2,P1<P2,a+b<c,Q>0
C. T1<T2,P1>P2,a+b<c,Q>0
D. T1<T2,P1>P2,a+b>c,Q<0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.现有以下物质:①NaCl固体;②液态CO2;③液态氯化氢;④汞;⑤固体BaSO4;⑥蔗糖;⑦酒精;⑧熔融的Na2CO3,请回答下列问题:
(1)以上物质中能导电的是____;
(2)以上物质属于电解质的是____;
(3)以上物质属于非电解质的是____;
(4)以上物质溶于水后形成的溶液能导电的是_____;
(5)属于盐的有____;
(6)写出⑧溶于水中的电离方程式____。
Ⅱ.在一定条件下,有下列物质:①8gCH4②6.02×1023个HCl分子③2molO2。按由小到大的顺序填写下列空白(填写序号):
(1)摩尔质量____;(2)物质的量_____;
(3)分子数目_____;(4)原子数目____;
(5)质量_____。
III.(1)分离胶体和溶液常用的方法叫____;
(2)等质量的O2和O3所含原子个数比为____;
(3)若ag某气体中含有的分子数为b,则cg该气体在标准状况下的体积是____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一学生设计入图所示装置进行NaHCO3的分解,并证实产物中有CO2产生。

(1)试管中发生的化学反应方程式是____________________________。
(2)指出该学生设计的装置图的错误之处,并改正(文字说明即可)(至少2处)____________。
(3)烧杯中发生反应的离子方程式是_______________________________。
(4)如果将16.8gNaHCO3加热一段时间,然后将剩余固体溶于水,并加入足量的CaCl2溶液,最终得到白色沉淀5.0g,则NaHCO3分解百分率为______________,加CaCl2后反应的离子方程式为____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应进行分类时,既属于氧化还原反应又属于置换反应的是 ( )
A. CH4+2O2![]() CO2+2H2O B. 2KClO3
CO2+2H2O B. 2KClO3![]() 2KCl+3O2↑
2KCl+3O2↑
C. S+O2![]() SO2 D. 8NH3+3Cl2=6NH4Cl+N2↑
SO2 D. 8NH3+3Cl2=6NH4Cl+N2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列有关说法正确的是
A. 1mol/L NaCl 的溶液中含有NA个钠离子
B. 标准状况下,22.4L SO3中含有SO3分子数为NA
C. 1molFe与1molCl2充分反应,转移电子数2NA
D. 1molNa2O2与足量CO2反应,转移的电子数2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】3 mol A和2.5 mol B混合于2 L密闭容器中,发生的反应:3A(g)+B(g)![]() xC(g)+2D(g) 5min后反应达到平衡,容器内压强变小,测得D的平均反应速率为0.1 mol/(L·min),下列结论不正确的是
xC(g)+2D(g) 5min后反应达到平衡,容器内压强变小,测得D的平均反应速率为0.1 mol/(L·min),下列结论不正确的是
A. A的平均反应速率为0.15mol/(L·min)
B. 平衡时,A的转化率为20%
C. 平衡时,C的浓度为 0.25 mol/L
D. 容器内的起始压强和平衡压强之比为11:10
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在三个体积均为2.0 L的恒容密闭容器中发生反应:PCl5(g)![]() PCl3(g)+Cl2(g)。
PCl3(g)+Cl2(g)。
编号 | 温度 /℃ | 起始物质 的量/mol | 平衡物质 的量/mol | 达到平衡 所需时间/s | |
PCl5(g) | PCl3(g) | Cl2(g) | |||
Ⅰ | 320 | 0.40 | 0.10 | 0.10 | t |
Ⅱ | 320 | 0.80 | t1 | ||
Ⅲ | 410 | 0.40 | 0.15 | 0.15 | t2 |
下列说法正确的是
A.平衡常数K:容器Ⅱ>容器Ⅲ
B.反应到达平衡时,PCl5的转化率:容器Ⅱ>容器Ⅰ
C.反应到达平衡时,容器Ⅰ中的平均速率为v(PCl5)=![]() mol·L-1·s-1
mol·L-1·s-1
D.起始时向容器Ⅲ中充入PCl5 0.30 mol、PCl3 0.45 mol和Cl2 0.10 mol,则反应将向逆反应方向进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以甲醇为原料制取高纯H2是重要的研究方向。回答下列问题:
(1)甲醇水蒸气重整制氢主要发生以下两个反应。
主反应:CH3OH(g)+H2O(g)![]() CO2(g)+3H2(g) △H=+49kJ·mol-1
CO2(g)+3H2(g) △H=+49kJ·mol-1
副反应:H2(g)+CO2(g) ![]() CO(g)+H2O(g) △H=+41kJ·mol-1
CO(g)+H2O(g) △H=+41kJ·mol-1
①甲醇在催化剂作用下裂解可得到H2和CO,反应的热化学方程式为__________________,既能加快反应速率又能提高CH3OH平衡转化率的一种措施是_________________________。
②适当增大水醇比[n(H2O):n(CH3OH)],有利于甲醇水蒸气重整制氢,理由是___________。
③某温度下,将n(H2O):n(CH3OH)=1:1的原料气充入恒容密闭容器中,初始压强为p1,反应达到平衡时总压强为p2,则平衡时甲醇的转化率为_________________(忽略副反应)。
(2)工业上常用CH4与水蒸气在一定条件下来制取H2,其反应原理为:CH4(g)+H2O(g)![]() CO(g)+3H2(g) △H=+203kJ·mol-1,在容积为3L的密闭容器中通入物质的量均为3mol的CH4和水蒸气,在一定条件下发生上述反应,测得平衡时H2的体积分数与温度及压强的关系如图所示。
CO(g)+3H2(g) △H=+203kJ·mol-1,在容积为3L的密闭容器中通入物质的量均为3mol的CH4和水蒸气,在一定条件下发生上述反应,测得平衡时H2的体积分数与温度及压强的关系如图所示。
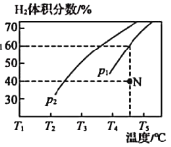
压强为p1时,在N点:v正_______v逆(填“大于”“小于”或“等于”),N点对应温度下该反应的平衡常数K=________mol2·L-2。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com