
【题目】中和热是指酸跟碱发生中和反应生成lmol H2O所放出的热量。某学生想通过测定反应过程中所放出的热量来计算中和热。他将50mL0.5mol/L的盐酸与50mL0.55mol/L的NaOH溶液在如图所示的装置中进行中和反应。请回答下列问题:

(1)从实验装置上看,图中尚缺少的一种玻璃用品是______,烧杯间填满碎塑料泡沫的作用是______。
(2)大烧杯上如不盖硬纸板,则求得的中和热数值_________(填“偏大”、“偏小’、“无影响”)
(3)实验中改用60 mL 0.50 mol/L的盐酸跟50mL 0.55 mol/L的NaOH溶液进形反应,与上述实验相比,所放出的热量________(填“相等”或“不相等”理由是________________;所求中和热的数值会________(填“相等”或“不相等”),理由是_______________________。
【答案】环形玻璃搅拌棒 保温、隔热,减少实验过程中的热最损失 偏小 不相等 因为酸、碱发生中和反应放出的热量与酸、碱的用量有关 相等 中和热是指酸跟碱发生中和反应生成lmol H2O所放出的热量,它与酸、碱的用量无关
【解析】
中和热是在稀溶液中,酸和碱发生中和反应生成1mol水时放出的热量。在实验室里可以用一定量的盐酸和一定量的NaOH溶液发生反应,测定反应放出的热量(依据Q=cmT),再折算成生成1mol水时的热量变化进而确定中和热。酸和碱的量决定着反应放出的热量,但不影响中和热的数值。
(1)为了使酸碱混合均匀,需环形玻璃搅拌棒搅拌,同时为了减少实验过程中的热量损失,应保温、隔热,在烧杯间填满碎塑料泡沫。
(2) 大烧杯上如不盖硬纸板,热量损失,测得的中和热数值偏小;
(3)因为酸、碱发生中和反应放出的热量与酸、碱的用量有关,前者有0.5mol/L×0.050L=0.025mol的酸与碱发生中和反应,后者有0.55mol/L×0.050L=0.0275mol的酸与碱发生中和反应,放出的热量不相等。所求中和热是指酸跟碱发生中和反应生成lmol H2O所放出的热量,它与酸、碱的用量无关,所求中和热数值相等。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】下列属于酯化反应的是( )
A.CH4 + Cl2 ![]() CH3Cl + HCl
CH3Cl + HCl
B.CH2 = CH2 + Br2![]() CH2BrCH2Br
CH2BrCH2Br
C.nCH2 = CH2 ![]()
![]()
D.CH3CH2OH + CH3COOH ![]() CH3COOCH2CH3 + H2O
CH3COOCH2CH3 + H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在25℃条件下将pH=11的氨水稀释100倍后溶液的pH为(填序号)__。
A.9 B.13 C.11~13之间 D.9~11之间
(2)25℃时,向0.1mol/L的氨水中加入少量氯化铵固体,当固体溶解后,测得溶液pH减小,主要原因是(填序号)_______________。
A.氨水与氯化铵发生化学反应 B.氯化铵溶液水解显酸性,增加了c(H+)
C.氯化铵溶于水,电离出大量铵离子,抑制了氨水的电离,使c(OH―)减小
(3)室温下,如果将0.1mol NH4Cl和0.05mol NaOH全部溶于水,形成混合溶液(假设无损失),
①_______________和______________两种粒子的物质的量之和等于0.1mol。
②_______________和______________两种粒子的物质的量之和比OH―多0.05mol。
(4)已知某溶液中只存在OH-、H+、NH4+、Cl-四种离子,某同学推测该溶液中各离子浓度大小顺序可能有如下四种关系:
A.c(Cl-)>c(NH4+)>c(H+)>c(OH-) B.c(Cl-)>c(NH4+)>c(OH-)>c(H+)
C.c(Cl-)>c(H+)>c(NH4+)>c(OH-) D.c(NH4+)>c(Cl-)>c(OH-)>c(H+)
①若溶液中只溶解了一种溶质,该溶质的名称是_________,上述离子浓度大小顺序关系中正确的是(选填序号)________________________。
②若上述关系中C是正确的,则溶液中溶质的化学式是__________________________。
③若该溶液中由体积相等的稀盐酸和氨水混合而成,且恰好呈中性,则混合前c(HCl)(填“>”、“<”、或“=”,下同)____________c(NH3·H2O),混合后溶液中c(NH4+)与c(Cl-)的关系c(NH4+)___________c(Cl-)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼位于ⅢA族,三卤化硼是物质结构化学的研究热点,也是重要的化工原料。三氯化硼(BCl3)可用于制取乙硼烷(B2H6),也可作有机合成的催化剂。
[查阅资料] ①BCl3的熔点为-107.3 ℃,沸点为12.5 ℃;②2B+6HCl![]() 2BCl3↑+3H2↑;③硼与铝的性质相似,也能与氢氧化钠溶液反应。
2BCl3↑+3H2↑;③硼与铝的性质相似,也能与氢氧化钠溶液反应。
[设计实验] 某同学设计如图所示装置制备三氯化硼:

请回答下列问题:
(1)常温下,可用高锰酸钾与浓盐酸发生的反应可替代A装置中的反应,请写出高锰酸钾与浓盐酸反应的离子方程式:_______________________________________________。
(2)E装置的作用是________________________________。如果拆去B装置,可能的后果是______________________________________________________________________。
(3)三氯化硼遇水剧烈反应生成硼酸(H3BO3)和白雾,写出该反应的化学方程式______________________________________________________。实验室保存三氯化硼的注意事项是___________________________________。
(4)实验中可以用一个盛装____________________(填试剂名称)的干燥管代替F和G装置,使实验更简便。
(5)为了顺利完成实验,正确的操作是_____(填序号)。
①先点燃A处酒精灯,后点燃D处酒精灯 ②同时点燃A、D处酒精灯 ③先点燃D处酒精灯,后点燃A处酒精灯
(6)请你补充完整下面的简易实验,以验证制得的产品中是否含有硼粉:取少量样品于试管中,滴加浓________________(填化学式)溶液,若有气泡产生,则样品中含有硼粉;若无气泡产生,则样品中无硼粉。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数的值。下列说法正确的是
A. 18g重水(D2O)所含的电子数目为10NA
B. Na2O2与足量的水反应生成1 molO2,转移电子数目为2NA
C. 100 mL1 molL-1 FeCl3溶液中含有 Fe3+数目为 0.1NA
D. 将2molSO2和1molO2充分反应,转移的电子数目为4NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A.25℃时某溶液中水电离出的c(H+)=1.0×1012 mol·L1,其pH一定是12
B.某温度下,向氨水中通入CO2,随着CO2的通入,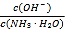 不断增大
不断增大
C.恒温恒容下,反应X(g)+3Y(g) ![]() 2Z(g),起始充入3 mol X和3 mol Y,当X的体积分数不变时,反应达到平衡
2Z(g),起始充入3 mol X和3 mol Y,当X的体积分数不变时,反应达到平衡
D.某温度下,向pH=6的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液的pH为2,该温度下加入等体积pH=10的NaOH溶液可使反应后的溶液恰好呈中性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒温下的密闭容器中,有可逆反应2NO(g)+O2(g)![]() 2NO2(g) ΔH<0,不能说明反应已达到平衡状态的是( )
2NO2(g) ΔH<0,不能说明反应已达到平衡状态的是( )
A.正反应生成NO2的速率和逆反应生成O2的速率相等
B.反应器中压强不随时间变化而变化
C.混合气体颜色深浅保持不变
D.混合气体平均相对分子质量保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各项反应对应的图象错误的是![]()

A.图甲:将氮气和氧气混合后在放电条件下反应
B.图乙:将稀盐酸逐滴加入一定量偏铝酸钠溶液中
C.图丙:将二氧化硫逐渐通入一定量氯水中
D.图丁:将铜粉逐渐加入一定量浓硝酸中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知H2的燃烧热为ΔH=-285.8 kJ·mol-1,CO的燃烧热为ΔH=-282.8 kJ·mol-1;现有H2和CO组成的混合气体5.6 L(标准状况),经充分燃烧后,放出总热量为71.15 kJ,并生成液态水。下列说法正确的是
A. CO燃烧的热化学方程式为2CO(g)+O2(g)===2CO2(g) ΔH=-282.8 kJ·mol-1
B. H2燃烧的热化学方程式为2H2(g)+O2(g)===2H2O(g) ΔH=-571.6 kJ·mol-1
C. 燃烧前混合气体中CO的体积分数为60%
D. 燃烧后的产物全部与足量的过氧化钠作用可产生0.125 mol O2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com