
| A、c(SO3)=0.4 mol?L-1 |
| B、c(SO2)=c(SO3)=0.15 mol?L-1 |
| C、c(SO2)=0.4mol?L-1 |
| D、c(SO2)+c(SO3)=0.4 mol?L-1 |
 2SO3(g),
2SO3(g),

科目:高中化学 来源: 题型:
| A、K+、H+、NO3-、SiO32- |
| B、H+、NH4+、Al3+、SO42- |
| C、Fe2+、H+、ClO-、SO42- |
| D、Al3+、Mg2+、SO42-、CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、已知某温度下纯水中的c(H+)=2×l0-7mol/L,据此无法求出水中c(OH-) | ||||||||||
| B、已知MgCO3的KSP=6.82×l0-6,则在含有固体MgCO3的MgCl2、Na2CO3溶液中,都有:c(Mg2+)=c(CO32-),且c(Mg2+)?c(CO32-)=6.82×10-6 mol2/L2 | ||||||||||
| C、常温下,Mg(OH)2能溶于氯化铵浓溶液的主要原因可能是NH4+结合OH-使沉淀溶解平衡发生移动 | ||||||||||
D、已知:
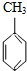 (g)+3H2(g)→ (g)+3H2(g)→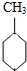 (g) 的焓变 (g) 的焓变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
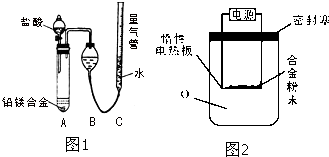 为测定某含铝95%一97%的铝镁合金(不含其它元素)中铝的质量分数,研究性学习小组的三位同学分别设计下列三种不同实验方案进行探究.填写下列空白.
为测定某含铝95%一97%的铝镁合金(不含其它元素)中铝的质量分数,研究性学习小组的三位同学分别设计下列三种不同实验方案进行探究.填写下列空白.| NaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:
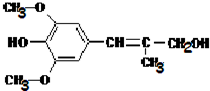 膳食纤维具有突出的保健功能,人体的“第七营养素”.木质素是一种非糖类膳食纤维,其学科王单体之一是芥子醇,结构简式如图所示.下列有关芥子醇的说法正确的是( )
膳食纤维具有突出的保健功能,人体的“第七营养素”.木质素是一种非糖类膳食纤维,其学科王单体之一是芥子醇,结构简式如图所示.下列有关芥子醇的说法正确的是( )| A、芥子醇的分子式是C12H16O4,属于芳香烃 |
| B、芥子醇分子中所有碳原子不 可能在同一平面 |
| C、芥子醇能与FeCl3溶液发生显色反应 |
| D、芥子醇能发生的反应类型有氧化、取代、加成、消去 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、混合物中不存在FeCl2 |
| B、反应④的离子反应式 AlO2-+H++H2O═Al(OH)3↓ |
| C、混合物一定含有Al、(NH4)2SO4和MgCl2三种物质,无法判断混合物中是否含有AlCl3 |
| D、白色沉淀5.80g 是Mg(OH)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com