
【题目】某温度时在2L容器中X、Y、Z三种气态物质的物质的量(n)随时间(t)变化的曲线如图所示,由图中数据分析:

(1)该反应的化学方程式为:______________________________。
(2)反应开始至2min,用Z表示的平均反应速率为:_______________。
(3)下列叙述能说明上述反应达到化学平衡状态的是_________(填序号)
A.混合气体的总物质的量不随时间的变化而变化
B.混合气体的压强不随时间的变化而变化
C.单位时间内每消耗3mol X,同时生成2 mol Z
D.混合气体的总质量不随时间的变化而变化
E.恒定容积,混合气体的密度不再发生改变
(4)在密闭容器里,通入a mol X(g)和b mol Y(g),发生反应X(g)+ Y(g)![]() 2Z(g),当改变下列条件时,反应速率会发生什么变化(选填“增大”、“减小”或“不变”)
2Z(g),当改变下列条件时,反应速率会发生什么变化(选填“增大”、“减小”或“不变”)
①升高温度,反应速率_____________;
②保持容器体积不变,充入不参加反应的惰性气体,反应速率____________。
【答案】 3X + Y![]() 2Z 0.05 mol·L-1·min-1 AB 增大 不变
2Z 0.05 mol·L-1·min-1 AB 增大 不变
【解析】(1)由图象可以看出X、Y的物质的量减小,Z的物质的量增多,则X、Y为反应物,Z为生成物,化学反应中各物质的物质的量变化量与化学计量数之比呈正比,则有Y:X:Z=(1.0mol-0.9mol):(1.0mol-0.7mol):0.2mol=1:3:2,则反应的化学方程式为3X+Y ![]() 2Z;(2)反应开始至2min,用Z表示的平均反应速率为v=
2Z;(2)反应开始至2min,用Z表示的平均反应速率为v= ![]() =
= ![]() =0.05 mol
=0.05 mol![]() L-1
L-1![]() min-1;(3)A、该反应是气体的物质的量减小的反应,当达到化学平衡时,混合气体的总物质的量不随时间的变化而变化,选项A正确;B、反应前后气体的计量数之和不相等,混合气体的压强不随时间的变化而变化,说明上述反应达到平衡状态,选项B正确;C、无论反应是否平衡,单位时间内每消耗3molX,同时生成2molZ,选项C错误;D、反应遵循质量守恒定律,无论是否平衡,混合气体的总质量不随时间的变化而变化,不能说明上述反应达到平衡状态,选项D错误;E、反应遵循质量守恒定律,无论是否平衡,混合气体的总质量不随时间的变化而变化,而容器体积不变,则密度也不随时间的变化而变化,不能说明上述反应达到平衡状态,选项E错误。答案选AB;(4)根据条件对反应速率的影响,①升高温度,反应速率增大;②保持容器体积不变,充入不参加反应的惰性气体,参与反应的气体物质的浓度不变,反应速率不变。
min-1;(3)A、该反应是气体的物质的量减小的反应,当达到化学平衡时,混合气体的总物质的量不随时间的变化而变化,选项A正确;B、反应前后气体的计量数之和不相等,混合气体的压强不随时间的变化而变化,说明上述反应达到平衡状态,选项B正确;C、无论反应是否平衡,单位时间内每消耗3molX,同时生成2molZ,选项C错误;D、反应遵循质量守恒定律,无论是否平衡,混合气体的总质量不随时间的变化而变化,不能说明上述反应达到平衡状态,选项D错误;E、反应遵循质量守恒定律,无论是否平衡,混合气体的总质量不随时间的变化而变化,而容器体积不变,则密度也不随时间的变化而变化,不能说明上述反应达到平衡状态,选项E错误。答案选AB;(4)根据条件对反应速率的影响,①升高温度,反应速率增大;②保持容器体积不变,充入不参加反应的惰性气体,参与反应的气体物质的浓度不变,反应速率不变。


 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案科目:高中化学 来源: 题型:
【题目】25℃时,取浓度均为0.1 mol·L-1的醋酸溶液和氨水溶液各20 mL,分别用0.1 mol·L-1NaOH溶液、0.1 mol·L-1盐酸进行中和滴定,滴定过程中pH随滴加溶液的体积变化关系如右图所示。下列说法正确的是( )

A. 曲线Ⅰ:滴加溶液到10 mL时:c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
B. 曲线Ⅰ:滴加溶液到20 mL时: c(Cl-)>c(NH4+)>c(OH-)>c(H+)
C. 曲线Ⅱ:滴加溶液到10 mL时:c(CH3COO-)-c(CH3COOH)=2[c(H+)-c(OH-)]
D. 曲线Ⅱ:滴加溶液在10 mL~20 mL之间存在:c(NH4+)=c(Cl-)>c(OH-)=c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在KCl、MgCl2、MgSO4形成的混合溶液中,c(K+)=0.1mol/L,c(Mg2+)=0.25mol/L,c(Cl﹣)=0.2mol/L,则c(SO42﹣)为( )
A.0.15mol/L
B.0.20mol/L
C.0.25mol/L
D.0.40mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(Ⅰ)在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)=CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
t/℃ | 700 | 800 | 830 | 1000 | 1200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K=____________________。
(2)某温度下,平衡浓度符合下式: c(CO2)·c(H2)= c(CO)·c(H2O),试判断此时的温度为______℃。
(Ⅱ)在一定温度下将2molA和2molB两种气体混合于2L密闭容器中,发生如下反应:3A(g)+B(g)== 2C(g)+2D(g),2分钟末反应达到平衡状态,生成了0.8mol D。B的平衡浓度为________, A的转化率为_______,用D表示的平均反应速率为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A.Si与SiO2在常温下都可与NaOH溶液反应
B.C与SiO2之间可以反应制备Si,同时得到CO
C.Si与SiO2都可以与氢氟酸反应
D.Si→SiO2→H2SiO3可以通过一步反应实现
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校学生小组为探究乙酸、碳酸和苯酚的酸性强弱进行下述实验。该校学生设计了下图的实验装置(夹持仪器已略去)。
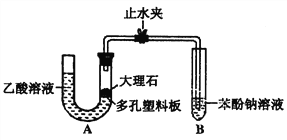
(1)某生检查装置A的气密性时,先关闭止水夹,从左管向U型管内加水,至左管液面高于右管液面,静置一段时间后,若U型管两侧液面差不发生变化,则气密性良好。你认为该生的操作正确与否?_______(填“正确”或“错误”),大理石与乙酸溶液反应的离子方程式为______________。
(2)装置A中反应产生的气体通入苯酚钠溶液中,实验现象为________________反应的离子方程式为_________________
(3)有学生认为(2)中的实验现象不足以证明碳酸的酸性比苯酚强,理由是_______________改进该装置的方法是____________________。
(4)在相同温度下,测定相同物质的量浓度 a.NaHCO3溶液 b.Na2CO3溶液 c. CH3COONa溶液 d. ![]() -ONa溶液的pH, 其pH由大到小排列的顺序为 _______________(填溶液编号)
-ONa溶液的pH, 其pH由大到小排列的顺序为 _______________(填溶液编号)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列应用不涉及氧化还原反应的是( )
A.Na2O2用作呼吸面具的供氧剂
B.工业上电解熔融状态的Al2O3制备Al
C.工业上利用合成氨实现人工固氮
D.实验室用NH4Cl和Ca(OH)2制备NH3
查看答案和解析>>
科目:高中化学 来源: 题型:
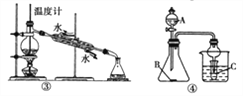
【题目】下列装置(必要的夹持装置及石棉网已省略)或操作能达到实验目的的是( )
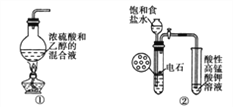
A. ①是实验室制乙烯
B. ②是实验室制乙炔并验证乙炔可以发生氧化反应
C. ③是实验室中分馏石油
D. ④中若A为稀硫酸,B为碳酸钠,C为硅酸钠溶液,验证硫酸、碳酸、硅酸酸性的强弱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中正确的是
A.NH3、CO、CO2都是极性分子
B.CH4、CCl4都是含有极性键的非极性分子
C.HF、HCl、HBr、Hl的稳定性依次增强
D.CS2、H2O、C2H2都是直线型分子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com