
某校研究性学习小组的同学进行了以下化学实验:将金属钙置于空气中燃烧,然后向所得固体产物中加入一定量蒸馏水,此过程中反应放出大量的热,并且放出有臭味的气体。
(1)甲同学提出:运用类比学习的思想,Ca与Mg是同一主族元素,化学性质具有一定的相似性。
请写出Ca在空气中燃烧发生反应的化学方程式: 。
(2)乙同学提出:Ca的性质比Na活泼,在空气中燃烧还应有CaO2生成,请写出燃烧后固体产物与水反应放出气体的化学方程式: 。
丙同学提出用实验的方法探究放出臭味气体的成份:
【查阅资料】1:CaO2遇水反应生成H2O2,H2O2可能会分解产生一定量的O3
2:碘量法是最常用的臭氧测定方法:其原理为强氧化剂臭氧(O3)与碘化钾(KI)水溶液反应生成游离碘(I2)。臭氧还原为氧气。反应式为:O3+2KI+H2O=O2+I2+2KOH 【提出假设】假设1:该臭味气体只有NH3;
假设2:该臭味气体只有 ;
假设3:该臭味气体含有 。
【设计方案进行实验探究】
(3)基于假设l,该小同学组设计如下实验方案,并进行实验。请在答题卡上按下表格式完成相关的实验操作步骤、预期现象及结论(仪器自选)。
【限选实验试剂】:红色石蕊试纸、蓝色石蕊试纸、pH试纸、淀粉一KI溶液、蒸馏水。设计实验方案证明你的假设,并按下表格式写出实验操作步骤、预期现象和结论。
|
实验操作 |
预期现象和结论 |
|
取少量反应后固体于试管中,
。 |
|
(1)Ca+O2=CaO2(1分)3Ca+N2=Ca3 N2 (1分)2Ca+CO2=2CaO+C (1分);
(2)2CaO2+2H2O=2Ca(OH)2 +O2 ↑(2分)Ca3N2+6H2O=3Ca(OH)2+2NH3↑ (2分);
(3)假设2:该臭味气体只有O 3(1分);
假设3:该臭味气体含有O 3和NH3 (1分);
|
实 验 操 作 |
预 期 现 象 与 结 论 |
|
取少量反应后固体于试管中,向试管中加入少量水,将湿润的红色石蕊试纸置于试管口; 另取少量反应后固体于试管中,向试管中加入少量水,将产生气体通入淀粉—KI溶液中; (2分)
|
若红色石蕊试纸显蓝色,且淀粉—KI溶液不变色 则假设1成立; 若 红色石蕊试纸不显蓝色,且淀粉—KI溶液变蓝色, 则假设2成立; 若红色石蕊试纸显蓝色,且淀粉—KI溶液变蓝色,则假设3成立;(3分) |
【解析】
试题分析:(1)Mg在空气中燃烧,可与O2、N2、CO2反应,所以Ca也能与O2、N2、CO2反应,进而写出化学方程式。
(2)CaO2类比Na2O2,写出CaO2与H2O的化学方程式:2CaO2+2H2O=2Ca(OH)2 +O2 ↑;Ca3N2与H2O发生水解反应,生成Ca(OH)2与NH3:Ca3N2+6H2O=3Ca(OH)2+2NH3↑。
(3)根据题目所给信息:CaO2遇水反应生成H2O2,H2O2可能会分解产生一定量的O3 ,可推出假设2为:该臭味气体只有O 3,假设3为:该臭味气体含有O 3和NH3;根据NH3溶于水显碱性,可用湿润的红色湿润试纸检验是否含NH3,利用O3具有强氧化性,可用淀粉-KI溶液检验是否含O3。
考点:本题考查化学方程式的书写、实验方案的设计与分析。


 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案科目:高中化学 来源: 题型:阅读理解


查看答案和解析>>
科目:高中化学 来源: 题型:
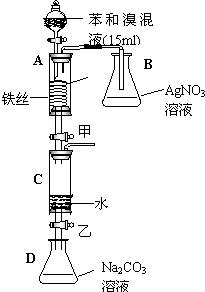 如图是某校研究性学习小组的同学设计的有关苯与溴在铁作催化剂时反应的实验装置图.请回答下列问题:
如图是某校研究性学习小组的同学设计的有关苯与溴在铁作催化剂时反应的实验装置图.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
(1)氨分子的电子式是____________,苯分子的空间构型为_____________。
(2)提出减少室内空气污染的一条措施:________________________________________。
(3)我国《室内空气质量标准》规定室内空气中甲醛含量不得超过0.08 mg·m-3,甲醛测定的方法主要有分光光度法、色谱法、电化学法和化学滴定法等。某校研究性学习小组的同学拟采用化学滴定法对教室内空气中甲醛的含量进行测定,如果你参与该研究课题,你采集甲醛样品的方法是________________________________________________________________。
(4)碘量法是化学滴定法之一。碘量法原理为在碱性介质(NaOH)中,碘转化为次碘酸钠和碘化钠,次碘酸钠将溶液中游离的甲醛氧化为甲酸钠;经适当酸化后,剩余的次碘酸钠与碘化钠又生成碘;以淀粉为指示剂,用硫代硫酸钠标准溶液滴定。上述过程中涉及的化学反应的离子方程式依次为I2+2OH-![]() IO-+I-+H2O、___________________________________、____________________________、I2+2
IO-+I-+H2O、___________________________________、____________________________、I2+2![]()
![]()
![]() +2I-。实验过程中需要测定的数据除总碘量外,还有_____________。
+2I-。实验过程中需要测定的数据除总碘量外,还有_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
居室是我们日常生活中最重要的场所。现代人在“煤烟型”、“光化学烟雾”污染后,正在进入以“室内空气污染”为标志的第三污染时期。造成室内环境污染的有毒物质主要有甲醛、苯、氨、氡四种。
请回答下列问题:
(1)氨分子的电子式是 ?? ,苯分子的空间构型为 ?? 。
(2)提出减少室内空气污染的一条措施: ?? 。
(3)我国《室内空气质量标准》规定室内空气中甲醛含量不得超过0.08mg??m-3,甲醛测定的方法主要有分光光度法、色谱法、电化学法、化学滴定法等。某校研究性学习小组的同学拟采用化学滴定法对教室内空气中甲醛的含量进行测定,如果你参与该研究课题,你采集甲醛样品的方法是 ?? 。
(4)碘量法是化学滴定法之一。碘量法原理为在碱性介质(NaOH)中,碘转化为次碘酸钠和碘化钠,次碘酸钠将溶液中游离的甲醛氧化为甲酸钠;经适当酸化后,剩余的次碘酸钠与碘化钠又生成碘;以淀粉为指示剂,用硫代硫酸钠标准溶液滴定。上述过程中涉及的化学反应的离子方程式依次为I2+2OH-====IO-+I-+H2O、
?? 、 ?? 、I2+2S2O32-====S4O62-+2I-。实验过程中需要测定的数据除总碘量外,还有 ?? 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com