
A.CaCl2溶液 B.石灰水?
C.饱和Na2CO3溶液 D.水玻璃?
科目:高中化学 来源: 题型:
 (1)把AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是
(1)把AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是查看答案和解析>>
科目:高中化学 来源: 题型:
下列选项中有关物质性质实验得到的结论正确的是( )
|
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列选项中,有关实验操作、现象和结论都正确的是( )
|
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源:2013-2014学年辽宁省抚顺市六校联合体高三上学期期中考试化学试卷(解析版) 题型:选择题
下列选项中,有关实验操作、现象和结论都正确的是( )
选项 实验操作 现象 结论
A 将过量的CO2通入CaCl2溶液中 无白色沉淀出现 生成的Ca(HCO3)2可溶于水
B 常温下将Al片插入浓硫酸中 无明显现象 Al片和浓硫酸不反应
C 向饱和Na2CO3溶液中通入足量CO2 溶液变浑浊 析出了NaHCO3
D 将SO2通入溴水中 溶液褪色 SO2具有漂白性
查看答案和解析>>
科目:高中化学 来源:2010-2011学年温州市高三八校联考化学试卷 题型:填空题
(10分)(1)已知:在常温下,浓度均为0.1mol·L-1的下列六种溶液的pH:
|
溶质 |
CH3COONa |
NaHCO3 |
Na2CO3 |
NaClO |
NaCN |
C6H5ONa |
|
pH |
8.8 |
9.7 |
11.6 |
10.3 |
11.1 |
11.3 |
依据复分解反应的规律,请你判断下列反应不能成立的是 (填编号)。
A.CH3COOH+ Na2CO3=NaHCO3+CH3COONa
B.CH3COOH+NaCN=CH3COONa+HCN
C.CO2+H2O+2NaClO=Na2CO3+2HClO
D.CO2+H2O+2C6H5ONa=Na2CO3+2C6H5OH
(2)根据前面描述的信息判断,浓度均为0.05mol·L-1的下列六种物质的溶液中,pH最小的是 (填编号);将各溶液分别稀释100倍,pH变化最小的是 (填编号)。
①C6H5OH ②CH3COOH ③HCN ④HClO ⑤H2SO4 ⑥HClO4
(3)根据前述信息,写出将过量的氯气通入到少量的碳酸钠溶液中反应的离子方程式: 。
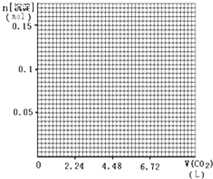
(4)标准状况下,向1L含NaOH、Ca(OH)2各0.1 mol的溶液中不断通入CO2至过量,请画出产生的沉淀的物质的量(mol)随CO2通入体积(L)的变化趋势图。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com