
| A、澄清透明的溶液中:Cu2+、Mg2+、SO42-、Cl- |
| B、c(Fe3+)=0.1mol?L-1的溶液中:Na+、NH4+、SCN-、SO42- |
| C、加入铝粉能产生氢气的溶液中:NH4+、Fe2+、SO42-、NO3- |
| D、0.1mol?L-1NaHCO3溶液中:K+、Ba2+、OH-、Cl- |


 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案科目:高中化学 来源: 题型:
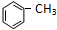 +Cl2
+Cl2| 光 |
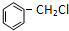 +HCl ②R-CH2-CH=CH2+Cl2
+HCl ②R-CH2-CH=CH2+Cl2| 500~600℃ |
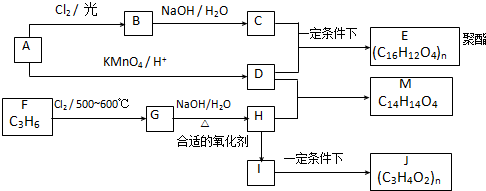
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| 3n |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
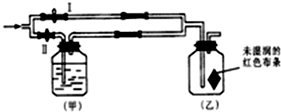
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、电解NaNO3溶液,在阴极上和阳极上析出产物的物质的量之比为2:1 |
| B、电解CuSO4溶液一段时间后,再加入一定质量Cu(OH)2,溶液能与原溶液完全一样 |
| C、电解硫酸钠溶液时,Na+向阳极移动 |
| D、电解KOH溶液,实质上是电解水,故溶液pH不变 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com