
【题目】将3L常温常压下的NO2依次通过盛有足量的下列物质,碳酸氢钠溶液、浓硫酸、过氧化钠固体,最后所得到的气体通入足量的水中,最后得到的气体及其体积(常温常压下)为( )
A.1L O2B.0.25L O2C.0.25L NOD.0.5L O2和1L NO2
 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案科目:高中化学 来源: 题型:
【题目】实验室用化合物A模拟工业上制备含氧酸D的过程如图所示,已知D为强酸,请回答下列问题。
![]()
(1)若A在常温下为固体,B是能使品红溶液褪色的有刺激性气味的无色气体。
①D的化学式是________;
②在工业生产中,B气体的大量排放被雨水吸收后形成了_____而污染了环境。
(2)若A在常温下为气体,C是红棕色的气体。
①A的化学式是_________;C的化学式是_______。
②D的浓溶液在常温下可与铜反应并生成C气体,反应的化学方程式是____,该反应______(填“属于”或“不属于”)氧化还原反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】观察图中 A、B、C 三个装置,回答下列问题:
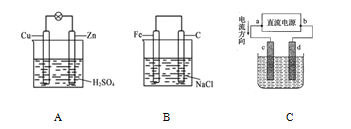
(1)把一块纯净的锌片插入装有稀硫酸的烧杯中,可观察到锌片上有气泡,再平行插入一铜片,可观察到铜片上_________(填“有”或“没有”)气泡产生。用导线把锌片和碳棒连接起来组成一个原电池(图A),正极的反应式为_______。
(2) 如果烧杯中最初装入的是 500 mL 2 mol·L-1 硫酸溶液,构成铜锌原电池,当收集到 11.2 L(标准状况下)H2 时,溶液体积变化忽略不计,则烧杯内溶液中硫酸的物质的量的浓度为_______mol/L。
(3) 如果电极材料分别是铁片和石墨并进行连接,插入氯化钠溶液中(图 B),放置数天后,铁片生锈。负极反应式为_______。
(4) 图 C 是电解 CuCl2 溶液的装置,其中 c、d 为石墨电极。
①正极为_______(填“a”或“b”)。
②阳极电极反应式为_______,检验该阳极产物的方法是将_______试纸靠近电极。
③电解一段时间后发现阴极增重 6.4 g,若该电解反应所需的电子全部由氢氧燃料电池提供,则至少需要消耗_______L 氢气(标准状况下)才能满足需要。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】磷化硼是一种超硬耐磨涂层材料。下图为其晶体结构中最小的重复结构单元,其中的每个原子均满足8电子稳定结构。下列有关说法正确的是( )
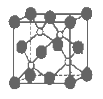
A.磷化硼晶体的化学式为BP,属于离子晶体
B.磷化硼晶体的熔点高,且熔融状态下能导电
C.磷化硼晶体中每个原子均形成4条共价键
D.磷化硼晶体结构微粒的空间堆积方式与氯化钠相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丙烯(C3H6)是重要的有机化工原料。下图为丙烷直接脱氢法中丙烷和丙烯的平衡体积分数与温度、压强的关系(图中的压强分别为104Pa和105 Pa)。
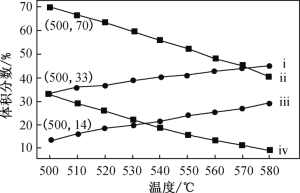
①104 Pa时,图中表示丙烯的曲线是____(填“ⅰ”、“ⅱ”、“ⅲ”或“ⅳ”)。
②104 Pa、500 ℃时,主反应用平衡分压代替平衡浓度表示的化学平衡常数Kp=_____(已知:气体分压=气体总压×体积分数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对有机物的描述错误的是( )
A.核糖核酸和脱氧核糖核酸都含有磷酯键
B.甲酰胺、丙氨酰甘氨酸分子中均含有酰胺基
C.人体内组成蛋白质的氨基酸均为α—氨基酸,其中一部分需从食物中摄取
D.1mol纤维素最多和3mol乙酸发生酯化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A.用分液漏斗可以分离乙酸乙酯和饱和碳酸钠溶液
B.用溴水除去甲烷中的乙烯气体
C.碳酸钠是焙制糕点所用的发酵粉主要成分之一
D.蒸馏是分离液态混合物一种常用方法,广泛应用于石油工业
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验及其分析叙述正确的是( )
A.向2.0mL浓度均为0.lmolL-l的KC1、KI混合溶液中滴加1~2滴0.0lmol/LAgNO3溶液,振荡,沉淀呈黄色,说明AgCl的Ksp比AgI的Ksp大
B.在稀硫酸中加入铜粉,铜粉不溶解;再加入适量的H2O2,铜粉仍不溶解
C.向AlC13溶液中滴加氨水,产生白色沉淀;再加入NaHSO4溶液,沉淀不消失
D.将CO2通入Ba(NO3)2溶液中至饱和,无沉淀产生;再通入SO2,也无沉淀产生
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锌在工业中有重要作用,也是人体必需的微量元素。回答下列问题:
(1)Zn原子核外电子排布式为________。
(2)黄铜是人类最早使用的合金之一,主要由Zn和Cu组成。第一电离能I1(Zn)________I1(Cu)(填“大于”或“小于”)。原因是______________________。
(3)ZnF2具有较高的熔点(872 ℃),其化学键类型是________;ZnF2不溶于有机溶剂而ZnCl2、ZnBr2、ZnI2能够溶于乙醇、乙醚等有机溶剂__。
(4)《中华本草》等中医典籍中,记载了炉甘石(ZnCO3)入药,可用于治疗皮肤炎症或表面创伤。ZnCO3中,阴离子空间构型为________,C原子的杂化形式为______。
(5)金属Zn晶体中的原子堆积方式如图所示,这种堆积方式称为________。六棱柱底边边长为acm,高为ccm,阿伏加德罗常数的值为NA,Zn的密度为________g·cm-3(列出计算式)。
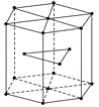
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com