
灰锡(以粉末状存在)和白锡是锡的两种同素异形体。已知:①Sn(s、白)+2HCl(aq)=SnCl2(aq)+H2(g) △H1 ②Sn(s、灰)+2HCl(aq)=SnCl2(aq)+H2(g) △H2 ③Sn(s、灰)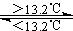 Sn(s、白)
Sn(s、白)
△H3=+2.1kJ/mol 下列说法正确的是( )
A.△H1>△H2
B.锡在常温下以灰锡状态存在
C.灰锡转化为白锡的反应是放热反应
D.锡制器皿长期处于低于13.2℃的环境中,会自行毁坏
科目:高中化学 来源:2014-2015学年广东省高二上学期第一次月考文科化学卷(解析版) 题型:选择题
化石燃料仍是目前能源的主体,但已经面临危机,开发新能源是解决能源问题的关键。下列能量转换过程,不涉及化学变化的是
A.利用氢氧燃料电池提供电能 B.利用太阳能分解水制备氢气
C.利用水流驱动涡轮机发电 D.利用植物秸秆为原料生产乙醇燃料
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东省第一学期高一第一次月考化学试卷(解析版) 题型:选择题
进行化学实验必须注意安全,下列说法正确的是( )
A.不慎将酸液溅到眼中,应立即用水冲洗,边洗边眨眼睛
B.不慎将浓碱液沾到皮肤上,要立即用大量的稀硫酸冲洗
C.酒精灯着火时可用水扑灭
D.稀释浓硫酸时,可往装有一定体积浓硫酸的量筒中,慢慢加入水
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东省广州市高一上学期期中化学试卷(解析版) 题型:选择题
关于物质的类别,下列说法正确的是
A.食盐水、糖水和冰水都是饮料,属于混合物
B.某物质只含有一种元素,则该物质一定是单质
C.烧碱属于碱,纯碱属于盐
D.CuSO4·5H2O是一种混合物
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东东莞市高二上学期第一次月考化学试卷(解析版) 题型:选择题
25℃,101 k Pa时,强酸与强碱的稀溶液发生中和反应生成1mol水时所放出的热量约为57.3 kJ/mol;辛烷的燃烧热为5518 kJ/mol。下列热化学方程式书写正确的是
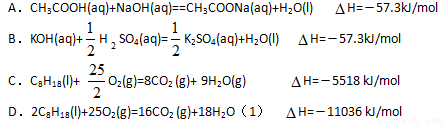
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东东莞市高二上学期第一次月考化学试卷(解析版) 题型:选择题
未来新能源的特点是资源丰富,在使用时对环境无污染或污染很小,且可以再生。下列属于未来新能源标准的是
①天然气 ②煤 ③核能 ④石油 ⑤太阳能 ⑥生物质能 ⑦风能 ⑧氢能
A.①②③④ B.⑤⑥⑦⑧ C.③⑤⑥⑦⑧ D.③④⑤⑥⑦⑧
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山西省高一上学期第一次考试化学试卷(解析版) 题型:选择题
混合气体由N2和CH4组成,测得混合气体在标准状况下的密度为0.821g/L,则混合气体中N2和CH4的体积之比为( )
A.5:1 B.1:4 C.4:1 D.1:5
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山西省高二10月月考化学试卷(解析版) 题型:填空题
二甲醚是一种重要的清洁燃料,也可替代氟利昂作制冷剂等,对臭氧层无破坏作用。工业上可利用煤的气化产物(水煤气)合成二甲醚。
(1)利用水煤气合成二甲醚的三步反应如下:
①2H2(g) + CO(g)  CH3OH(g);ΔH = -90.8 kJ·mol-1
CH3OH(g);ΔH = -90.8 kJ·mol-1
②2CH3OH(g)  CH3OCH3(g) + H2O(g);ΔH= -23.5 kJ·mol-1
CH3OCH3(g) + H2O(g);ΔH= -23.5 kJ·mol-1
③CO(g) + H2O(g)  CO2(g) + H2(g);ΔH= -41.3 kJ·mol-1
CO2(g) + H2(g);ΔH= -41.3 kJ·mol-1
总反应:3H2(g) + 3CO(g)  CH3OCH3(g) + CO2(g)的ΔH= ___________;
CH3OCH3(g) + CO2(g)的ΔH= ___________;
(2)已知反应②2CH3OH(g)  CH3OCH3(g) + H2O(g)某温度下的平衡常数为400 。此温度下,在密闭容器中加入CH3OH ,反应到某时刻测得各组分的浓度如下:
CH3OCH3(g) + H2O(g)某温度下的平衡常数为400 。此温度下,在密闭容器中加入CH3OH ,反应到某时刻测得各组分的浓度如下:
物质 | CH3OH | CH3OCH3 | H2O |
浓度/(mol·L-1) | 0.44 | 0.6 | 0.6 |
①比较此时正、逆反应速率的大小:v正 ______ v逆 (填“>”、“<”或“=”);
②若加入CH3OH后,经10 min反应达到平衡,此时c(CH3OH) = _______________,该时间内反应速率v(CH3OH) = __________________;
(3)在溶液中,反应A+2B C分别在三种不同实验条件下进行,它们的起始浓度均为c(A)=0.100mol/L、c(B)=0.200mol/L及c(C)=0mol/L。反应物A的浓度随时间的变化如下图所示。
C分别在三种不同实验条件下进行,它们的起始浓度均为c(A)=0.100mol/L、c(B)=0.200mol/L及c(C)=0mol/L。反应物A的浓度随时间的变化如下图所示。
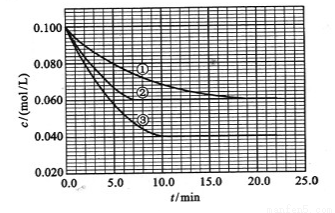
请回答下列问题:
与①比较,②和③分别仅改变一种反应条件。所改变的条件和判断的理由是:
②________________________________________________________________________;
③________________________________________________________________________;
该反应的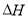 _________0,判断其理由是______________________________________________;
_________0,判断其理由是______________________________________________;
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山西大学附中第一学期高二化学试卷(解析版) 题型:选择题
我国首创的海洋电池以铝板为负极,铂网为正极,海水为电解质溶液,空气中的氧气与铝反应产生电流。电池总反应为:4Al+3O2+6H2O=4Al(OH)3,下列说法不正确的是( )
A.正极反应为:O2+2H2O+4e-=4OH-
B.电池工作时,电流由铝电极沿导线流向铂电极
C.以网状的铂为正极,可增大与氧气的接触面积
D.该电池通常只需更换铝板就可继续使用
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com