
二甲醚是一种重要的清洁燃料,也可替代氟利昂作制冷剂等,对臭氧层无破坏作用。工业上可利用煤的气化产物(水煤气)合成二甲醚。
(1)利用水煤气合成二甲醚的三步反应如下:
①2H2(g) + CO(g)  CH3OH(g);ΔH = -90.8 kJ·mol-1
CH3OH(g);ΔH = -90.8 kJ·mol-1
②2CH3OH(g)  CH3OCH3(g) + H2O(g);ΔH= -23.5 kJ·mol-1
CH3OCH3(g) + H2O(g);ΔH= -23.5 kJ·mol-1
③CO(g) + H2O(g)  CO2(g) + H2(g);ΔH= -41.3 kJ·mol-1
CO2(g) + H2(g);ΔH= -41.3 kJ·mol-1
总反应:3H2(g) + 3CO(g)  CH3OCH3(g) + CO2(g)的ΔH= ___________;
CH3OCH3(g) + CO2(g)的ΔH= ___________;
(2)已知反应②2CH3OH(g)  CH3OCH3(g) + H2O(g)某温度下的平衡常数为400 。此温度下,在密闭容器中加入CH3OH ,反应到某时刻测得各组分的浓度如下:
CH3OCH3(g) + H2O(g)某温度下的平衡常数为400 。此温度下,在密闭容器中加入CH3OH ,反应到某时刻测得各组分的浓度如下:
物质 | CH3OH | CH3OCH3 | H2O |
浓度/(mol·L-1) | 0.44 | 0.6 | 0.6 |
①比较此时正、逆反应速率的大小:v正 ______ v逆 (填“>”、“<”或“=”);
②若加入CH3OH后,经10 min反应达到平衡,此时c(CH3OH) = _______________,该时间内反应速率v(CH3OH) = __________________;
(3)在溶液中,反应A+2B C分别在三种不同实验条件下进行,它们的起始浓度均为c(A)=0.100mol/L、c(B)=0.200mol/L及c(C)=0mol/L。反应物A的浓度随时间的变化如下图所示。
C分别在三种不同实验条件下进行,它们的起始浓度均为c(A)=0.100mol/L、c(B)=0.200mol/L及c(C)=0mol/L。反应物A的浓度随时间的变化如下图所示。
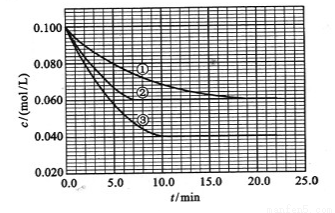
请回答下列问题:
与①比较,②和③分别仅改变一种反应条件。所改变的条件和判断的理由是:
②________________________________________________________________________;
③________________________________________________________________________;
该反应的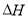 _________0,判断其理由是______________________________________________;
_________0,判断其理由是______________________________________________;
(1)-246.4kJ·mol-1
(2)①> ②0.04 mol·L-1 0.16 mol·L-1·min-1
(3)②加催化剂;达到平衡的时间缩短,平衡时A的浓度未变
③温度升高;达到平衡的时间缩短,平衡时A的浓度减小
﹥;升高温度向正方向移动,故该反应是吸热反应
【解析】
试题分析:(1)①2H2(g)+CO(g) CH3OH(g)△H=-90.8KJ/mol-1
CH3OH(g)△H=-90.8KJ/mol-1
②2CH3OH(g) ?CH3OCH3(g)+H2O(g)△H=-23.5KJ/mol-1
?CH3OCH3(g)+H2O(g)△H=-23.5KJ/mol-1
③CO(g)+H2O(g) CO2(g)+H2(g)△H=-41.3KJ/mol-1
CO2(g)+H2(g)△H=-41.3KJ/mol-1
由盖斯定律②+③+①×2得到
3H2(g)+3CO(g) CH3OCH3(g)+CO2(g)的△H=-246.4 Kj/mol-1,
CH3OCH3(g)+CO2(g)的△H=-246.4 Kj/mol-1,
(2)①表中数据分析计算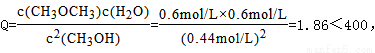 说明反应正向进行,v正>v逆
说明反应正向进行,v正>v逆
②甲醇起始量浓度为0.44+1.2=1.64mol/L.设转化的甲醇浓度为x
2CH3OH(g) CH3OCH3(g)+H2O(g)
CH3OCH3(g)+H2O(g)
起始量( mol/L) 1.64 0 0
变化量(mol/L) x 0.5x 0.5x
平衡量(mol/L) 1.64-x 0.5x 0.5x
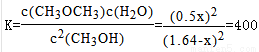
计算得到x=1.6mol/L
若经10 min后反应达到平衡,此时c(CH3OH)=0.04 mol/L
0~10min内甲醇平衡浓度=0.04mol/L,平均反应速率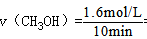 = 0.16 mol·L-1·min-1
= 0.16 mol·L-1·min-1
(3)①因催化剂能加快化学反应速度率,缩短达到平衡的时间,化学平衡不移动,所以②为使用催化剂;因升高温度,化学反应速度率加快,化学平衡移动,平衡时A的浓度减小;因③温度升高,化学平衡向吸热的方向移动,平衡时A的浓度减小,说明正反应方向吸热,△H>0
考点:考查热化学方程式和盖斯定律的分析应用,化学平衡的有关知识和化学计算。


 巧学巧练系列答案
巧学巧练系列答案科目:高中化学 来源:2014-2015学年广东省第一学期高一第一次月考化学试卷(解析版) 题型:实验题
(18分)下图所示是分离混合物时常用的仪器,回答下列问题:
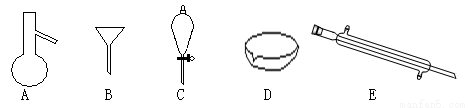
(1)写出仪器C、E的名称 、
(2)分离以下混合物应该主要选用上述什么仪器?(填字母符号)
①NaCl固体和泥沙: ②花生油和水:
(3)若向C装置中加入碘水和足量CCl4,充分振荡后静置,观察到现象是:C内液体分两层,上层液体呈 色,下层液体 色。
(4)碘单质和溴单质有相类似的性质,都可以用有机溶剂萃取水溶液中的单质,若利用C仪器提取溴水中的溴单质,下列有机溶剂中不能选用的是:
A.汽油 B.CCl4 C.酒精 D.醋酸
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东东莞市高二上学期第一次月考化学试卷(解析版) 题型:选择题
灰锡(以粉末状存在)和白锡是锡的两种同素异形体。已知:①Sn(s、白)+2HCl(aq)=SnCl2(aq)+H2(g) △H1 ②Sn(s、灰)+2HCl(aq)=SnCl2(aq)+H2(g) △H2 ③Sn(s、灰)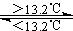 Sn(s、白)
Sn(s、白)
△H3=+2.1kJ/mol 下列说法正确的是( )
A.△H1>△H2
B.锡在常温下以灰锡状态存在
C.灰锡转化为白锡的反应是放热反应
D.锡制器皿长期处于低于13.2℃的环境中,会自行毁坏
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山西省高一上学期第一次考试化学试卷(解析版) 题型:选择题
过滤后的食盐水仍含有可溶性的CaCl2、MgCl2、Na2SO4等杂质,通过如下几个实验步骤,可制得纯净的食盐水:①加入稍过量的Na2CO3溶液;②加入稍过量的NaOH溶液;③加入稍过量的BaCl2 溶液;④滴入稀盐酸至无气泡产生;⑤过滤 正确的操作顺序( )
A.①②③⑤④ B.③②①⑤④
C.②③①④⑤ D.③⑤②①④
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山西省高一上学期第一次考试化学试卷(解析版) 题型:选择题
将下列各组物质按单质、氧化物、酸、碱、盐分类顺序排列,其中正确的是 ( )
A.银、干冰、硫酸、烧碱、食盐
B.碘酒、冰、盐酸、烧碱、食盐
C.氢气、二氧化硫、硝酸、纯碱、硝酸钾
D.铜、氧化铜、醋酸、石灰水、氯化铜
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山西省高二10月月考化学试卷(解析版) 题型:选择题
一定温度下,在恒容密闭容器中发生如下反应:2A(g)+B(g) 3C(g),若反应开始时充入2 mol A和2 mol B,达平衡后A的体积分数为a %。其他条件不变时,若按下列四种配比作为起始物质,平衡后A的体积分数大于a %的是
3C(g),若反应开始时充入2 mol A和2 mol B,达平衡后A的体积分数为a %。其他条件不变时,若按下列四种配比作为起始物质,平衡后A的体积分数大于a %的是
A.2 mol C
B.1 mol A、1 mol B和1 mol He(不参加反应)
C.1 mol B和1 mol C
D.2 mol A、3 mol B和3 mol C
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山西省高二10月月考化学试卷(解析版) 题型:选择题
Cl2通入水中发生如下反应:Cl2+H2O  HCl+HClO,欲增大所得溶液中HClO的浓度,应采取的措施为
HCl+HClO,欲增大所得溶液中HClO的浓度,应采取的措施为
A.加CaCO3固体 B.加NaOH固体
C.加水 D.通入NH3气
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山西大学附中第一学期高二化学试卷(解析版) 题型:填空题
下列共有十二种化学符号:
①O2 ②614C ③238U ④1123Na ⑤O3 ⑥714N ⑦1224Mg ⑧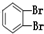
⑨235U ⑩ (11)
(11)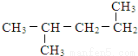 (12)
(12)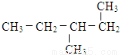
其中:
(1)表示核素的符号共有___种.
(2)互为同位素的是___(填序号,以下相同)
(3)质量数相等,但不能互称同位素的是__
(4)中子数相等,但质子数不相等的是___.
(5)互为同素异形体的是___.
(6)互为同分异构体的是___.
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省潍坊三县市高一上学期联考化学试卷(解析版) 题型:填空题
(12分)某工业残渣主要成分为Fe2O3。(含有少量FeO、Cu、Mg等杂质)某课外兴趣小组利用该残渣制取Fe2O3粉末的实验流程如下:(说明流程中向黄色溶液中加入MgO的目的是调节溶液的酸碱性,使Fe3+ 生成沉淀而Mg2+不沉淀。)
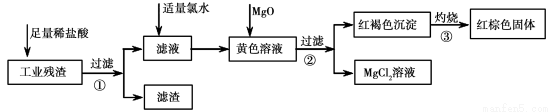
请回答下列问题:
(1)加入足量稀盐酸后,发生化学反应的类型有_____________(填写代号)。
A.置换反应 B.化合反应 C.分解反应 D.复分解反应 E.氧化还原反应
(2)加入适量氯水的作用是 ;
(3)写出灼烧红褐色沉淀时发生反应的化学方程式 。实验室灼烧红褐色沉淀可选用的装置是__________(填序号)。
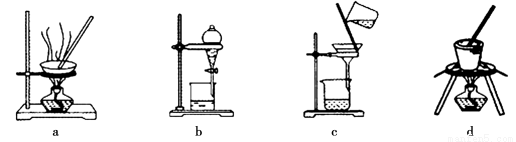
(4)若向黄色溶液中加入过滤①后的滤渣发生反应的离子方程式为 。
(5)检验黄色溶液中Fe3+是否完全沉淀的方法是:取过滤②后的少量滤液于试管中, 。(请补充完整实验操作、现象、结论)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com