
����Ŀ���״�����Ҫ�Ļ���ԭ�ϣ��ֿ���Ϊȼ�ϡ���ҵ�����úϳ���(��Ҫ�ɷ�ΪCO��CO2��H2) �ڴ����������ºϳɼ״�������������Ӧ����:
��CO(g)+2H2(g) ![]() CH3OH(g) ��H1
CH3OH(g) ��H1
��CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g) ��H=-58kJ/mol
CH3OH(g)+H2O(g) ��H=-58kJ/mol
��CO2(g)+H2(g) ![]() CO(g)+H2O(g) ��H=+41kJ/mol
CO(g)+H2O(g) ��H=+41kJ/mol
�ش���������:
(1)��֪��Ӧ���е���صĻ�ѧ��������������:
��ѧ�� | H-H | C-O | C=O | H-O | C-H |
E/(kJ/mol) | a | b | c | d | x |
��x=______�����ú�������ĸ�Ĵ���ʽ��ʾ��
(2)����lmolCO2��2molH2�����ݻ�Ϊ2L�ĺ����ܱ������У������ֲ�ͬ�¶��·�����Ӧ�ڡ����CH3OH�����ʵ�����ʱ��ı仯��ͼ��ʾ��
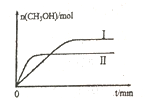
�����ߢ��Ӧ��ƽ�ⳣ����С��ϵΪK��_____K��(�>��=����<��)
��һ���¶���,���жϸ÷�Ӧ�ﵽ��ѧƽ��״̬����______��
a.������ѹǿ����
b.�״���ˮ����������ȱ��ֲ���
c.v��(H2)=3v��(CH3OH)
d.2��C=O���ѵ�ͬʱ��3��H-H�γ�
����5min��Ӧ�ﵽƽ��״̬��H2��ת����Ϊ90%������CO2��ʾ��ƽ����Ӧ����Ϊ_____�����¶��µ�ƽ�ⳣ��Ϊ_____���������ݻ����䣬���д�ʩ�����Ӽ״����ʵ���____��
a.�����¶� b.ʹ�ú��ʵĴ��� c.����He d.��ԭ�����ٳ���CO2��H2
���𰸡� 1/3(2a+c-b-d)+33 > a��c��d 0.06mol/(L��min) 450 d
��������(1)���ݸ�˹�����У����̢�=���̢�-���̢ۣ�������H1=-58kJ/mol-��+41kJ/mol��=-99 kJ/mol
��������H1=��Ӧ����ܼ���-��������ܼ���=��c+2a��-(3x+b+d)������x= 1/3(2a+c-b-d)+33��
(2) �١����ߢ��ȴﵽƽ�⣬���Ԣ��Ӧ���¶ȱȢ���¶ȸߣ����ڷ�ӦCO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g) ��H=-58KJ/mol��˵������ƽ�������ƶ���ƽ�ⳣ������K��>K����
CH3OH(g)+H2O(g) ��H=-58KJ/mol��˵������ƽ�������ƶ���ƽ�ⳣ������K��>K����
�ڡ��÷�Ӧ��������Ӹ���ǰ�����仯��������ѹǿ���䣬˵������ķ��Ӹ������ٱ仯������˵����Ӧ�Ѵ�ƽ�⣬a��ȷ�������ʼͶ�����ʼԭ��ֻ�з�Ӧ���ֻ���������Ұ���ѧ������Ͷ�ϣ���Ӧ�м״���ˮ�����������ʼ����һ����ֵ����˵����Ӧ�Ƿ�ƽ�⣬b����v��(H2)=3v��(CH3OH)������Ӧ�Ѵ�ƽ������v��(H2)= v��(H2)������v��(H2)=3v��(CH3OH)��˵����Ӧ�Ѵ�ƽ�⣬c��ȷ��2��C=O���ѵ�ͬʱ��3��H-H�γɣ��������ʷ����෴���ҷ��ϻ�ѧ������֮�ȣ�����˵���Ѵ�ƽ�⣬d��ȷ�������жϸ÷�Ӧ�ﵽ��ѧƽ��״̬����a��c��d��
����5minʱv(H2)=2mol��0.9��2L��5min=0.18 mol/(L��min)������v(CO2)= v(H2)/3=0.06 mol/(L��min)����������ģʽ��������õ�ƽ��ʱCO2��H2��CH3OH��H2O��Ũ�ȷֱ�Ϊ��0.2mol/L��0.1mol/L��0.3mol/L��0.3mol/L������K=(0.3��0.3)/(0.2��0.13)=450�����£�ƽ�������ƶ����״����ʽ��ͣ�������Ӱ��ƽ����ƶ����Լ״��IJ�����Ӱ�죻���������³���He����Ӧ��ϵ�и����ʵ�Ũ�Ȳ��䣬ƽ�ⲻ�ƶ����Լ״��IJ�����Ӱ�죻��ԭ�����ٳ���CO2��H2���൱���ڵ�Чƽ��Ļ�������ѹ��ƽ�������ƶ����״��IJ�������ѡ��d��


 ��������ѧ����ϵ�д�
��������ѧ����ϵ�д� ��Ԫ������ĩ��ϵ�д�
��Ԫ������ĩ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���й�������ϸ�����Ԫ�ص�������������ǣ� ��
A. �ڲ�ͬ�������ϸ���ڣ�������ǵĻ�ѧԪ�����������ͬ
B. ���ϸ���������Ԫ����C
C. ��ͬһ����IJ�ͬ��ϸ���ڣ����ֻ�ѧԪ�صĺ�����ͬ
D. ���������ϸ���Ļ�ѧԪ�أ�������Ȼ���ж����ҵ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������к�Cu2+�ķ�ˮ����MnS��s�������������䷴Ӧԭ��Ϊ�� Cu2+��aq��+MnS��s��CuS��s��+Mn2+��aq��
�����йظ÷�Ӧ����������ȷ���ǣ�������
A.�÷�Ӧ�ﵽƽ��ʱ��c��Cu2+��=c��Mn2+��
B.CuS���ܽ�ȱ�MnS���ܽ��С
C.��ƽ����ϵ�м�������Cu��NO3��2��s����c��Mn2+�����
D.�÷�Ӧƽ�ⳣ������ʽ��K= ![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Ϊ2L�ĺ����ܱ������з�����ӦxA (g) +yB (g) ![]() zC (g),ͼI��ʾ200��ʱ������A��B��C���ʵ�����ʱ��ı仯��ͼ���ʾ��ͬ�¶���ƽ��ʱC�������������ʼn (A): n (B)�ı仯��ϵ�����н�����ȷ����
zC (g),ͼI��ʾ200��ʱ������A��B��C���ʵ�����ʱ��ı仯��ͼ���ʾ��ͬ�¶���ƽ��ʱC�������������ʼn (A): n (B)�ı仯��ϵ�����н�����ȷ����
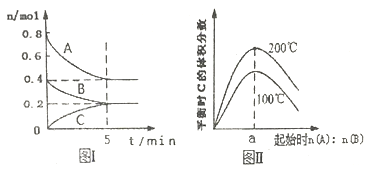
A. 200��ʱ����Ӧ�ӿ�ʼ��ƽ���ƽ������v(B)��0.04 molL��1min��1
B. ͼ����֪��ӦxA(g)+yB(g)![]() zC(g)�Ħ�H<0����a��2
zC(g)�Ħ�H<0����a��2
C. ����ͼ����ʾ��ƽ��״̬�£�������ϵ�г���He�����´ﵽƽ��ǰv����v��
D. 200��ʱ���������г���2 mol A ��1 mol B���ﵽƽ��ʱ��A ���������С��50%
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������Ի������Һ�о�����NO3-����������ԭ��Ӧ��ת����ϵ����:
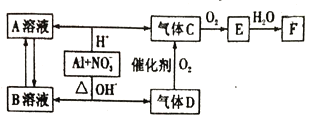
��ش���������:
(1) ����D ��F ��Ӧ�������Σ����εĻ�ѧʽΪ_________��
(2) C��E��������л���ɴ�����Ⱦ���ڴ��������£�D���Խ�C��Eת��Ϊ������̬���ʣ��õ��ʵĽṹʽ��___________��
(3) ����Dת��Ϊ����C �Ļ�ѧ����ʽ__________��
(4) Al ��NO3-�����������·�Ӧ��Al�뱻��ԭ��NO3-�����ʵ���֮����_____________��
(5) Al ��NO3-�ڼ��������·�Ӧ�����ӷ���ʽΪ_____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼʾװ�ý�������ʵ�飬�ܴﵽʵ��Ŀ�ĵ���
��Һa | ����b | ��Һc | ʵ��Ŀ�ģ���֤ |
| |
A | Ũ���� | NaHCO3 | Na2SiO3 | �ǽ����ԣ�N��C��Si | |
B | Ũ���� | KMnO4 | Na2S | �����ԣ�KMnO4��Cl2��S | |
C | Ũ���� | CaCO3 | NaAlO2 | ���ԣ�HCl��H2CO3��Al(OH)3 | |
D | Ũ��ˮ | CaO | ��̪��Һ | NH3��H2O������ |
A. A B. B C. C D. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ����2 molL-1��Na2SO4��ҺΪ�������Һ�������ӵ�ص��ܷ�Ӧ���£�PΪ+5�ۣ���NaTi2(PO4)3+Zn+Na2SO4![]() Na3Ti2(PO4)3+ZnSO4�����й�˵����ȷ���ǣ� ��
Na3Ti2(PO4)3+ZnSO4�����й�˵����ȷ���ǣ� ��
A. �ŵ�ʱ��NaTi2(PO4)3����������Ӧ
B. �ŵ�ʱ��Na����п��һ���ƶ�
C. ���ʱ��������ӦʽΪ[Ti2(PO4)3]+-2e-=[Ti2(PO4)3]3+
D. ���ʱ��ÿת��0. 2 mol���ӣ���������6.5 g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��CuCl���л��ϳɵ���Ҫ���������������ϡ������ȹ�ҵ����ҵ���ɷ�ͭ�ϣ���Fe��Al���仯���SiO2���ʣ�������CuCl�Ĺ����������£�
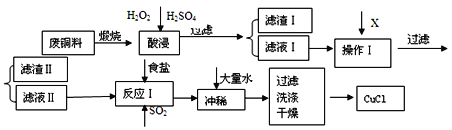
���� | ��ʼ���� | ������ȫ |
Fe(OH)3 | 2.7 | 3.7 |
Cu(OH)2 | 5.6 | 6.7 |
Al(OH)3 | 3.8 | 4.7 |
��֪��CuCl����NaCl��Ũ��Һ������CuCl2-��CuCl2-����Һ��ˮϡ�ͺ������CuCl������
��1�����յ���ҪĿ������______________________________________��
��2��������Ϊ������Һ��pHֵ����ΧΪ___________�����������X������_________________________ ��
A.CuO B.Cu(OH)2 C .NaOH ��Һ D.CaCO3
��3������I����Ҫ�ɷ���________�����������Ҫ�ɷ���_________��
��4������Һ���м���ʳ�β�ͨ��SO2������CuCl����д����Ӧ�����ӷ���ʽ________________________________________________________________________________________ ��
��5���ڷ�Ӧ���У����Ȳ�ʹ��ŨNaC1��Һ����ҪĿ����_____________________________________________________________________________________ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ϸ����Ԫ��C��������ȷ���ǣ� ��
A. �����Ԫ�ء� B. ����Ԫ�� C. ��Ԫ�� D. ����Ԫ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com