
| A、标准状况下11.2L的水中含有0.5个NA水分子 |
| B、22.4L N2的所含的电子数是14NA个 |
| C、氧化还原反应中,若消耗7.1g Cl2,必转移0.2NA个电子 |
| D、常温常压下,1mol N2和NO的混合气体中含2NA个原子 |
| V |
| Vm |
| V |
| Vm |
| 22.4L |
| 22.4L/mol |
| V |
| Vm |


 步步高达标卷系列答案
步步高达标卷系列答案科目:高中化学 来源: 题型:
| A、生成40.0 L N2(标准状况下) |
| B、有0.250 mol KNO3被氧化 |
| C、转移电子的物质的量为1.5 mol |
| D、被氧化的N原子的物质的量为3.75 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向FeCl3溶液中滴加氨水:Fe3++3OH-═Fe(OH)3↓ |
| B、向Na[Al(OH)4]溶液中通入少量CO2:2[Al(OH)4]-+CO2═2Al(OH)3↓+CO32-+H2O |
| C、向Ca(ClO)2溶液中通入过量的CO2:Ca2++2ClO-+CO2+H2O═CaCO3↓+2HClO |
| D、向NH4HCO3溶液中加入足量NaOH溶液:NH4++OH-═NH3↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温常压下,0.1mol C8H18所含有的共价键数目为2.0 NA |
| B、标准状况下,2.24L乙酸乙酯中所含氧原子数为0.2NA |
| C、0.1mol乙醇与氧化铜完全反应时转移电子数为0.1NA |
| D、现有乙烯、丙烯、丁烯的混合气体共14 g,其原子数为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、乙烧杯中d的电极反应为 2Cl--2e-=Cl2↑ | ||||
| B、a、c两极产生气体的物质的量相等 | ||||
C、乙烧杯中发生的反应为2NaCl+2H2O
| ||||
| D、甲、乙两烧杯中溶液的pH均保持不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、KClO3和SO3溶于水后能导电,故KClO3和SO3为电解质 |
| B、25℃时,用醋酸溶液滴定等浓度NaOH溶液至pH=7,V(醋酸)<V(NaOH) |
| C、AgCl沉淀易转化成AgI沉淀且Ksp(AgX)=c(Ag+)?c(X-),故Ksp(AgI)<Ksp (AgCl) |
| D、BaSO4的水溶液不导电,故BaSO4是弱电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Ba2+、Na+、NO3-、SO42- |
| B、Mg2+、Al3+、Cl-、SO42- |
| C、K+、Fe3+、Cl-、SCN- |
| D、Na+、Fe2+、Cl2、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、36g镁在足量的氮气中完全燃烧共转移的电子数为3NA |
| B、标准状况下,44.8 L NO与22.4 LO2混合后气体中分子总数为2NA |
| C、室温下,21.0g乙烯和丁烯的混合气体中含有的碳氢共价键数目为3NA |
| D、1 molNa2O和Na2O2混合物中含有的阴、阳离子总数是3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
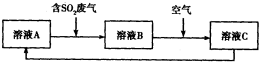
| ClO2 |
| 反应Ⅰ |
| Na2SO3水溶液 |
| 反应Ⅱ |
c(S
| ||
c(HS
|
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com