
【题目】以下图像与相对应的反应情况分析正确的是
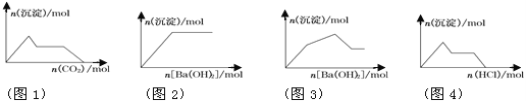
A. 图1:向含KOH和Ca(OH)2的混合溶液中缓慢通入CO2
B. 图2:向NaHSO4溶液中逐滴加入Ba(OH)2溶液
C. 图3:向KAl(SO4)2溶液中逐滴加入Ba(OH)2溶液
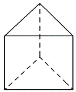
D. 图4:向Na[Al(OH)4]溶液中逐滴加入盐酸
【答案】B
【解析】
A、含 KOH和 Ca(OH)2的混合溶液中缓慢通入CO2,先生成碳酸钙沉淀,后有碳酸钾生成,再生成碳酸氢钾,最后沉淀溶解,生成碳酸氢钙,故图像错误;
B、 NaHSO4溶液中逐滴加入Ba(OH)2溶液先生成硫酸钡沉淀,后沉淀不再溶解变化,正确;
C、 KAl(SO4)2溶液中逐滴加入Ba(OH)2溶液,当物质的量之比是2:3时,生成硫酸钡和氢氧化铝沉淀,再加入1molBa(OH)2时,氢氧化铝沉淀溶解2mol,硫酸钡生成1mol,图像中沉淀应该减少,当滴入的物质的量之比为1:2后,再加入氢氧化钡后,沉淀不再变化,故图像错误;
D、 NaAlO2溶液中逐滴加入盐酸,先生成氢氧化铝沉淀,沉淀达最大后,再溶解转变为氯化铝溶液,故图像错误。
答案选B。


科目:高中化学 来源: 题型:
【题目】以高硫铝土矿(主要成分为Al2O3、Fe2O3、SiO2,少量FeS2)为原料,生产Fe3O4的部分工艺流程如下:

下列说法错误的是
A. 用NaOH溶液吸收焙烧过程产生的SO2有利于保护环境和资源再利用
B. 从高硫铝土矿中可制得Al、Fe的化合物
C. 向“过滤”得到的滤液中通入过量CO2,铝元素存在的形式由AlO转化为Al3+
D. FeS2与Fe2O3混合后在无氧条件下焙烧的目的是生成Fe3O4和SO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原子核磁共振谱(NMR)是研究有机化合物结构的有力手段之一。在所研究化合物的分子中,每一结构中的等性氢原子,在NMR谱中都给出相应的峰(信号)。谱中峰的强度与结构中的H原子数成正比。例如,乙醛的结构式为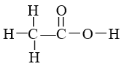 ,其NMR谱中有两个信号,其强度之比为3∶1。
,其NMR谱中有两个信号,其强度之比为3∶1。
(1)分子式为C3H6O2的二元混合物,如果在NMR谱中观察氢原子给出的峰有两种情况:第一种情况峰的强度比为3∶3;第二种情况峰的强度比为3∶2∶1。由此可推断该混合物的组成可能是(写结构简式)_____________________。
(2)在测得的CH3CH2CH2CI化合物的.NMR谱上可观察到三种峰,而测定化合物CH3CH=CHCl时,却得到氢原子给出的6个信号峰。根据原子空间排列方式不同,试写出CH3CH=CHCl分子的空间异构____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在150 ℃的条件下,总质量为3 g的一氧化碳和氢气的混合气体,在足量的氧气中燃烧后,再通过足量的过氧化钠,过氧化钠增加的质量为( )
A.1.5 gB.3 gC.6 gD.无法计算
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人们对苯的认识有一个不断深化的过程。已知分子式为 C6H6的结构有多种,其中的两种为:
Ⅰ.![]() Ⅱ.
Ⅱ.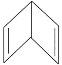
(1)这两种结构的化学性质区别表现在:Ⅰ能________(填字母,下同),而Ⅱ能________。
A.被酸性KMnO4溶液氧化
B.与溴水发生加成反应
C.与氢气发生加成反应
(2)1 mol C6H6与H2发生完全加成反应,Ⅰ需________molH2,而Ⅱ需________mol H2。
(3)今发现C6H6还可能有另一种如下图所示的立体结构,该结构的二氯代物有_________种。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镁及其化合物一般无毒(或低毒)、无污染,镁电池放电时电压高且平稳,因此镁电池越来越成为人们研制绿色电池的焦点。其中一种镁电池的反应:为:xMg+Mo3S4![]() MgxMo3S4;在镁原电池放电时,下列说法错误的是( )
MgxMo3S4;在镁原电池放电时,下列说法错误的是( )
A. Mg2+向正极迁移 B. 正极反应为:Mo3S4+2xe-═Mo3S42x-
C. Mo3S4发生氧化反应 D. 负极反应为:xMg-2xe-═xMg2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.A、B、C、D和E均为中学化学常见的纯净物,其中B为自然界中含量最多的液体,它们之间有如图反应关系:

(1)若A的溶液能使淀粉溶液变蓝,C为非金属氧化物,能使品红溶液褪色,该反应的离子方程式为____________________________________。
(2)若A为短周期的金属单质,D为气态单质,C溶液呈强酸性或强碱性时,该反应都能进行。写出C溶液呈强碱性时反应的离子方程式:_____________________________。
(3)若A、C均为化合物,E为白色沉淀(不含金属元素),C为引起温室效应的主要气体,则该反应的离子方程式为__________________________________。
Ⅱ. FeCl3可用于污水处理,具有效果好、价格便宜等优点。工业上可将铁屑溶于盐酸中先生成FeCl2,再通入Cl2氧化来制备FeCl3溶液。
(4)将标准状况下a L氯化氢气体溶于1000g水中得到盐酸,若该盐酸的密度为b g·mL-1,则该盐酸的物质的量浓度是____________________。
(5)向100 mL的FeBr2溶液中通入标准状况下Cl2 3.36 L,反应后的溶液中Cl-和Br-的物质的量浓度相等,则原FeBr2溶液的物质的量浓度为____________。
(6)用100 mL 2 mol·L-1的FeCl3溶液净水时,生成具有净水作用的微粒数_____0.2NA (填“大于”“等于”或“小于”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一密闭容器中,反应aA(g)![]() bB(g)达到平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,B的浓度是原来的60%,则( )
bB(g)达到平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,B的浓度是原来的60%,则( )
A. 平衡向正反应方向移动了B. 物质A 的转化率减小了
C. 气体总物质的量减小了D. a>b
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com