
【题目】需加入适当氧化剂才能实现的反应是( )
A.MnO2→Mn2+B.SO2→SO32-
C.PCl3→PCl5D.CaCO3→CO2
科目:高中化学 来源: 题型:
【题目】下列有关氧化还原反应的叙述错误的是
A.复分解反应一定不是氧化还原反应
B.氧化还原反应一定有元素化合价的升降
C.氧化还原反应中氧化剂和还原剂可能是同一种物质
D.氧化剂失电子,被还原
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用硫酸厂烧渣(含铁的氧化物和少量FeS及SiO2)制碱式硫酸铁的流程如下:

(1)SO2与过量NaOH溶液反应的离子方程式为_____________。
(2)滤渣的主要成分为_________(填化学式)。
(3)反应1中加双氧水的目的是将Fe2+氧化为Fe3+,该反应的离子方程式为________。
(4)碱式硫酸铁的化学式为Fex(OH)y(SO4)z·nH2O,为确定其组成进行如下实验:
①称取1.6920g样品溶于足量的稀盐酸中;
②加足量的BaCl2溶液,过滤、洗涤、干燥、称重,得固体质量为2.3300g;
③向步骤②的滤液中加过量的NaOH溶液,过滤、洗涤、灼烧、称重,得固体质量为0.6400g。
根据以上实验数据确定该碱式硫酸铁的化学式_________(写出计算过程)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,H2(g)+CO2(g)H2O(g)+CO(g)的平衡常数K= ![]() .该温度下在甲、乙、丙三个恒容密闭容器中,投入H2(g)和CO2(g),其起始浓度如表所示.下列判断不正确的是( )
.该温度下在甲、乙、丙三个恒容密闭容器中,投入H2(g)和CO2(g),其起始浓度如表所示.下列判断不正确的是( )
起始浓度 | 甲 | 乙 | 丙 |
c(H2)/mol/L | 0.010 | 0.020 | 0.020 |
c(CO2)/mol/L | 0.010 | 0.010 | 0.020 |
A.平衡时,乙中CO2的转化率大于60%
B.平衡时,甲中和丙中H2的转化率均是60%
C.平衡时,丙中c(CO2)是甲中的2倍,是0.012mol/L
D.反应开始时,丙中的反应速率最快,甲中的反应速率最慢
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中,一定量混合气体发生下列反应:aA(g)+bB(g)cC(g)+dD(g),达到平衡后,测得C气体的浓度为0.5mol/L.当在恒温下,将密闭容器的体积缩小为 ![]() ,再达平衡时,测得C气体的浓度为0.9mol/L.则下列叙述正确的是( )
,再达平衡时,测得C气体的浓度为0.9mol/L.则下列叙述正确的是( )
A.反应速率降低
B.平衡向右移动
C.B的转化率提高
D.a+b<c+d
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列描述中,不正确的是( )
A. 14N与15N具有相同的质子数 B. 18O和17O具有相同的电子数
C. 18O与19F具有相同的中子数 D. 12C与13C具有相同的质量数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】两种金属混合粉末15g,与足量的盐酸反应时生成11.2L H2(标况下),符合上述情况的金属混合物是( )
A. Mg、Fe B. Zn、Ag C. Fe、Zn D. Mg、Al
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据所学知识完成题目:
(1)(Ⅰ)已知在448℃时,反应H2(g)+I2(g)2HI(g)的平衡常数 K1为49,则该温度下反应2HI(g)H2(g)+I2(g)的平衡常数K2为![]() ;反应
;反应 ![]() H2(g)+
H2(g)+ ![]() I2(g)HI(g)的平衡常数K3为 .
I2(g)HI(g)的平衡常数K3为 .
(2)(Ⅱ)在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表所示:
t/℃ | 700 | 800 | 830 | 1 000 | 1 200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
①该反应的化学平衡常数表达式为K= .
②该反应为反应(填“吸热”或“放热”).
③能判断该反应达到化学平衡状态的依据是 .
A.容器中压强不变 B.混合气体中c(CO)不变 C.v(H2)正=v(H2O)逆 D.c(CO2)=c(CO)
④在800℃时,发生上述反应,某一时刻测得容器内各物质的浓度分别为c(CO2)为2mol/L,c(H2)为1.5mol/L,c(CO)为1mol/L,c(H2O)为3mol/L,则下一时刻,反应向(填“正向”或“逆向”)进行.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是( ) 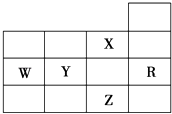
A.W元素的第一电离能小于Y元素的第一电离能
B.Y、Z的阴离子电子层结构都与R原子的相同
C.p能级未成对电子最多的是Z元素
D.X元素是电负性最大的元素
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com