
【题目】航天飞机用铝粉与高氯酸铵(NH4ClO4)的混合物为固体燃料,反应方程式表示为2NH4ClO4![]() N2↑+Cl2↑+2O2↑+4H2O。下列对该反应的叙述中错误的是( )
N2↑+Cl2↑+2O2↑+4H2O。下列对该反应的叙述中错误的是( )
A.瞬间产生大量高温气体推动航天飞机飞行
B.从能量变化的角度,主要是化学能转变为热能和动能
C.反应的焓变小于零
D.在方程式后增加ΔH及其数值即为热化学方程式
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】为验证氧化性:Cl2>Fe3+>SO2,某小组用图所示装置进行实验(夹持仪器和甲中加热装置已略,气密性已检验)。
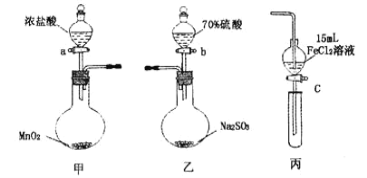
实验步骤:
(1)在甲装置中,打开活塞a,加热,待装置中充满黄绿色气体时,与丙装置连接。
(2)当丙装置中FeC12溶液变黄时,停止加热。
(3)打开活塞c,使约2mL的溶液滴入试管中,检验溶液中的离子。
(4)在乙装置中,打开活塞b,待空气排尽后,将乙中产生的气体通入上述丙装置变黄后的溶液中,一段时间后停止。
(5)更新丙中试管,打开活塞c,使约2mL的溶液滴入试管中,检验溶液中的离子。
回答下列问题:
(1)乙中发生反应的化学方程式为_________。
(2)实验中,证明氧化性Fe3+>SO2的离子方程式为_________。
(3)将甲装置与丙装置连接的目的是_______。
(4)有I、II、III三组同学分别完成了上述实验,实验结果如图:

上述实验结果一定能够证明氧化性:Cl2>Fe3+>SO2的是______(用“I”、“II”、“III”代号回答)。
(5)若要用以上甲和丙装置证明氧化性为:Cl2> Fe3+> I2的结论,则步骤为:
①往丙的漏斗中加入两种试剂____、___和一种溶剂_____。
②将甲装置中产生的Cl2慢慢通入丙中,观察丙的漏斗中溶液颜色变化。
③如果观察到丙中溶液________则结论正确。
④停止通入Cl2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列四幅图示所表示的信息与对应的叙述相符的是( )

A. 图1表示H2与O2发生反应过程中的能量变化,则H2的燃烧热为241.8kJ·mol—1
B. 图2表示某吸热反应分别在有、无催化剂的情况下反应过程中的能量变化
C. 图3表示一定条件下H2和Cl2生成HCl的反应热与途径无关,则 △H1=△H2+△H3
D. 图4表示压强对可逆反应2A(g)+2B(g)![]() 3C(g)+D(s)的影响,乙的压强大
3C(g)+D(s)的影响,乙的压强大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】依巴斯汀是一种抗过敏药物,羟基依巴斯汀(H)是该药物在人体中的初级代谢产物,其人工合成路线如下:
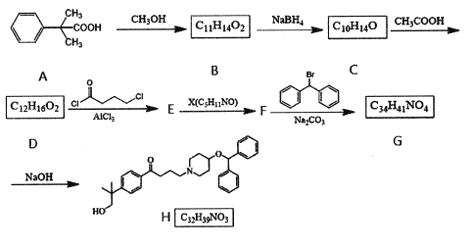
已知: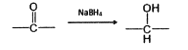
R-Cl![]() R-NH-R’
R-NH-R’
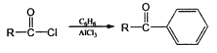
(1)F的结构简式为____________________
(2)下列说法不正确的是__________
A.l mol B可以和4 mol H2加成
B.X具有碱性
C.C可以发生取代、消去、加成等反应
D.1 mol E可以和3 mol NaOH反应
(3)写出由C生成D的反应方程式__________________________________________
(4)在F生成G过程中,Na2CO3的作用:___________________________________
(5)以苯和![]() 为原料合成
为原料合成![]() ,请设计出合成路径。___________
,请设计出合成路径。___________
(6)有机物Y的分子组成比X(C5H11NO)多1个“CH2”,写出三个满足下列条件的Y的同分异构体:________________________
①Y的分子中含有六元环状结构
②核磁共振氢谱表明Y分子中含有4种不同化学环境的氢
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为纪念迪米特里·门捷列夫发明的元素周期表诞生150周年,联合国大会宣布2019年是“国际化学元素周期表年”.元素周期表是科学界最重要的成就之一,表是元素周期表的一部分,其中每个数字序号代表一种短周期元素.
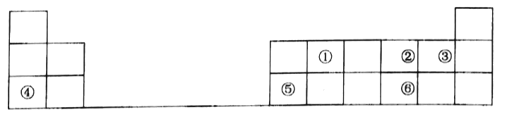
请按要求回答下列问题:
(1)将①、②和③三种元素相比较,非金属性最强的是(填元素符号)______;用原子结构解释原因,理由是:_________
(2)元素②与⑥的氢化物的稳定性顺序为________(填化学式);
(3)元素②与元素④能形成原子个数比为1:1的化合物Y,Y在常温下为固态,焰色反应为黄色,Y与①的最高价氧化物反应的化学方程式为__________
(4)元素④和元素⑤的最高价氧化物对应的水化物在溶液中相互反应的离子方程式是___
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】密闭容器中发生可逆反应:H2(g)+I2(g)![]() 2HI(g)达到平衡状态时的标志是
2HI(g)达到平衡状态时的标志是
A.容器的压强恒定不变
B.混合气体的颜色不再改变
C.H2、I2、HI的浓度相等
D.I2在混合气体中的体积分数与H2在混合气体中的体积分数相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A--F六种有机化合物是重要的有机合成原料,结构简式见下表,请根据要求回答下列问题:
化合物 | A | B | C |
结构简式 |
|
|
|
化合物 | D | E | F |
结构简式 |
|
|
|
![]() 写出符合下列条件的A的同分异构体的结构简式: ______ 。
写出符合下列条件的A的同分异构体的结构简式: ______ 。
A.核磁共振氢谱有4组峰
B.能发生水解反应
C.在加热条件下能够与新制的氢氧化铜悬浊液生成砖红色沉淀
![]() 化合物B是制取抗心律失常药物--氟卡尼的中间体,下列有关描述不正确的是______
化合物B是制取抗心律失常药物--氟卡尼的中间体,下列有关描述不正确的是______ ![]() 填字母
填字母![]() 。
。
A.能与氯化铁溶液显色![]() 分子中含有羧基、羟基等官能团
分子中含有羧基、羟基等官能团
C.能与溴水反应![]() 能与碳酸钠溶液反应产生二氧化碳
能与碳酸钠溶液反应产生二氧化碳
![]() 化合物B在一定条件下,可以与NaOH溶液发生反应,则1mol化合物B最多需要NaOH的物质的量为 ______ 。
化合物B在一定条件下,可以与NaOH溶液发生反应,则1mol化合物B最多需要NaOH的物质的量为 ______ 。
![]() 化合物C与D在一定条件下发生如下转化得到高分子化合物Z,部分产物已略去。
化合物C与D在一定条件下发生如下转化得到高分子化合物Z,部分产物已略去。
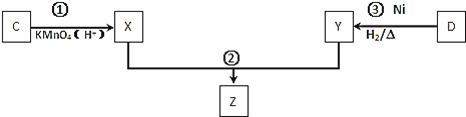
反应![]() 中D与
中D与![]() 按物质的量1:1反应生成Y,则反应
按物质的量1:1反应生成Y,则反应![]() 的化学方程式为 ______ 。
的化学方程式为 ______ 。
![]() 化合物D与银氨溶液反应的化学方程式
化合物D与银氨溶液反应的化学方程式![]() 有机物用结构简式表示
有机物用结构简式表示![]() : ______ 。
: ______ 。
![]() 化合物F是合成克矽平的原料之一,
化合物F是合成克矽平的原料之一,![]() 克矽平是一种治疗矽肺病的药物
克矽平是一种治疗矽肺病的药物![]() ,其合成路线如下
,其合成路线如下![]() 反应均在一定条件下进行
反应均在一定条件下进行![]() :
:

![]() 反应
反应![]() 是原子利用率
是原子利用率![]() 的反应,则该反应的化学方程式为 ______ ;
的反应,则该反应的化学方程式为 ______ ;
![]() 上述转化关系中没有涉及的反应类型是 ______
上述转化关系中没有涉及的反应类型是 ______ ![]() 填代号
填代号![]() 。
。
![]() 加成反应
加成反应![]() 消去反应
消去反应![]() 还原反应
还原反应![]() 氧化反应
氧化反应![]() 加聚反应
加聚反应![]() 取代反应。
取代反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制备Cl2通常采用如图所示装置:

(1)A装置中发生反应的化学方程式是________;每生成0.5 mol Cl2,被氧化的物质的物质的量是_____mol。
(2)仪器a的名称是_________;
(3)B装置中所盛的试剂是________________;
(4)实验时,通常采用密度为1.19 g/cm3、浓度为36.5%的浓盐酸。该浓盐酸的物质的量浓度为________;
(5)将如图装置代替装置D和E,可进行“氯气与金属钠反应”的实验,以下叙述正确的是________。
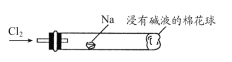
A. 反应生成的大量白烟是氯化钠晶体
B. 玻璃管尾部塞一团浸有碱液的棉球是用于吸收过量的氯气,以免其污染空气
C. 玻璃管中,钠燃烧时会产生苍白色火焰
D. 若在棉球外沿滴一滴淀粉碘化钾溶液,可据其颜色变化判断氯气是否被碱液完全吸收
(6)E装置中发生反应的化学方程式是________________;为验证E装置反应后的溶液中存在Cl-,正确的操作是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计一个燃料电池(如图所示),目的是探究氯碱工业原理和粗铜的精炼原理。

根据要求回答相关问题:
(1)甲装置中,通入氢气的电极为________(填“正极”或“负极”),该极电极反应式为________;若将KOH溶液换成硫酸溶液,则正极电极反应式为__________________________。
(2)关于乙装置,下列说法正确的是________(填序号);
①溶液中Na+向C极移动
②从C极处逸出的气体能使湿润的KI淀粉试纸变蓝
③反应一段时间后通入适量HCl可恢复到电解前电解质的浓度
④若标准状况下Fe极产生2.24L气体,则溶液中转移0.2mol电子
该装置中发生的总反应的离子方程式为__________________________。
(3)乙装置中,X为阳离子交换膜,反应一段时间后交换膜左侧溶液中pH____(填“增大”、“减小”或“不变”);若用饱和MgCl2溶液代替饱和氯化钠溶液,则该装置中发生的总反应______(填“改变”或“不变”)。
(4)如果粗铜中含有锌、银等杂质,丙装置中反应一段时间,硫酸铜溶液浓度将________(填“增大”“减小”或“不变”),精铜电极上的电极反应式为_______________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com