
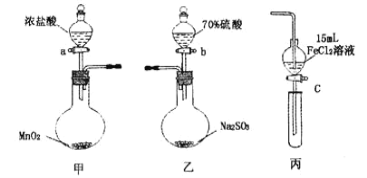
【题目】为验证氧化性:Cl2>Fe3+>SO2,某小组用图所示装置进行实验(夹持仪器和甲中加热装置已略,气密性已检验)。
实验步骤:
(1)在甲装置中,打开活塞a,加热,待装置中充满黄绿色气体时,与丙装置连接。
(2)当丙装置中FeC12溶液变黄时,停止加热。
(3)打开活塞c,使约2mL的溶液滴入试管中,检验溶液中的离子。
(4)在乙装置中,打开活塞b,待空气排尽后,将乙中产生的气体通入上述丙装置变黄后的溶液中,一段时间后停止。
(5)更新丙中试管,打开活塞c,使约2mL的溶液滴入试管中,检验溶液中的离子。
回答下列问题:
(1)乙中发生反应的化学方程式为_________。
(2)实验中,证明氧化性Fe3+>SO2的离子方程式为_________。
(3)将甲装置与丙装置连接的目的是_______。
(4)有I、II、III三组同学分别完成了上述实验,实验结果如图:

上述实验结果一定能够证明氧化性:Cl2>Fe3+>SO2的是______(用“I”、“II”、“III”代号回答)。
(5)若要用以上甲和丙装置证明氧化性为:Cl2> Fe3+> I2的结论,则步骤为:
①往丙的漏斗中加入两种试剂____、___和一种溶剂_____。
②将甲装置中产生的Cl2慢慢通入丙中,观察丙的漏斗中溶液颜色变化。
③如果观察到丙中溶液________则结论正确。
④停止通入Cl2
【答案】Na2SO3+H2SO4 (70%)=Na2SO4+SO2↑+H2O 2Fe3++SO2+2H2O=2Fe2++SO![]() +4H+ 为了证明Cl2的氧化性强于Fe3+ I、III FeI2 KSCN CCl4 下层(CCl4层)先由无色变为紫红色,后看到上层溶液由浅绿色变为红色
+4H+ 为了证明Cl2的氧化性强于Fe3+ I、III FeI2 KSCN CCl4 下层(CCl4层)先由无色变为紫红色,后看到上层溶液由浅绿色变为红色
【解析】
在甲装置中MnO2与浓盐酸混合加热制取Cl2,将制取得到的Cl2通入丙装置中,发生反应2FeCl2+Cl2=2FeCl3,证明物质的氧化性:Cl2>Fe3+,溶液由浅绿色变为黄色,打开活塞c,使约2 mL的溶液滴入试管中,向其中滴加KSCN溶液,若溶液变为红色,证明反应产生了Fe3+;打开乙装置的b活塞,使硫酸进入烧瓶,发生反应产生SO2气体,将SO2气体通入丙装置的分液漏斗中,发生反应:2Fe3++SO2+2H2O=2Fe2++SO![]() +4H+,通过检验SO
+4H+,通过检验SO![]() 证明物质的氧化性Fe3+>SO2。
证明物质的氧化性Fe3+>SO2。
(1)在装置乙中使硫酸进入烧瓶,与发生Na2SO3反应产生SO2气体,反应的化学方程式为Na2SO3+H2SO4 (70%)=Na2SO4+SO2↑+H2O;
(2)实验中,向FeCl3溶液中通入SO2气体,发生反应:2Fe3++SO2+2H2O=2Fe2++SO![]() +4H+,溶液由黄色逐渐变为浅绿色,就证明氧化性Fe3+>SO2;
+4H+,溶液由黄色逐渐变为浅绿色,就证明氧化性Fe3+>SO2;
(3) Cl2通入丙装置中,发生反应2FeCl2+Cl2=2FeCl3,溶液由浅绿色变为黄色,证明物质的氧化性:Cl2>Fe3+,所以将甲装置与丙装置连接的目的是:为了证明Cl2的氧化性强于Fe3+;
(4)若物质的氧化性:Cl2>Fe3+>SO2,根据物质的氧化性:氧化剂>氧化产物,可知会发生反应:2Fe2++Cl2=2Cl-+2Fe3+;2Fe3++SO2+2H2O=2Fe2++SO![]() +4H+;所以只要步骤3中证明含有Fe3+,就证明氧化性Cl2>Fe3+;若步骤3中同时还存在Fe2+,说明在溶液中不存在Cl2,但是在步骤5能检验出含有SO
+4H+;所以只要步骤3中证明含有Fe3+,就证明氧化性Cl2>Fe3+;若步骤3中同时还存在Fe2+,说明在溶液中不存在Cl2,但是在步骤5能检验出含有SO![]() ,说明只能是Fe3+氧化SO2所致。因此可以证明物质的氧化性:Cl2>Fe3+>SO2,Ⅰ正确;
,说明只能是Fe3+氧化SO2所致。因此可以证明物质的氧化性:Cl2>Fe3+>SO2,Ⅰ正确;
若步骤3溶液中有Fe3+而无Fe2+,则可能是Cl2与Fe2+恰好反应,也可能是Cl2过量。因此步骤5的溶液中含有的SO![]() 也可能是Cl2氧化所致,因此不能证明该结论的正确性,Ⅱ错误;
也可能是Cl2氧化所致,因此不能证明该结论的正确性,Ⅱ错误;
若步骤3溶液中有Fe3+而无Fe2+,则可能是Cl2与Fe2+恰好反应,也可能是Cl2过量,而步骤5的溶液中含有的Fe2+,则发生反应2Fe3++ SO2+2H2O=2Fe2++SO![]() +4H+;证明氧化性Fe3+>SO2,Ⅲ正确;
+4H+;证明氧化性Fe3+>SO2,Ⅲ正确;
故合理选项是I、III;
(5)将甲装置产生的Cl2通入到丙装置中的FeI2溶液中,氯气先氧化I-产生I2单质,然后氧化Fe2+生成Fe3+,用CCl4萃取碘单质,用
①根据以上分析可知,往丙的漏斗中加入两种试剂FeI2、KSCN和一种溶剂CCl4;
②将甲装置中产生的Cl2慢慢通入丙中,观察丙的漏斗中溶液颜色变化;
③如果观察到下层(CCl4层)先由无色变为紫红色,后看到上层溶液由浅绿色变为红色,就证明结论:Cl2>Fe3+> I2。


科目:高中化学 来源: 题型:
【题目】下列各实验操作中错误的是![]()
![]() 实验室制乙烯时,温度计水银球应插入混合液中
实验室制乙烯时,温度计水银球应插入混合液中
![]() 配制氢氧化铜悬浊液时,向硫酸铜溶液中逐滴滴加氢氧化钠溶液,直到沉淀完全为止
配制氢氧化铜悬浊液时,向硫酸铜溶液中逐滴滴加氢氧化钠溶液,直到沉淀完全为止
![]() 配制银氨溶液时,向硝酸银溶液中逐滴滴加氨水,边滴边振荡,直到生成的沉淀溶解为止
配制银氨溶液时,向硝酸银溶液中逐滴滴加氨水,边滴边振荡,直到生成的沉淀溶解为止
![]() 用醋酸、碳酸氢钠、苯酚钠和必须的仪器可以检验苯酚、醋酸、碳酸的酸性强弱
用醋酸、碳酸氢钠、苯酚钠和必须的仪器可以检验苯酚、醋酸、碳酸的酸性强弱
![]() 做过银镜反应的试管用浓硝酸清洗
做过银镜反应的试管用浓硝酸清洗
![]() 卤代烃与氢氧化钠溶液共热后,再滴入硝酸银溶液,可检验卤原子的种类
卤代烃与氢氧化钠溶液共热后,再滴入硝酸银溶液,可检验卤原子的种类
![]() 若苯酚不慎沾到皮肤上,应立即用酒精洗涤
若苯酚不慎沾到皮肤上,应立即用酒精洗涤
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是一种“纳米药物分子运输车”,该技术可提高肿瘤的治疗效果。回答下列问题:
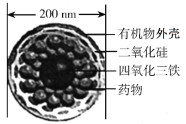
(1)“纳米药物分子车”分散于水中所得的分散系__(填“属于”或“不属于”)胶体。
(2) “纳米药物分子车”的外壳属于有机物。酒精、蔗糖、冰醋酸这三种有机物中,属于电解质的是__。
(3)从元素组成的角度分析,SiO2和Fe3O4可归为同一类物质,其类别属于化合物中的__。
(4)纳米级的Fe3O4是一种非常重要的磁性材料。
①Fe3O4溶于稀盐酸生成FeCl3、__和H2O。
②铁在氧气中燃烧生成Fe3O4,反应中每生成1molFe3O4转移__mol电子。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】华法林(Warfarin)又名杀鼠灵,为心血管疾病的临床药物。其合成路线(部分反应条件略去)如下所示:
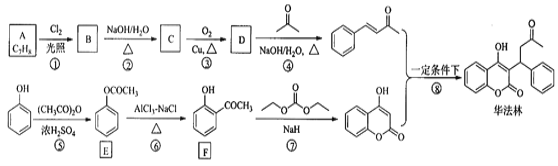
回答下列问题:
(1)A的名称为________,E中官能团名称为________。
(2)B的结构简式为________。
(3)由C生成D的化学方程式为___________
(4)⑤的反应类型为_________,⑧的反应类型为________。
(5)F的同分异构体中,同时符合下列条件的同分异构体共有___________种。
a.能与FeCl3溶液发生显色反应 b.含有-CHO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子反应方程式书写正确的是
A.往稀盐酸中逐滴加入Na2CO3溶液,开始时:H++CO32-=HCO3-
B.草酸(H2C2O4)溶液中加入酸性KMnO4溶液:2MnO4-+5C2O42-+16H+=2Mn2++10CO2↑+8H2O
C.往少量澄清石灰水中加入Ca(HCO3)2溶液:Ca2++OH-+HCO3-=CaCO3↓+H2O
D.用HI溶液溶解Fe2O3固体:Fe2O3+6H+=2Fe3++3H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某二元酸(化学式用H2X表示)在水中的电离方程式是:H2X=H++HX- HX-![]() H++X2-,常温下,向10 mL 0.1000 mol/L的H2X溶液中逐滴加入0.1000 mol/L的NaOH溶液,pH随NaOH溶液体积的变化如图所示。下列叙述中正确的是
H++X2-,常温下,向10 mL 0.1000 mol/L的H2X溶液中逐滴加入0.1000 mol/L的NaOH溶液,pH随NaOH溶液体积的变化如图所示。下列叙述中正确的是
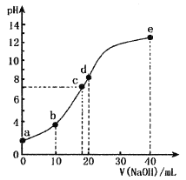
A.a点pH>1
B.b点溶液中:c(Na+)>c(HX-)>c(X2-)>c(H2X)>c(H+)>c(OH-)
C.d点溶液中:c(Na+)=2c(X2-)+2c(HX-)
D.水的电离程度:c>a>e
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生成水的能量关系如图所示:下列说法不正确的是
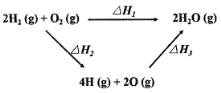
A.△H2>0
B.若2H2(g)+O2(g)=2H2O(l) △H4,则△H4<△H1
C.一定条件下,气态原子生成1 mol H-O放出a kJ热量,则该条件下△H3=-4akJ/mol
D.△H1+△H2+△H3=0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硬脂酸甘油酯在碱性条件下水解的装置如图所示。
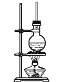
进行皂化反应实验的操作步骤如下:
(1)在圆底烧瓶中加入7~8g硬脂酸甘油酯,然后加入2~3gNaOH、5mL水和10mL酒精,其中加入酒精的作用是___。
(2)加热反应混合物约10min,皂化反应基本完成,所得的混合物为___(填“悬浊液”、“乳浊液”、“溶液”或“胶体”)。
(3)向所得混合物中加入食盐细粒,静置一段时间,溶液分为上下两层,高级脂肪酸钠盐在___层,这个过程称为___。
(4)装置中长玻璃导管的作用为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】航天飞机用铝粉与高氯酸铵(NH4ClO4)的混合物为固体燃料,反应方程式表示为2NH4ClO4![]() N2↑+Cl2↑+2O2↑+4H2O。下列对该反应的叙述中错误的是( )
N2↑+Cl2↑+2O2↑+4H2O。下列对该反应的叙述中错误的是( )
A.瞬间产生大量高温气体推动航天飞机飞行
B.从能量变化的角度,主要是化学能转变为热能和动能
C.反应的焓变小于零
D.在方程式后增加ΔH及其数值即为热化学方程式
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com