
【题目】某同学将Fe+2FeCl3=3FeCl2设计成原电池装置如图所示.下列说法正确的是( ) 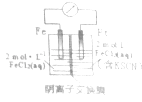
A.电子由铁极经溶液向铂极迁移
B.放电过程中交换膜右侧溶液颜色逐渐变浅
C.正极的电极反应式为Fe3++3e﹣=Fe
D.若转移2mole﹣ , 交换膜右侧溶液中约减少3mol离子
 轻松暑假总复习系列答案
轻松暑假总复习系列答案科目:高中化学 来源: 题型:
【题目】现有NaOH、Na2CO3和Ba(OH)2三种无色溶液,用一种试剂就可将它们鉴别出来,这种试剂是
A.HCl B.H2SO4 C.Na2SO4 D.CaCl2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】雾霾天气严重影响人们的生活,其中氮氧化物和硫氧化物是造成雾霾天气的主要原因之一.消除氮氧化物和硫氧化物有多种方法.可用活性炭还原法可以处理氮氧化物.某研究小组向某密闭容器中加入一定量的活性炭和NO,发生反应:C(s)+2NO(g)═N2(g)+CO2(g)△H=QkJmol﹣1 . 在T1℃时,反应进行到不同时间测得各物质的浓度如下:
时间(min) | 0 | 10 | 20 | 30 | 40 | 50 |
NO | 1.00 | 0.58 | 0.40 | 0.40 | 0.48 | 0.48 |
N2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
CO2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
0~10min内,CO2的平均反应速率v(CO2)= , 反应进行到30min时,NO 的转化率= .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表对某些反应方程式的评价合理的是( )
编号 | 离子方程式或电极反应式 | 评价 | |
A | 次氯酸钙溶液中通入足量SO2 | Ca2++ClO﹣+SO2+H2O=CaSO4+Cl﹣+2H+ | 正确 |
B | 硫酸铁溶液与氢氧化钡溶液混合 | Fe3++SO | 正确 |
C | 醋酸铵溶于水 | CH3COO﹣+NH | 错误,阴离子水解相互促进,应该用“=”号 |
D | 用惰性电极电解氯化铜和氯化钠的混合溶液一段时间 | 阴极:2Cu2++4e﹣=2Cu | 错误,该阴阳两极反应不可能同时发生 |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知 aAn、 b B(n1) 、cC n 、d D(n1) 具有相同的核外电子排布, 则 a 、b 、 c 、 d 由大到小的顺序是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组拟制备氯气并验证其一系列性质.Ⅰ.【查阅资料】
①当溴水浓度较小时,溶液颜色与氯水相似也呈黄色.
②硫代硫酸钠溶液在工业上可作为脱氯剂.
(1)Ⅱ.【性质验证】实验装置如图1所示(省略夹持装置)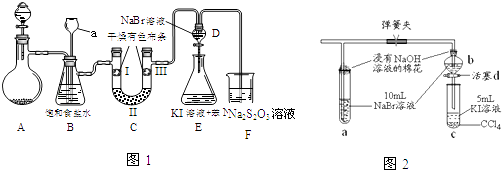
实验步骤:
a.检查装置气密性,按图2加入试剂.仪器a的名称是;装置CⅡ处加的试剂可以是(选填下列字母编号).
A.碱石灰 B.硅胶 C.浓硫酸 D.无水氯化钙
b.装置B的作用有 .
c.写出装置F中相应的离子反应方程式: .
(2)Ⅲ.【探究与反思】a.图1中设计装置D、E的目的是比较氯、溴、碘的非金属性,有同学认为该设计不能达到实验目的,其理由是 . 该组的同学思考后将上述D、E、F装置改为实验操作步骤如下:
①打开弹簧夹,缓缓通入氯气
②当a和b中的溶液都变为黄色时,夹紧弹簧夹.
③当a中溶液由黄色变为棕色时,停止通氯气.
④ .
b.设计步骤③的实验思想是 .
c.步骤④的操作是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在平板电视显示屏生产过程中产生的大量废玻璃粉末中含有二氧化铈(CeO2).
(1)①煅烧Ce(OH)CO3可制备CeO2 , 配平该反应的化学方程式Ce(OH)CO3+O2=CeO2+CO2+H2O
②已知在一定条件下,电解熔融状态的CeO2可制备Ce,在阴极获得铈,写出阴极的电极反应式;
(2)某课题组以上述废玻璃粉末(含有SiO2、Fe2O3、CeO2以及其他少量不溶于稀酸的物质)为原料,设计如图1流程对资源进行回收,得到Ce(OH)4和硫酸铁铵.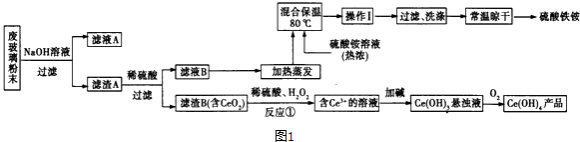
①得到滤渣B时,需要将其表面杂质洗涤干净.检验滤渣B已经洗涤干净的方法是 .
②反应①的离子方程式为 .
③如图2,氧化还原滴定法测定制得的Ce(OH)4产品的纯度.
该产品中Ce(OH)4的质量分数为(保留小数点后两位).若滴定所用FeSO4溶液已在空气中露置了一段时间,则测得该Ce(OH)4产品的纯度(“偏高”、“偏低”或“无影响”).
(3)操作I的名称是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com