
【题目】如图所示原电池,盐桥中装有含琼胶的KCl饱和溶液,相关的叙述中,不正确的是( )
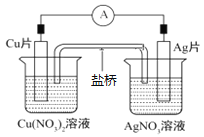
A. 正极的电极反应是Ag++e-=Ag
B. 电子沿导线由Cu片流向Ag片
C. 盐桥中的K+向Cu片移动
D. Cu片上发生氧化反应,Ag片上发生还原反应
 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案科目:高中化学 来源: 题型:
【题目】某反应使用催化剂后,其反应过程中能量变化如图。下列说法错误的是
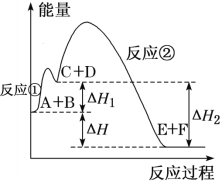
A.任何化学反应都伴随着能量的变化,能量变化主要是以热能的形式体现
B.总反应为反应物的总能量高于生成物总能量的反应,但反应①是吸热反应,
C.使用催化剂后,总反应的反应热不变、活化能减小
D.ΔH=ΔH2-ΔH1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用氨气还原氧化铜的方法测定铜的近似相对原子质量,反应的化学方程式为:2NH3+3CuO![]() N2+3Cu+3H2O,试回答:
N2+3Cu+3H2O,试回答:
(1)如果选用测定反应物CuO和生成物H2O的质量[m(CuO)、m(H2O)] 时,请用下图所列仪器设计一个简单的实验方案。
(2)①请写出用下图装置制备氨气的化学反应方程式___________________。

②仪器连接的顺序为(用字母编号表示,仪器可重复使用) ______________________,(d)中浓硫酸的作用是___________,实验完毕时观察到(a)中的现象是______________________。
③列出计算Cu的相对原子质量的表达式:______________________。
(2)有同学认为NH3与CuO反应生成的红色物质中可能含有Cu2O。已知Cu2O是红色粉末,在酸性溶液中,Cu+能自身发生氧化还原反应生成Cu2+和Cu。
①若CuO未完全分解,则所测定的Cu的相对原子质量会______________(偏大或偏小)。
②请设计一个简单的实验检验该红色物质中是否含有Cu2O________________。
(3)在解决了问题(2)后,又有同学提出:Cu2O与CuO的热稳定性哪个更强?于是他们进行了如下实验:取0.98 g Cu(OH)2固体,加热到80℃~100℃时,得到黑色固体粉末,继续加热到1000℃以上,黑色粉末全部变成红色粉末B。如下图所示:
据此可推得A为__________,且AB段发生的反应为_________________,
由此得到的热稳定性的结论是____________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为元素周期表短周期的一部分,下列有关A、B、C、D四种元素的叙述中不正确的是( )

A.A、C两元素形成的化合物都为共价化合物
B.AD2的电子式为![]()
C.B、C形成的化合物BC中所含化学键为非极性共价键
D.B2的结构式为N≡N
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳和氮的氢化物是广泛的化工原料,回答下列问题:
(1)工业上合成氨的反应为N2(g)+3H2(g)![]() 2NH3(g) △H=-92.2kJ/mol,反应过程中能量变化如图I所示。
2NH3(g) △H=-92.2kJ/mol,反应过程中能量变化如图I所示。

①氨分解:2NH3(g)![]() N2(g)+3H2(g)的活化能为_________kJ/mol
N2(g)+3H2(g)的活化能为_________kJ/mol
②合成氨时加入铁粉可以加快生成NH3的速率,在图I中画出加入铁粉后的能量变化曲线。_______
(2)联氨作火箭燃料的反应为:2N2H4(l)+N2O4(l)=3N2(g)+4H2O(g) △H1
已知:2O2(g)+N2(g)=N2O4(1) △H2 N2H4(1)+O2(g)=N2(g)+2H2O(g) △H3
上述热效应之间的关系式为△H1=____。某新型火箭用液氧/煤油代替联氨/N2O4,这种替换可能的好处是___(一条即可)。
(3)天然气制氢气是工业上制氢气的主要方法之一,其主要反应如下:
i.CH4(g)+H2O(g)![]() CO(g)+3H2(g) ΔH=-+206.4kJ/mol,
CO(g)+3H2(g) ΔH=-+206.4kJ/mol,
ii.CO(g)+ H2O(g)![]() CO2(g)+H2(g) ΔH=-41.0kJ/mol
CO2(g)+H2(g) ΔH=-41.0kJ/mol
在一定温度下,2L的密闭容器中加入a molCH4和2amolH2O发生反应,t min时反应达平衡,测得容器内CObmol、CO2cmol。回答下列问题:
①下列可判断体系达到平衡状态的是_______。
A.CO的体积分数不变 B.容器内气体密度不变 C.3v(CH4)=v(H2) D.![]() 不再变化
不再变化
②0~tmin反应速率v(CO2)=_____,CH4的的转化率为_____,反应ⅱ的平衡常数K=______。
③图Ⅱ中T℃之后c(CO2)随温度升高而减小的原因是_________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】叠氮化钠(NaN3)常用作汽车安全气囊中的药剂。实验室制取叠氮化钠的原理、实验装置及实验步骤如下:
①打开装置D导管上的旋塞,加热制取氨气。
②再加热装置A中的金属钠,使其熔化并充分反应后,再停止加热装置D并关闭旋塞。
③向装置A中b容器内充入加热介质并加热到210~220℃,然后通入N2O。
④冷却,向产物中加入乙醇(降低NaN3的溶解度),减压浓缩结晶后,再过滤,并用乙醚洗涤,晾干。

已知:I.NaN3是易溶于水的白色晶体,微溶于乙醇,不溶于乙醚;
II.NaNH2熔点210℃,沸点400℃,在水溶液中易水解。
请回答下列问题:
(1)装置B中盛放的药品为_____________;装置C的主要作用是______________________。
(2)步骤①中先加热通氨气的目的是_____________________________________;步骤②氨气与熔化的钠反应生成NaNH2的化学方程式为_______________________________。步骤③中最适宜的加热方式为 ___________(填“水浴加热”,“油浴加热”)。
(3)N2O可由NH4NO3在240~245℃分解制得(硝酸铵的熔点为169.6℃),则可选择的气体发生装置是(填序号)___________。

(4)生成NaN3的化学方程式为 _____________________________________。
(5)图中仪器a用的是铁质而不用玻璃,其主要原因是__________________。
(6)步骤④中用乙醚洗涤的主要目的是_______________________________。
(7)实验室用滴定法测定叠氮化钠样品中NaN3的质量分数:①将2.500 g试样配成500.00 mL溶液。②取50.00 mL溶液置于锥形瓶中,加入50.00 mL 0.1010 mol·L-1(NH4)2Ce(NO3)6溶液。③充分反应后,将溶液稍稀释,向溶液中加入8 mL浓硫酸,滴入3滴邻菲啰啉指示液,用0.0500mol·L-1(NH4)2Fe(SO4)2标准溶液滴定过量的Ce4+,消耗溶液体积为29.00mL。测定过程的反应方程式为:2(NH4)2Ce(NO3)6+2NaN3=4NH4NO3+2Ce(NO3)3+2NaNO3+3N2↑;Ce4++Fe2+=Ce3++Fe3+;试样中NaN3的质量分数为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科学家研发了一种室温下“可呼吸”的Na—CO2二次电池。将NaClO4溶于有机溶剂作为电解液,钠和负载碳纳米管的镍网分别作为电极材料,电池的总反应为:3CO2+4Na![]() 2Na2CO3+C。下列说法错误的是
2Na2CO3+C。下列说法错误的是

A. 放电时,ClO4-向负极移动
B. 充电时释放CO2,放电时吸收CO2
C. 放电时,正极反应为:3CO2+4e =2CO32-+C
D. 充电时,正极反应为:Na++e=Na
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关晶体的结构如图所示,下列说法中不正确的是
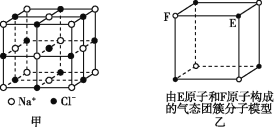
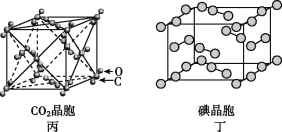
A. 在NaCl晶体(图甲)中,距Na+最近的Cl-形成正八面体
B. 该气态团簇分子(图乙)的分子式为EF或FE
C. 在CO2晶体(图丙)中,一个CO2分子周围有12个CO2分子紧邻
D. 在碘晶体(图丁)中,存在非极性共价键和范德华力
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜的相关化合物在化工、材料等领域有着广泛的应用。回答下列问题:
(1)基态Cu原子中,核外电子占据的最高能层的符号是___________,占据该能层电子的电子云轮廓图形状为__________;Cu2+价层电子的电子排布图为___________。
(2)离子晶体中Cu2O熔点比Cu2S熔点高,其原因是___________________________。
(3)Cu可与N、S,O等元素形成化合物,N、S、O三种元素的第一电离能由大到小的顺序为______________;在Cu的催化作用下,乙醇可被氧化为乙醛,乙醛分子中碳原子的杂化方式是________________。
(4)1mo[Cu(NH3)4]SO4中含有σ键的数目为___________。
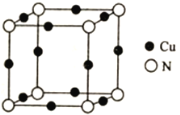
(5)Cu与N所形成的某种晶体的立方晶胞如图所示,其晶胞参数为anm。该晶体的化学式为___________,晶体的密度为___________g·cm-3(列出计算式即可,用NA表示阿伏加德罗常数)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com