
【题目】A为分子式为C7H8的芳香烃根据下面的反应路线及所给信息填空. 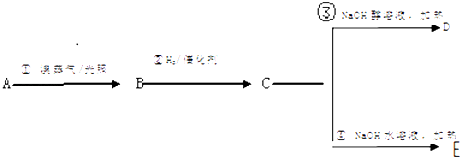
(1)A的名称是 .
(2)①的反应类型是;③的反应类型是 .
(3)简述B中卤素原子的检验方法
(4)反应①的化学方程式是 反应③的化学方程式是
反应④的化学方程式是 .
【答案】
(1)甲苯
(2)加成反应;消去反应
(3)取少量B溶液于试管中,加NaOH溶液加热,一段时间后,加入足量HNO3酸化,再加Ag NO3 , 若产生淡黄色沉淀则为溴元素
(4)![]() +Br2
+Br2 ![]()
![]() +HBr;
+HBr;![]() +NaOH
+NaOH ![]()
![]() +NaBr+H2O;
+NaBr+H2O;![]() +NaOH
+NaOH ![]()
![]() +NaBr
+NaBr
【解析】解:A为分子式为C7H8的芳香烃,则A为 ![]() ,反应①为甲苯在光照条件下发生甲基上的取代反应,反应②发生苯环与氢气的加成反应,反应③为醇的消去反应,反应为卤代烃发生水解反应,可推知B为
,反应①为甲苯在光照条件下发生甲基上的取代反应,反应②发生苯环与氢气的加成反应,反应③为醇的消去反应,反应为卤代烃发生水解反应,可推知B为 ![]() ,C为
,C为 ![]() ,D为
,D为 ![]() ,E为
,E为 ![]() .(1)A的名称是甲苯,所以答案是:甲苯;(2)①的反应类型是:取代反应.③的反应类型是消去反应,所以答案是:取代反应;消去反应;(3)B(
.(1)A的名称是甲苯,所以答案是:甲苯;(2)①的反应类型是:取代反应.③的反应类型是消去反应,所以答案是:取代反应;消去反应;(3)B( ![]() )中卤素原子的检验方法:取少量B溶液于试管中,加NaOH溶液加热,一段时间后,加入足量HNO3酸化,再加Ag NO3 , 若产生淡黄色沉淀则为溴元素, 所以答案是:取少量B溶液于试管中,加NaOH溶液加热,一段时间后,加入足量HNO3酸化,再加Ag NO3 , 若产生淡黄色沉淀则为溴元素;(4)反应①的化学方程式是:
)中卤素原子的检验方法:取少量B溶液于试管中,加NaOH溶液加热,一段时间后,加入足量HNO3酸化,再加Ag NO3 , 若产生淡黄色沉淀则为溴元素, 所以答案是:取少量B溶液于试管中,加NaOH溶液加热,一段时间后,加入足量HNO3酸化,再加Ag NO3 , 若产生淡黄色沉淀则为溴元素;(4)反应①的化学方程式是: ![]() +Br2
+Br2 ![]()
![]() +HBr,
+HBr,
反应③的化学方程式是: ![]() +NaOH
+NaOH ![]()
![]() +NaBr+H2O,
+NaBr+H2O,
反应④的化学方程式是: ![]() +NaOH
+NaOH ![]()
![]() +NaBr,
+NaBr,
所以答案是: ![]() +Br2
+Br2 ![]()
![]() +HBr;
+HBr;![]() +NaOH
+NaOH ![]()
![]() +NaBr+H2O;
+NaBr+H2O;![]() +NaOH
+NaOH ![]()
![]() +NaBr.
+NaBr.


 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案科目:高中化学 来源: 题型:
【题目】下列有关热化学方程式的叙述正确的是( )
A.反应物的总能量高于生成物的总能量时,该反应常温下即可发生
B.氢气燃烧热为285.8kJmol﹣1 , 则有H2(g)+1/2O2(g)=H2O(g)△H=﹣285.8kJmol﹣1
C.将1molBa(OH)2的稀溶液与稀盐酸完全中和,放出114.6kJ的热量,热化学方程式为:OH﹣(aq)+H+(aq)=H2O(l)△H=﹣114.6kJmol﹣1
D.2SO2(g)+O2(g)2SO3(g);△H=﹣QkJmol﹣1(Q>0),则将2molSO2(g)和足量O2置于一密闭容器中,充分反应后放出的热量一定小于QkJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在无色透明的酸性溶液中,可大量共存的溶液是 ( )
A. Cu2+、Ca2+、Cl、NO3B. Mg2+、SO42-、NH4+、Cl-
C. K+、Na+、HCO3-、Cl-D. K+、MnO4、Cl、S2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯及其化合物对人类生产及生活有重要作用。
(1)氯的原子结构示意图为_______;实验室氯气的尾气处理常用NaOH溶液,请用离子方程式表示该反应:________;工业上将氯气通入冷的消石灰制取漂白粉,漂白粉的有效成分是___(填化学式)。
(2)NaClO2的漂白能力是漂白粉的4到5倍。NaClO2广泛用于造纸工业、污水处理等。工业上生产NaClO2的工艺流程如下:
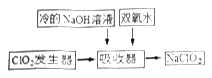
①发生器中用NaClO3与Na2SO3在酸性环境下反应制备ClO2,则氧化剂与还原剂的物质的量之比为:_____________。
②吸收器中生成NaClO2反应的离子方程式为_______,吸收器中的反应温度不能过高,可能的原因为__________。
③Cl2和ClO2均能将工业废水中得CN-氧化成无毒的物质,而自身被还原为Cl-,则处理相同量的CN-所需Cl2的质量是ClO2的多少倍。______(计算结果保留一位小数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物A的分子式为C10H10O5 , 能发生如下变化.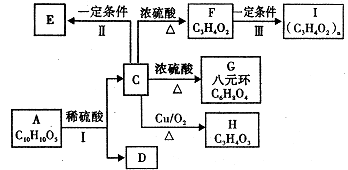
已知:①A、C、D均能与NaHC03反应;
②只有A、D能与FeCl3溶液发生显色反应;
③A苯环上只有两个对位的取代基;
④F能使溴水褪色;
⑤H能发生银镜反
应.根据题意回答下列问题:
(1)反应I的反应类型是 .
(2)F中含氧官能团的名称为 , F在一定条件下与氢气加成,生成分子式为C3H6O2的有机物,该有机物的名称为 .
(3)G的结构简式为 , 反应Ⅲ的化学方程式为 .
(4)写出A与足量NaOH溶液共热的化学方程式 .
(5)D有多种同分异构体,写出同时满足下列要求的一种同分异构体的结构简式①能与FeCl3溶液发生显色反应
②能发生银镜反应但不能水解
③苯环上的一卤代物只有2种.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学反应2A(g)B(g)+D(g)在四种不同条件下进行,B、D起始浓度为零,反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表:
实验 | 时间 | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
1 | 800℃ | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
2 | 800℃ | c2 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
3 | 800℃ | c3 | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
4 | 820℃ | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
根据上述数据,完成下列填空:
(1)在实验1,反应在10至20分钟时间内平均速率为mol/(Lmin).
(2)在实验2,A的初始浓度c2=mol/L,推测实验2中还隐含的条件是 .
(3)设实验3的反应速率为v3 , 实验1的反应速率为v1 , 则v3v1(填>、<、=),且c31.0mol/L(填>、<、=)
(4)比较实验4和实验1,可推测该反应是反应(选填“吸热”、“放热”).理由是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取浓度相等的NaOH和HCl溶液,以3:2体积比相混合(忽略溶液体积变化),所得溶液中的c(OH﹣)=0.01mol/L,则原溶液的浓度为( )
A. 0.01 mol/L B. 0.017 mol/L C. 0.05 mol/L D. 0.50 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有机化学反应方程式书写及反应类型均正确的是( )
A.CH2=CH2+HCl ![]() CH3CH2Cl????????????????????? 加聚反应
CH3CH2Cl????????????????????? 加聚反应
B.CH3COOH+CH3CH2OH ![]() CH3COOCH2CH3+H2O??? 酯化反应
CH3COOCH2CH3+H2O??? 酯化反应
C.![]() ??????????? 加成反应
??????????? 加成反应
D.![]() ??????????? 取代反应
??????????? 取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是依据各种元素(原子)的性质与原子序数(1-20)的关系而作出的,各图的纵轴可能代表下列某一性质:核电荷数、中子数、最高正化合价、原子半径、得电子能力,A、B、C分别代表三种元素。注意:图3中原子序数为8、9的元素和图4中原子序数为2、10、 18的元素在纵轴上没有对应的数值。
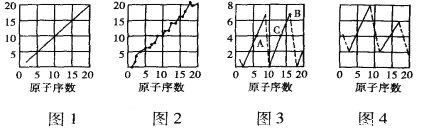
请回答下列问题:
(1)图2、图3、图4的纵轴分别代表的性质是_____、____、______。
(2)B元素的名称是________,工业上制备C的单质的化学反应方程式为______。
(3)元素A和元素C的气态氢化物的沸点高低及原因______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com