
【题目】关于石油和石油化工的说法错误的是( )
A. 石油的主要成分是碳氢化合物
B. 石油分馏得到的各馏分仍是混合物
C. 石油裂解气的主要成分是甲烷
D. 石油裂化的目的是为了提高轻质油的产量
科目:高中化学 来源: 题型:
【题目】铜版画的一种制版方法。以沥青涂于薄铜板表面作防腐膜,用刀刻去防腐膜作画,然后放在FeCl3腐蚀液中。刮去膜之处被腐蚀,形成凹线。印刷时凹线可储油墨,在铜版机纸压制下油墨吸于纸上,形成典雅、庄重的铜版画。

(1)写出FeCl3腐蚀铜板的离子方程式___________________
(2)下列措施可以加快铜板的腐蚀速率的有____________(填编号)
A. 加热 B. 加氯化铜 C. 加少量碳粉 D. 加盐酸
(3)通常不采用加快腐蚀速率的原因是_________________
(4)除去沥青防腐膜后版即形成。可用________除去防腐膜(填编号)
A. 饱和Na2CO3溶液 B. 煤油 C. 酸液 D.碱液
(5)实验室用固体氯化铁配置FeCl3溶液的简单操作是_____________
(6)腐蚀后的废液(酸性)中加入NaNO3,产生NO气体,写出发生反应的离子方程式,并注明电子转移的方向和数目:__________________________
(7)要验证腐蚀后的废液中含有Fe3+,可在溶液中加入试剂_________,现象_______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电化学气敏传感器可用于监测环境中NH3的含量,其工作原理示意图如下。下列说法不正确的是( )
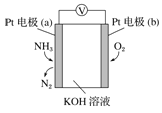
A.溶液中OH-向电极a移动
B.O2在电极b上发生还原反应
C.反应消耗的NH3与O2的物质的量之比为 4:5
D.电极 a 的反应式为 2NH3-6e-+6OH-=N2+6H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水合肼(N2H4·H2O)是无色、有强还原性的液体,实验室制备水合肼的原理为:
CO(NH2)2+2NaOH+NaClO==Na2CO3+N2H4·H2O+NaCl
据此,某学生设计了下列实验.
【制备NaClO溶液】实验装置如下图左图所示(部分夹持装置已省略)
已知:3NaClO![]() 2NaCl+NaClO3
2NaCl+NaClO3

(1)配制30 %NaOH溶液时,所需玻璃仪器除量筒外还有__________(填字母)。
A.容量瓶 B.烧杯 C.移液管 D.玻璃棒
(2)装置I中发生的离子反应方程式是_______________;Ⅱ中玻璃管a的作用为____________;为了提高NaClO的产率,需对I中产生的Cl2进行净化,所用试剂是________________;Ⅱ中用冰水浴控制温度在30℃以下,其主要目的___________________
【制取水合肼】实验装置如上图右图所示
(3)反应过程中,如果分液漏斗中溶液的滴速过快, 部分N2 H4·H2O参与A中反应并产生大量氮气,产品产率因此降低,请写出降低产率的相关化学反应方程式____________________;充分反应后,加热蒸馏A内的溶液即可得到水合肼的粗产品,B装置的名称是______________
【测定肼的含量】
(4)称取馏分0.3000 g,加水配成20.0 mL溶液,一定条件下用0.1500 mol.L-1 的I2溶液滴定。
已知: N2H4·H2O + 2I2 = N2↑+ 4HI + H2O。
①滴定时,可以选用的指示剂为____________;
②实验测得消耗I2溶液的平均值为20. 00 mL,馏分中N2H4·H2O的质量分数为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】POCl3常用作半导体掺杂剂及光导纤维原料,实验室制备POCl3并测定产品含量的实验过程如下:

实验室制备POCl3。
采用氧气氧化液态PCl3法制取POCl3,实验装置(加热及夹持仪器略)如下:

(1)B中所盛的试剂是______,干燥管的作用是________。
(2)装置C中生成POCl3的化学方程式为______________。
(3)装置B的作用除干燥O2外,还有______、_______。
(4)反应温度要控制在60~65℃,原因是________________。
测定POCl3产品的含量:
实验步骤:
①制备POCl3实验结束后,待三颈瓶中液体冷却至室温,准确称取16.73gPOC13产品,置于盛有60.00mL蒸馏水的水解瓶中摇动至完全水解,将水解液配成100.00mL溶液。
②取10.00mL溶液于锥形瓶中,加入10.00mL3.2mol/LAgNO3标准溶液。
③加入少许硝基苯(硝基苯无色、难溶于水、密度比水大)。
④以Fe2(SO4)3溶液为指示剂,用0 .2mol/LKSCN溶液滴定过量的AgNO3溶液,达到滴定终点时共用去10.00mL KSCN溶液。
(5)步骤③中加入硝基苯的作用是__________。
(6)达到滴定终点时的现象为__________。
(7)产品中POCl3的百分含量为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室保存下列物质的方法中,不正确的是
A. 少量金属钠保存在煤油里
B. 烧碱溶液盛装在带玻璃塞的磨口玻璃瓶中
C. 新制氯水通常保存在棕色试剂瓶中
D. FeSO4溶液存放在加有少量铁粉的试剂瓶中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列陈述正确并且有因果关系的是( )
A. SiO2有导电性,可用于制备光导纤维
B. 浓硫酸具有氧化性,可用于干燥H2
C. Al2O3具有很高的熔点,可用于制造熔融烧碱的坩埚
D. FeCl3溶液能与Cu反应,可用于蚀刻印刷电路板
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F六种元素的原子序数依次递增。己知:
①已知F为第四周元素,除最外层只有一个电子外,其他各层上均填满电子,另外五种元素均为短周期主族元素;②A、C原子p轨道的电子数分别为2和4;③D原子最外层电子数为偶数;④E原子价电子(外围电子)排布为msnmpn-1。请回答下列问题:
(1)下列叙述正确的是_____(填序号)。
A.金属键的强弱:D>E B.基态原子第一电离能:D>E
C.六种元素中,电负性最大的元素是E D.晶格能:NaCl<DCl2
(2)F基态原子的核外电子排布式为______;与F同一周期的元素中基态原子轨道上成单电子数最多的元素为______ (填元素符号)。
(3)A与C形成的非极性分子,该分子与过量强碱反应生成的酸根离子的空间构型为_____。
(4)已知原子数和价电子数相同的分子或离子为等电子体,互为等电子体的微粒结构相同,B 3-中心原子的杂化轨道类型为____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com