
| A、7.2g | B、8.0g |
| C、9.0g | D、10.7g |
 阶梯计算系列答案
阶梯计算系列答案科目:高中化学 来源: 题型:
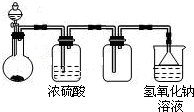
| A、浓氨水与氧化钙固体反应制氨气 |
| B、稀硫酸与硫化亚铁固体反应制硫化氢 |
| C、浓盐酸与次氯酸钙固体反应制氯气 |
| D、饱和食盐水与电石反应制乙炔 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、苯、乙烯都既能发生加成反应,又能发生氧化反应 |
| B、石油的分馏和煤的干馏都是物理变化 |
| C、淀粉、植物油和蛋白质都是天然高分子,在一定条件下都能发生水解反应 |
| D、棉花、蚕丝、羊毛燃烧后都只生成CO2和H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| t/s | 0 | 50 | 150 | 250 | 350 |
| n(PCl3)/mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
| A、反应在前50 s的平均速率为v(PCl3)=0.0032mol?L-1?s-1 |
| B、保持其他条件不变,升高温度,平衡时,c(PCl3)=0.11mol?L-1,则反应的△H<0 |
| C、相同温度下,起始时向容器中充入1.0molPCl5、0.20molPCl3和0.20molCl2,达到平衡前v(正)>v(逆) |
| D、相同温度下,起始时向容器中充入2.0molPCl5、2.0molCl2,达到平衡时,PCl5的转化率大于20% |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 催化剂 |
| 加热 |
| A、使用催化剂是为了加快反应速率 |
| B、增大O2浓度可以使SO2转化率达到100% |
| C、加压可以增大反应速率 |
| D、增大O2浓度可以增大反应速率 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、摩尔是可以把物质的质量与微观粒子数联系起来的一个基本物理量 |
| B、0.012 kg 12C中所含的碳原子数为NA |
| C、物质的摩尔质量等于其相对分子(原子)质量 |
| D、1mol任何物质都含有约6.02×1023个原子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com