
����Ŀ�������������͵���Ҫ�ɷ�֮һ���������������Ҫ���壺
��ӦI�����ѽ⣩��CH3COOH(g)2CO(g)+2H2(g) ��H1
��ӦII�����Ȼ�����CH3COOH(g)CH4(g)+CO2(g) ��H2
��֪����ӦI�Ļ��Ϊ��E5-E2��kJ����ӦI�淴Ӧ�Ļ��Ϊ��E5-E3��kJ����ӦII�Ļ��Ϊ��E4-E2��kJ����ӦII�淴Ӧ�Ļ��Ϊ��E4-E1��kJ��E1��E5������������
��1����H1+��H2=___________kJ/mol (���й�E�Ĵ���ʽ��ʾ)��
��2���ڲ�ͬ�¶��£����ܱ������г������������������Ӧ��ͬʱ���ø�����IJ������¶ȵĹ�ϵ��ͼ��ʾ��

��Լ650��֮ǰ���������ʵ��ڼ����ԭ���ǣ�________________________________��
��Լ650��֮�������¶����ߺ��������ʸ��ڼ����ԭ���ǣ�___________�������ţ�
a. ��ӦII���ʼ���
b. ��ӦI���ʼӿ�ij̶ȱȷ�ӦII��
c. ��ӦI�����ƶ�������ӦII�����ƶ�
d. ��ӦI�����ƶ��ij̶ȴ��ڷ�ӦII�����ƶ��ij̶�
������ͼ���������������һ������������ĸ���Ӧ�������ǣ�______________��
��3��Ͷ��һ���������ᣬ����ͬѹǿ�£�������ͬ��Ӧʱ��������ʵ�����ݣ�
�¶ȣ����� | ���� | CH3COOHת���� | H2��ѡ���� |
550 | �� | 14.5 | 40.2 |
550 | �� | 11.1 | 62.1 |
600 | �� | 11.2 | 41.2 |
600 | �� | 10.3 | 63.3 |
��H2��ѡ���ԣ�ת����CH3COOH������H2�İٷֱ���
������ʵ�����ݱ���������ͬ�¶��²�ͬ�Ĵ�����CH3COOHת����H2��ѡ������������Ӱ�죬��ԭ����________��
�����������CH3COOHת��ΪH2ƽ��ת���ʵĴ�ʩ��________��
A��ʹ�ô����� B��ʹ�ô�����
C�����߷�Ӧ�¶� D�����ӷ�Ӧ���Ũ��
���𰸡�E1+E3-2E2 ��ӦI�Ļ�ܸ��ڷ�ӦII��ʹ����H2�����ʵ�������CH4������ bc ���ݷ�ӦI����������CO��H2�ı���Ϊ1��1����ͼ��������������IJ�����Ȼ��1��1�� ��ʱ��Ӧδ�ﵽƽ�⣬��ͬ�Ĵ����Է�Ӧ��Ĵ�������ͬ������ڸ�ʱ���¶Լ״�ѡ������Ӱ�졣 C 16.7% ![]()
��������
(1)��֪����ӦI�Ļ��Ϊ(E5-E2)kJ����ӦI�淴Ӧ�Ļ��Ϊ(E5-E3)kJ����ӦII�Ļ��Ϊ(E4-E2)kJ����ӦII�淴Ӧ�Ļ��Ϊ(E4-E1)kJ��E1��E5��������������������ϵ������ͼ�����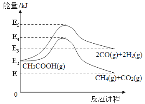 ��������H=������������-��Ӧ�����������㣻
��������H=������������-��Ӧ�����������㣻
(2)��Լ650��֮ǰ���������Ӧ��ܵ����ʿ죬���������ʵ��ڼ��飻
�����ѽⷴӦCH3COOH(g)��2CO(g)+2H2(g)���������ȷ�Ӧ�������¶������ڷ�Ӧ������У�����ƽ����еij̶������������ӦCH3COOH(g)CH4(g)+CO2(g)�����Ƿ��ȷ�Ӧ�������¶ȣ���Ӧ��������У�����ƽ����еij̶ȼ�С���ݴ˽��
��ͼ�������֪����Ӧ������CO��H2�ı���Ϊ1��1�����ͼ�����������ʵ���֮�ȷ����жϣ�
(3)����ͬ�Ĵ����Ĵ�������ͬ���Ҵ�������ѡ���ԣ�
��CH3COOH(g)2CO(g)+2H2(g)���������ȷ�Ӧ�����CH3COOHת��ΪH2ƽ��ת���ʣ�Ӧʹƽ�������ƶ����������¶ȣ���С�������Ũ�ȣ�
(4)����ʼʱn(CH3COOH)=1mol�����ѽⷴӦ��������40%���������ѽⷴӦCH3COOH(g)2CO(g)+2H2(g)��n(CO)=n(H2)=0.4mol��2=0.8mol���������Ӧ��������20%�������������ӦCH3COOH(g)CH4(g)+CO2(g)��n(CH4)=n(CO2)=0.2mol��ƽ��ʱʣ��n(CH3COOH)=1mol0.4mol0.2mol=0.4mol���������������ʽ��ѹǿƽ�ⳣ������ʽ�ֱ���㡣
(1)��֪����ӦI�Ļ��Ϊ(E5-E2)kJ����ӦI�淴Ӧ�Ļ��Ϊ(E5-E3)kJ����ӦII�Ļ��Ϊ(E4-E2)kJ����ӦII�淴Ӧ�Ļ��Ϊ(E4-E1)kJ��E1��E5��������������������ϵ������ͼ�����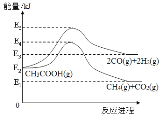 ��������H=������������-��Ӧ���������ɵã���H1=E3-E2����H2=E1-E2�����H1+��H2= E3-E2+E1-E2= E3+E1-2E2��
��������H=������������-��Ӧ���������ɵã���H1=E3-E2����H2=E1-E2�����H1+��H2= E3-E2+E1-E2= E3+E1-2E2��
(2)��Լ650��֮ǰ���������Ӧ��ܵ����ʿ죬��ӦI�Ļ�ܸ��ڷ�ӦII��ʹ����H2�����ʵ�������CH4�����ʣ����������ʵ��ڼ��飻
������(1)������ͼ��������ѽⷴӦCH3COOH(g)2CO(g)+2H2(g)���������ȷ�Ӧ�������¶������ڷ�Ӧ������У�����ƽ����еij̶�����ʹH2�����������࣬���������ӦCH3COOH(g)CH4(g)+CO2(g)�����Ƿ��ȷ�Ӧ�������¶ȣ���Ӧ��������У�ʹCH4�����������٣����������¶����ߺ����ѽⷴӦ���ʼӿ죬ͬʱ�������ʸ��ڼ��飬��ѡbc��
����Ӧ��(���ѽ�):CH3COOH(g)2CO(g)+2H2(g)���ݷ�ӦI����������CO��H2�ı���Ϊ1:1����ͼ��������������IJ�����Ȼ��1:1��˵����������һ������������ĸ���Ӧ��
(3)����ͼ�ϵ����ݿ���֪����һ��ʱ���ڣ���Ӧδ�ﵽƽ�⣬��ͬ�Ĵ����Է�Ӧ���Ĵ�������ͬ������ڸ�ʱ���¶Լ״�ѡ������Ӱ�죻
��A���������ı�ƽ��ת���ʣ���A����
B���������ı�ƽ��ת���ʣ���B����
C����ӦIΪ���ȷ�Ӧ�����������¶ȣ�ƽ��������У�ת��������C��ȷ��
D������Ӧ���Ũ�ȣ���ʹƽ��������У�����������CH3COOH��ת���ʣ���D����
��ѡC��
(4)����ʼʱn(CH3COOH)=1mol�����ѽⷴӦ��������40%���������ѽⷴӦCH3COOH(g)2CO(g)+2H2(g)��n(CO)=n(H2)=0.4mol��2=0.8mol���������Ӧ��������20%�������������ӦCH3COOH(g)CH4(g)+CO2(g)��n(CH4)=n(CO2)=0.2mol��ʣ��n(CH3COOH)=1mol0.4mol0.2mol=0.4mol������ƽ��ʱ�����������![]() ��100%=16.7%��ƽ��ʱp(CO)=p(H2)=
��100%=16.7%��ƽ��ʱp(CO)=p(H2)=![]() ��p=
��p=![]() ��p(CH3COOH)=
��p(CH3COOH)=![]() ��p=
��p=![]() �����ѽⷴӦ��ƽ�ⳣ��Kp=
�����ѽⷴӦ��ƽ�ⳣ��Kp=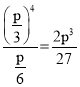 ��
��


 ͨ��ѧ��Ĭд����ϵ�д�
ͨ��ѧ��Ĭд����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������(FePO4)�������缫���ϡ��մɼ���ҩ�ȡ���������(��Ҫ�ɷ���FeS2������SiO2��Fe3O4)Ϊԭ���Ʊ����������������£�
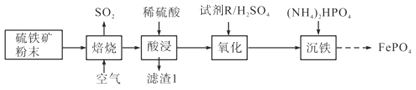
(1)����ʱFeS2ת��ΪFe2O3���÷�Ӧ���������뻹ԭ�����ʵ���֮��Ϊ___________��
(2)�������ʱΪ�����ܽ⣬��ȡ�Ĵ�ʩ��_________________________________(��д����)��
(3)����1��___________��
(4)���������ǽ�������Fe2��ת��ΪFe3�����Լ�R���ѡ��___________(����ĸ)��
A.KMnO4 B.H2O2 C.ϡ����
(5)д������ʱ��Ӧ�����ӷ���ʽ______________________________________________��
(6)1 t�������к�FeS2 a mol��Fe3O4 b mol����������������c t��FePO4����FePO4�IJ���Ϊ__________________��(�ú�a��b��c����ʽ��ʾ�����ػ���)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��W��X��Y��Z���ֶ�����Ԫ�أ����������ڱ���λ����ͼ��ʾ������˵������ȷ����(����)
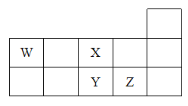
A.Z��Y��W������������ˮ������������μ���
B.Z��Y��X��ԭ�Ӱ뾶���μ�С���ǽ��������μ���
C.��̬�⻯����ȶ��ԣ�H2X��H2Y
D.W��λ���ǵڶ����ڵڢ�A��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪M�Ƕ����ڽ���Ԫ�أ�X��Y�Ƕ����ڷǽ���Ԫ�أ���X��M��Y��ԭ��������������������ɵ�����M3XY(����ΪM2XMY)��һ�����õ����ӵ��塣�о����ڳ�ѹ���������з�Ӧ�ϳ�M3XY: 2M + 2MXA +2MY==2M3XY +A2�����г��³�ѹ��A2����ɫ��ζ���壬��֪������Ӧ������0.92 g M�ĵ��ʿɵõ���״����448 mL��A2�������й�˵����ȷ����
A.�����Ӱ뾶��Y��M��X
B.���⻯��ķе㣺XС��Y
C.MXA�ǹ��ۻ�����
D.M3XY����ˮ����Һ�ʼ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ�Ͽ����õ��ԭ�������������������л���Ⱦ��ķ�ˮ����ԭ����ͼ��ʾ������˵����������

A.���������ڵ缫A�Ϸ���������Ӧ���缫AΪ����
B.�������ӱ������õ���ǿ����������ΪCl2��O2
C.�л���Ⱦ����ʯī�缫�ϱ���ԭΪ����Ⱦ����
D.����������ΪOH�����缫B�Ϸ����ķ�ӦΪ2H2O+2e��=H2��+ 2OH��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ѱ���Ϊ��������֮��ĵ�����������ش��������⣺
��1����̬��ԭ�ӵļ۲�����Ų�ͼΪ__________����ԭ�Ӻ����______�ֿռ��˶�״̬��ͬ�ĵ��ӣ������ѵĶѻ���ʽ��ͼ��ʾ��Ϊ________(��ѻ���ʽ)�ѻ�
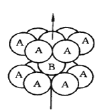
��2������֪TiCl4��ͨ�����������ɫҺ�壬�۵�Ϊ��37�����е�Ϊ136���������ڽṹ�������Ƶ�CCl4����Ҫԭ����_______��
��TiCl4������Ũ�����H2[TiCl6]������Һ�м���NH4ClŨ��Һ��������ɫ��(NH4)2[TiCl6]���塣�þ�����������֮�����������______��
A�����Ӽ� B�����ۼ� C�����Ӽ������� D����� E��������
��3���������Ѿ�����������Ϊ��״�ۺ���ʽ���ṹ��ͼ��ʾ������Ti-O-Ti��һ��ֱ���ϡ��������ӻ�ѧʽΪ__________������Oԭ�ӵ��ӻ���ʽΪ_______��
![]()
��4��2016��7�£��о���Ա������ij���ѽ�Ͻ�Ļ�ѧʽ��Ti3Au�����������������ԣ���������˹��Źؽں�ϥ�ؽڣ��侧���ṹ��ͼ��ʾ����������Ϊa pm�������Tiԭ�Ӿ���Ϊ![]() ��Aԭ�ӵ��������Ϊ��
��Aԭ�ӵ��������Ϊ��![]() ,
,![]() ,
,![]() ������Bԭ���������Ϊ_______������Tiԭ���ν���Tiԭ����_______����Ti-Au���������Ϊ_______pm
������Bԭ���������Ϊ_______������Tiԭ���ν���Tiԭ����_______����Ti-Au���������Ϊ_______pm

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������ij���ӵ�Ũ��Խ��ʱ���������Ի�ԭ��Խǿ��������һ���ʣ�������Ƴ���ͼ��ʾ��Ũ������(��綯��ȡ�������ʵ�Ũ�Ȳ����һ�����ʴӸ�Ũ�����Ũ��ת�ƶ�������)��ʵ�鿪ʼ�ȶϿ�K1���պ�K2�����ֵ�����ָ�뷢��ƫת������˵���������
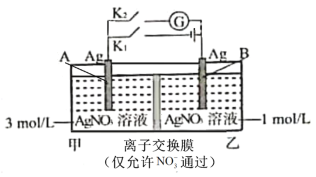
A.�Ͽ�K1���պ�K2��һ��ʱ��������ָ����㣬��ʱ����Ag+Ũ�����
B.�Ͽ�K1���պ�K2����ת��0.1mol e-ʱ���ҳ���Һ��������17.0 g
C.��������ָ�����Ͽ�K2���պ�K1��һ��ʱ���B�缫����������
D.��������ָ�����Ͽ�K2���պ�K1���ҳ���ҺŨ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪����ԭ��HSO��3>I����������IO��3>I2���ں�0.3mol NaHSO3����Һ����μ���KIO3��Һ������KIO3������I2�����ʵ����Ĺ�ϵ��������ͼ��ʾ������˵������ȷ����
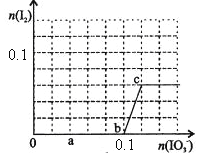
A��0��b��ķ�Ӧ�����������ӷ���ʽ��ʾ��3HSO3����IO3��=3SO42����I����3H��
B��a��ʱ����NaHSO3�����ʵ���Ϊ0.12mol
C������Һ��I����I2�����ʵ���֮��Ϊ5��2ʱ�������KIO3Ϊ0.18mol
D��b��ʱ�Ļ�ԭ���������KI��NaI��b��c��Ļ�ԭ������I2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ɽ���ۺ��� P �ĺϳ�·����ͼ��
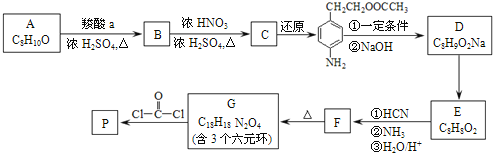
��֪��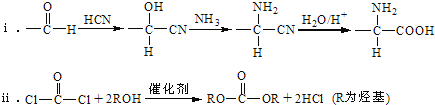 .
.
��1��A���������������______��
��2������a�ĵ��뷽��ʽ��______��
��3��B��C�Ļ�ѧ����ʽ��______��
��4��������D�����ϵ�һ�ȴ�����2�֣�D�Ľṹ��ʽ��______��
��5��E��F�з�Ӧ�ٺ͢ڵķ�Ӧ���ͷֱ���______��______��
��6��F�Ľṹ��ʽ��______��
��7��G���ۺ���P�Ļ�ѧ����ʽ��______��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com