
【题目】氧杂环化合物R具有消炎、抗肿瘤的作用,分子结构如图所示,下列有关R的叙述错误的是
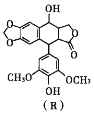
A.分子式为C21H22O8
B.分子中含有3种官能团
C.1mol R与NaOH溶液反应,最多消耗2mol NaOH
D.发生消去反应后的有机物分子中含有2个手性碳原子
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】根据下列图示所得出的结论正确的是( )

A. 图甲表示1 mL pH=2某一元酸溶液加水稀释时,pH随溶液总体积的变化曲线,说明该酸是强酸
B. 图乙表示恒容密闭容器中其他条件相同时改变温度,反应CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g)中n(CH3OH)随时间的变化曲线,说明反应平衡常数KⅠ>KⅡ
CH3OH(g)+H2O(g)中n(CH3OH)随时间的变化曲线,说明反应平衡常数KⅠ>KⅡ
C. 图丙表示不同温度下水溶液中-lg c(H+)、-lg c(OH-)变化曲线,说明T1>T2
D. 图丁表示1 mol H2和0.5 mol O2反应生成1 mol H2O过程中的能量变化曲线,说明H2的燃烧热是241.8 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:CH3CH=CH2+HBr→CH3CHBrCH3,1mol某烃A充分燃烧后可以得到8molCO2和4molH2O。该烃A在不同条件下能发生如图所示的一系列变化。

(1)A的化学式:____________,A的结构简式:__________。
(2)上述反应中,①是__________反应,⑥是__________反应(填反应类型)。
(3)写出 C、D、E 物质的结构简式:C ___________; D _________; E __________。
(4)写出 D→F反应的化学方程式__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法错误的是( )
A. ![]() 、
、![]() 、H+和H2是氢元素的四种不同粒子
、H+和H2是氢元素的四种不同粒子
B. ![]() 和
和 ![]() 、石墨和金刚石均为同素异形体
、石墨和金刚石均为同素异形体
C. 1H和2H是不同的核素
D. 12C和14C互为同位素,物理性质不同,但化学性质几乎完全相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实能用勒夏特列原理解释的是( )
A.煅烧粉碎的黄铁矿矿石有利于SO2的生成
B.合成氨工业中使用铁触媒做催化剂
C.用饱和食盐水除去氯气中氯化氢杂质
D.容器中有2NO2(g)![]() N2O4(g),增大压强颜色变深
N2O4(g),增大压强颜色变深
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下存在反应:H2(g) + I2(g)![]() 2HI(g) ΔH<0,现有三个相同的1 L恒容绝热(与外界没有热量交换)密闭容器Ⅰ、Ⅱ、Ⅲ,在Ⅰ中充入1 mol H2和1 mol I2(g),在Ⅱ中充入2 molHI(g) ,在Ⅲ中充入2 mol H2和2 mol I2(g),700 ℃条件下开始反应。达到平衡时,下列说法正确的是( )
2HI(g) ΔH<0,现有三个相同的1 L恒容绝热(与外界没有热量交换)密闭容器Ⅰ、Ⅱ、Ⅲ,在Ⅰ中充入1 mol H2和1 mol I2(g),在Ⅱ中充入2 molHI(g) ,在Ⅲ中充入2 mol H2和2 mol I2(g),700 ℃条件下开始反应。达到平衡时,下列说法正确的是( )
A. 容器Ⅰ、Ⅱ中正反应速率相同
B. 容器Ⅰ、Ⅲ中反应的平衡常数相同
C. 容器Ⅰ中的气体颜色比容器Ⅱ中的气体颜色深
D. 容器Ⅰ中H2的转化率与容器Ⅱ中HI的转化率之和等于1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】重铬酸钾是工业合成的常用氧化剂和催化剂,如图所示的微生物电池,能利用K2Cr2O7实现对含苯酚(或醛类)废水的有效处理,该电池工作一段时间后,中间室内的NaC1溶液浓度减小,则下列叙述正确的是

A.a电极为负极,电子从a电极经过中间室到达b电极
B.M为阳离子交换膜,电解过程中中间室内的n(NaC1)减小
C.处理含苯甲醛废水时a电极反应式为:C6H5CHO-32e-+13H2O=7CO2+32H+
D.当b电极消耗等物质的量的K2Cr2O7时,a电极消耗的C6H5OH或C6H5CHO的物质的量之比为8:7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化锶可做荧光粉的原料,可通过金属锶与干燥纯净的氮气在460℃时反应制得。锶与镁、钙同主族,能与水、NH3反应。实验室设计以下装置来制备氮化锶(夹持装置略去)。
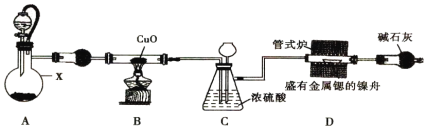
(1)实验简单步骤如下:①连接装置,检验装置的气密性②加装实验药品③点燃B处的酒精灯④加热D处的管式炉⑤打开A处的分液漏斗活塞。正确的实验操作步骤是________。
(2)仪器X的名称是__________;装置A是制取氨气的简易装置,仪器X中的固体是______________。
(3)装置B中的化学方程式是____________________。
(4)装置C的作用是平衡装置中的压强和____________________。
(5)装置D中的固体物质中含有氮化锶,已知氮化锶极易与水反应生成微溶于水的氢氧化锶,写出反应的化学方程式_________________________。
(6)锶的金属性比钠强,但锶与水反应的剧烈程度不如钠,原因足锶的熔点比钠高和____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把一块镁铝合金投入到1mol/L盐酸中,待合金完全溶解后(盐酸有剩余),再往溶液里加入1mol/LNaOH溶液,生成沉淀的物质的量随加入NaOH溶液体积的变化如图所示。下列说法中错误的是( )
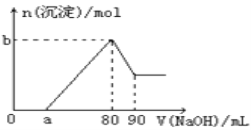
A. 盐酸的体积为80mL
B. a的取值范围为0<a<50
C. 当a值为30时,b值为0.01
D. n(Mg2+)<0.025mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com