
������������������ͭ�Ǻ�ɫ��ĩ���������ϡ�ijУһ��ѧʵ��С��ͨ��ʵ����̽��һ��ɫ��ĩ��Fc2O3��Cu2O����ߵĻ���̽���������£�
��������֪��Cu2O��һ�ּ������������ϡ��������Cu��CuSO4���ڿ����м�������CuO��
������裺����l����ɫ��ĩ��Fc2O3 ����2����ɫ��ĩ��Cu2O
����3����ɫ��ĩ��Fc2O3��Cu2O�Ļ����
���ʵ�飺ȡ������ĩ��������ϡ�����У���������Һ���ٵμ�KSCN��Һ��
��1��������1��������ʵ��������__ ��
��2�������� KSCN��Һ����Һ�����ɫ����֤��ԭ�����ĩ��һ����������������������Ϊ����˵��������____��Ͳ��������� .
��3���������ĩ��ȫ�ܽ�������ڣ��μ�KSCN��Һʱ��Һ�����ɫ����֤��ԭ�����ĩ��Fc2O3����Cu2O�Ļ�������������Ϊ____��д�����з�����������ԭ��Ӧ�����ӷ���ʽ ��̽�����죺��ʵ�������ȷ����ɫ��ĩΪFc2O3����Cu2O�Ļ���
��4��ʵ��С�����ü��ȷ��ⶨCu2O������������ȡag�����ĩ�ڿ����г�ּ��ȣ����������ٱ仯ʱ����������Ϊbg ����������Cu2O����������Ϊ
��
����������Cu2O����������Ϊ
��
��5��ʵ��С�������øú�ɫ��ĩ��ȡ�ϴ����ĵ�����CuSO4��5H2O�������������ϵ�֪����Һ��ͨ��������Һ������Զ�ʹCu2+��Fe3+��Fe2+�ֱ����ɳ�����pH���£�
|
�� �� |
Cu(OH)2 |
Fe(OH)2 |
Fe(OH)3 |
|
��ʼ����pH |
6.0 |
7.5 |
1.4 |
|
������ȫpH |
13 |
14 |
3.7 |
ʵ�����������Լ��ɹ�ѡ�� A����ˮ B��H2O2 C��NaOH D��Cu2��OH��2CO3
ʵ��С���������ʵ�鷽����
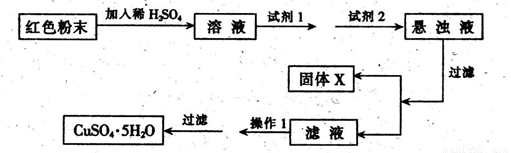
�Իش𣺢��Լ�1Ϊ___ _���Լ�2Ϊ ������ĸ����
�ڹ���X�Ļ�ѧʽΪ____���۲���IΪ_ ��
��1��������ȫ�ܽ⣬��Һ��Ϊ��ɫ����2�������� ��ɫ��ĩ����Fe2O3��Cu2O�Ļ�����������ϡ�����л���Cu���ɣ�Cu�ܽ�Fe3+��ԭΪFe2+���μ�KSCN�Լ�����Һ���ܲ����ɫ��
��3��10:9 Fe2O3+6H+=2Fe3++3H2O��Cu2O+2H+=Cu+Cu2++H2O��2Fe3++Cu=2Fe2++Cu2+
��4��[9(b−a) ]/a ��100%����5����B��D��Fe��OH��3ƒ ����Ũ�� ����ȴ�ᾧ
��������
�����������1������ɫ��ĩ��Fe2O3��Fe2O3�����ᷴӦ������������û�к�ɫ������μ�KSCN��Һ����Һ��Ϊ��ɫ����2����ɫ��ĩ����Fe2O3��Cu2O�Ļ�����������ϡ�����л���Cu���ɣ�Cu�ܽ�Fe3+��ԭΪFe2+���μ�KSCN�Լ�����Һ���ܲ����ɫ������˵������������3����ΪCu2O������������Cu��CuSO4����H2SO4�����ܽ�Cu�����Ի�����б�����Fe2O3���ڣ�ʹ�����ɵ�Fe3+�ܽ������Cu����Ӧ���й����ӷ���ʽΪFe2O3+6H+=2Fe3++3H2O��Cu2O+2H+=Cu+Cu2++H2O��2Fe3++Cu=2Fe2++Cu2+����Һ����죬�������������Ϊǡ����ȫ��Ӧ����������������ͭ�����ʵ�����ֵΪ1:1�������ȣ�10:9��
��4��Cu2O������2CuO �������ء�w
144 g 16 g
m��Cu2O�� ��b-a�� g
����m��Cu2O��=[144g��(b−a)g ]��16g =9��b-a��g��
�ʻ������Cu2O����������Ϊ[9(b−a) ]/a ��100%��
��5����ɫ��ĩΪFe2O3��Cu2O�Ļ����ɹ������̿�֪����������ϡ�����л���Cu���ɣ�Cu�ܽ�Fe3+��ԭΪFe2+�����õ���Һ����Fe2+�������Լ�1Ŀ����Fe2+��ΪFe3+�����������������ӣ����Լ�1Ӧѡ��B��H2O2�������Լ�2Ŀ���ǵ�����Һ��PHֵʹFe3+ת��ΪFe��OH��3������ȥ�����˵õ�����ͭ��Һ���������ƻ����������ӣ����Լ�2Ӧѡ��Cu2��OH��2CO3���õ��ij���xΪFe��OH��3������������Ũ������ȴ�ᾧ��
���㣺���⿼��ʵ�����Ƽ����ۣ��Լ����ʵ���ɵIJⶨ���ѶȽϴ�ע����������Ϣ���Ƕ�����֪ʶ���ۺϿ��飬��Ҫѧ��������ʵ�Ļ������ۺ����÷���������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
 ��������ͭ�ĵ��ʡ��Ͻ��仯���������������е�Ӧ�������㷺��
��������ͭ�ĵ��ʡ��Ͻ��仯���������������е�Ӧ�������㷺��
| ||
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| ���� | Cu��OH��2 | Fe��OH��2 | Fe��OH��3 |
| ��ʼ����pH | 6.0 | 7.5 | 1.4 |
| ������ȫpH | 13 | 14 | 3.7 |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ���� |
| ���� |

| 5 |
| 11 |
| 5 |
| 11 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ���� | Cu��OH��2 | Fe��OH��2 | Fe��OH��3 |
| ��ʼ����pH | 6.0 | 7.5 | 1.4 |
| ������ȫpH | 13 | 14 | 3.7 |

�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com