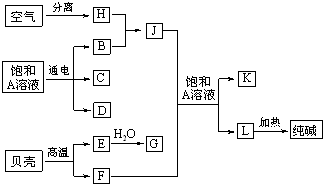
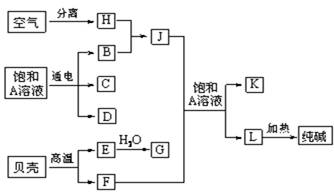
�Ժ�ˮ�г�������AΪԭ�Ͽ��Է�չ�ܶ��ֹ�ҵ����ͼ�а�������ѧ�α��н��ܵļ��ֻ�����ҵ���������������֮���ת����ϵ�ش��������⣺

��1��C��D��C��G��Ӧ��������ȡ��������C��G��Ӧ��ȡ������������Ч�ɷֵĻ�ѧʽΪ
Ca��ClO��2
Ca��ClO��2
��
��2��д�����A��Һ�Ļ�ѧ����ʽΪ
2NaOH+2H
2O
Cl
2��+H
2��+2NaOH
2NaOH+2H
2O
Cl
2��+H
2��+2NaOH
��
��3����ʹ��ҵ�ϳ�J��Ӧ��ƽ��������J�ķ����ƶ����ɲ�ȡ�Ĵ�ʩ��
BD
BD
������ĸ���ţ���
A�������¶�B������ѹǿC��ʹ�ô���D��Һ������
��4����F��Jͨ��A�ı�����Һ�е�˳��Ϊ
B
B
��
A����ͨ��F��ͨ��JB����ͨ��J��ͨ��F
C��ͬʱͨ��D��û���Ⱥ�˳��Ҫ��
��5��ͼ����ʾ��ҵ�Ʒ���õĴ����г�����NaCl���ʣ��������������Բⶨ��Ʒ��NaCl������������
��Ʒmg
��Һ
����
����ng
�ټ�������Ƿ�ϴ�Ӹɾ������õ����Լ��ǣ�
AgNO3��Һ
AgNO3��Һ
��
����Ʒ��NaCl��������������ѧ����ʽΪ��
��

 ���Ͱ�ͨ��ĩ���ϵ�д�
���Ͱ�ͨ��ĩ���ϵ�д�
 �Ժ�ˮ�г�������AΪԭ�Ͽ��Է�չ�ܶҵ��ͼ�а�������ѧ�α��н��ܵļ��ֻ�����ҵ����������ݸ�����֮���ת����ϵ�ش��������⣮
�Ժ�ˮ�г�������AΪԭ�Ͽ��Է�չ�ܶҵ��ͼ�а�������ѧ�α��н��ܵļ��ֻ�����ҵ����������ݸ�����֮���ת����ϵ�ش��������⣮