
【题目】铁及其化合物在日常生活、生产中应用广泛。
(1)某温度下,Ksp(FeS)=8.1×10-17,FeS饱和溶液中c(H+)与c(S2-)之间存在关系:
c2(H+)·c(S2-)=1.0×10-22,为了使溶液里c(Fe2+)达到1 mol·L-1,现将适量FeS投入其饱和溶液中,应调节溶液中的pH约为________(填字母)。
A.2 B.3 C.4 D.5
(2)氧化铁红颜料跟某些油料混合,可以制成防锈油漆。以黄铁矿为原料制硫酸产生的硫酸渣中含Fe2O3、SiO2、Al2O3、MgO等,用硫酸渣制备铁红(Fe2O3)的过程如下:
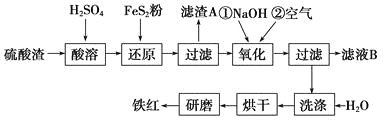
①酸溶过程中Fe2O3发生反应的离子方程式为_____________;“滤渣A”主要成分的化学式为_______________。
②还原过程中加入FeS2的目的是将溶液中的Fe3+还原为Fe2+,而本身被氧化为H2SO4,请完成该反应的离子方程式: FeS2+____Fe3++______===______Fe2++____SO42-+______
③氧化过程中,O2、NaOH与Fe2+反应的离子方程式为________________________。
④为了确保铁红的质量和纯度,氧化过程需要调节溶液的pH的范围是3.2~3.8。
沉淀物 | Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 |
开始沉淀pH | 2.7 | 3.8 | 7.6 | 9.4 |
完全沉淀pH | 3.2 | 5.2 | 9.7 | 12.4 |
如果pH过大,可能引起的后果是____________________(几种离子沉淀的pH见上表)。
⑤滤液B可以回收的物质有________(填序号)。
A.Na2SO4 B.Al2(SO4)3 C.Na2SiO3 D.MgSO4
【答案】B Fe2O3+6H+===2Fe3++3H2O SiO2 14 8H2O 15 2 16H+ 4Fe2++O2+2H2O+8OH-===4Fe(OH)3↓[或Fe2++2OH-===Fe(OH)2↓、4Fe(OH)2+O2+2H2O===4Fe(OH)3] Al3+、Mg2+形成沉淀,使制得的铁红不纯 ABD
【解析】
(1)根据硫化亚铁的溶度积常数和亚铁离子浓度计算硫离子浓度,再根据氢硫酸的电离平衡常数计算氢离子浓度,最后利用pH计算公式计算溶液的pH;
(2)硫酸渣中含Fe2O3、SiO2、Al2O3、MgO等,稀硫酸溶解主要除去不与酸反应的SiO2,加入FeS2将溶液中的Fe3+还原为Fe2+,再加氢氧化钠和空气,调节溶液的pH的范围是3.2~3.8主要是使三价铁沉淀,而二价镁,三价铝都不沉淀,最后洗涤、烘干、研磨使氢氧化铁分解生成氧化铁,从而得到铁红;
①氧化铁属于碱性氧化物,与酸反应生成盐和水;Fe2O3、Al2O3、MgO都和硫酸反应,二氧化硅不和酸反应;
②根据得失电子守恒和原子守恒来配平,FeS2中S元素的化合价从-1价升高到+6价,2个S原子转移14个电子,Fe3+转移1个电子,则二者的计量数之比为1:14,根据S守恒可知SO42-前面的化学计量数为2,根据氧守恒可知H20前面化学计量数为8,根据H守恒可知H+前化学计量数为16;
③NaOH与Fe2+反应生成的氢氧化亚铁易被氧化;
④根据几种离子沉淀的pH分析;
⑤因加入的是氢氧化钠来调节PH,所以滤液B中应是未沉淀离子的硫酸盐和硫酸钠。
(2)硫酸渣中含Fe2O3、SiO2、Al2O3、MgO等,稀硫酸溶解主要除去不与酸反应的SiO2,加入FeS2将溶液中的Fe3+还原为Fe2+,再加氢氧化钠和空气,调节溶液的pH的范围是3.23.8主要是使三价铁沉淀,而二价镁,三价铝都不沉淀,最后洗涤、烘干、研磨使氢氧化铁分解生成氧化铁,从而得到铁红;
①氧化铁与硫酸反应生成硫酸铁和水,方程式为:Fe2O3+3H2SO4═Fe2(SO4)3+3H2O;因二氧化硅不与硫酸反应,故“滤渣A”主要成份的化学式为SiO2.
故答案为:Fe2O3+3H2SO4═Fe2(SO4)3+3H2O;SiO2;
②FeS2中S元素的化合价从1价升高到+6价,2个S原子转移14个电子,Fe3+转移1个电子,则二者的计量数之比为1:14,根据S守恒可知SO42前面的化学计量数为2,根据氧守恒可知H2O前面化学计量数为8,根据H守恒可知H+前化学计量数为16,则反应的离子方程式为:1FeS2+14Fe3++8H2O═15Fe2++2SO42+16H+,
故答案为:14;8H2O;16H+;15;2;16H+;
③Fe2+与OH反应生成4Fe(OH)2,Fe(OH)2不稳定易被氧气氧化为Fe(OH)3,用化合价升价法配平方程式为4Fe2++O2+2H2O+8OH=4Fe(OH)3↓,
故答案为:4Fe2++O2+2H2O+8OH=4Fe(OH)3↓;
④根据几种离子沉淀的pH,如果pH过大,Al3+、Mg2+形成沉淀,使制得的铁红不纯;
故答案为:Al3+、Mg2+形成沉淀,使制得的铁红不纯;
⑤未沉淀的离子为Na+、Mg2+、Al3+,故滤液B可以回收的物质有:Na2SO4、Al2(SO4)3、MgSO4,
故选:ABD。


科目:高中化学 来源: 题型:
【题目】福酚美克是一种影响机体免疫功能的药物,可通过以下方法合成:
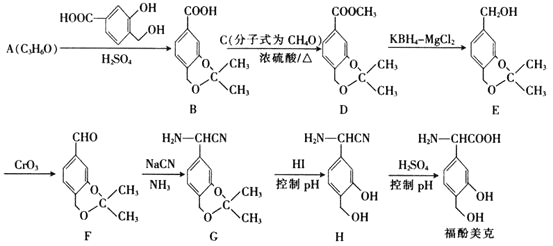
已知:
①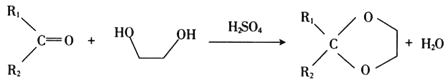 ;
;
②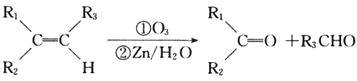 。
。
(1)C的名称为________,A的结构简式为________________。
(2)福酚美克中所含官能团有________________![]() 填名称
填名称![]() 。
。![]() 的反应类型为________。
的反应类型为________。
(3)已知![]() 的转化属于取代反应,则该反应的另一产物的结构简式为________。
的转化属于取代反应,则该反应的另一产物的结构简式为________。
(4)写出F发生银镜反应的化学方程式:________________________________。
(5)E的一种同分异构体Q满足下列条件,则Q的结构简式为________。
①Q的苯环上只有2个取代基,且Q的核磁共振氢谱图中有4组吸收峰
②Q能与![]() 溶液发生显色反应
溶液发生显色反应
③![]() 最多能与
最多能与![]() 发生反应
发生反应
(6)根据已有知识并结合题给信息,写出以![]() 为原料
为原料![]() 无机试剂任用
无机试剂任用![]() 制备
制备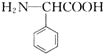 的合成路线流程图_________
的合成路线流程图_________![]() 无机试剂任选
无机试剂任选![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学电源在日常生活和高科技领域中都有广泛应用。下列说法不正确的是( )
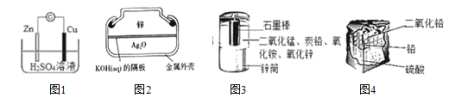
A.图 1 锌铜原电池中,Zn2+向 Cu 电极方向移动,Cu 电极附近溶液中 H+浓度增加
B.图 2 纽扣式银锌电池中,正极的电极反应式为 Ag2O+2e -+H2O = 2Ag+2OH-
C.图 3 锌锰干电池中,锌筒作负极,发生氧化反应,锌筒会变薄
D.图 4 铅蓄电池中,使用一段时间后,电解质溶液的酸性减弱,导电能力下降
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】烟气中![]() 和
和![]() 的转化和综合利用既有利于节约资源,又有利于保护环境。
的转化和综合利用既有利于节约资源,又有利于保护环境。
![]() 采用“联合脱硫脱氮技术”处理烟气
采用“联合脱硫脱氮技术”处理烟气![]() 含
含![]() 、
、![]() 、
、![]() 可获得含
可获得含![]() 、
、![]() 、
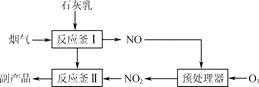
、![]() 的副产品,工业流程如图1所示。
的副产品,工业流程如图1所示。
![]() 反应釜 Ⅰ中
反应釜 Ⅰ中![]() 与足量石灰乳反应的化学方程式为________。
与足量石灰乳反应的化学方程式为________。
![]() 下列措施能提高各反应釜中气体去除率的有 ________
下列措施能提高各反应釜中气体去除率的有 ________![]() 填字母
填字母![]() 。
。
A. 加快通入气体的速率
B. 采用气、液逆流的方式吸收气体
C. 吸收过程中定期补充吸收液
![]() 反应釜 Ⅱ中
反应釜 Ⅱ中![]() 转化为
转化为![]() 反应的化学方程式为________。
反应的化学方程式为________。
![]() 预处理器中发生的主要反应为
预处理器中发生的主要反应为![]() ,
,![]() 。室温下,固定进入预处理器的NO的物质的量,改变加入
。室温下,固定进入预处理器的NO的物质的量,改变加入![]() 的物质的量,反应一段时间后体系中
的物质的量,反应一段时间后体系中![]() 、
、![]() 随反应前
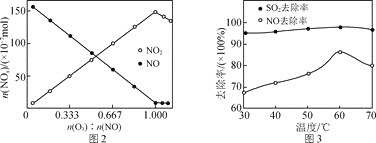
随反应前![]() 的变化如图2所示。当
的变化如图2所示。当![]() 时,反应后
时,反应后![]() 的物质的量减少,其原因是__________________________________。
的物质的量减少,其原因是__________________________________。
![]() 研究表明:
研究表明:![]() 酸性复合吸收剂可同时有效脱硫、脱硝。图3所示为复合吸收剂组成一定时,温度对脱硫、脱硝的影响。
酸性复合吸收剂可同时有效脱硫、脱硝。图3所示为复合吸收剂组成一定时,温度对脱硫、脱硝的影响。
![]() 温度高于
温度高于![]() 后,NO去除率下降的原因为________。
后,NO去除率下降的原因为________。
![]() 写出废气中的
写出废气中的![]() 与
与![]() 反应的离子方程式:________。
反应的离子方程式:________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能证明乙烯分子里含有一个碳碳双键的事实是( )
A.乙烯分子里碳氢原子个数之比为1∶2
B.乙烯完全燃烧生成的CO2和H2O的物质的量相等
C.乙烯能使酸性KMnO4溶液褪色
D.乙烯易与溴水发生加成反应,且1mol乙烯完全加成消耗1mol溴单质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】当电池工作时,下列说法错误的

A. 甲池中N极的电极反应式为:O2+4e-+4H+=2H2O
B. 当N极消耗5.6L(标准状况下)O2时,铁极增重32g
C. 电子的流动方向为M→Fe→CuSO4溶液→Cu→N
D. M极上发生的是氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业制得的氮化铝(AlN)产品中常含有少量Al4C3、Al2O3、C等杂质。某同学设计如下实验分别测定氮化铝(AlN)样品中AlN和Al4C3的质量分数(忽略NH3在强碱性溶液中的溶解)。
(1)实验原理:
①Al4C3与硫酸反应可生成CH4;
②AIN溶于强酸产生铵盐,溶于强碱生成氨气,请写出AlN与NaOH溶液反应的化学方程式:__________________________________________________________________
(2)实验装置(如图所示,量气管为碱式滴定管改装)
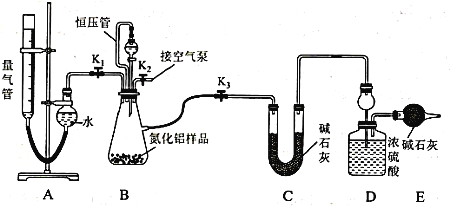
连好装置后,首先应进行的操作是_____________________________________ 。
(3)实验过程:称得装置D的初始质量为y g;称取x g AlN样品置于装置B锥形瓶中,各装置中加入相应药品,重新连好装置;读取量气管的初始读数为a mL(量气装置左右液面相平)。
①欲首先测量Al4C3质量分数的有关数据,对K1、K2、K3三个活塞的操作是关闭活塞_______,打开活塞______。
②若无恒压管,对所测气体体积的影响是_______(填“偏大”、“偏小”或“无影响”)。
③量气管中液面不再发生变化,说明反应已经结束。读取读数之前,应对量气管进行的操作为 ______________________________________ ;若量气管中的液面高于右侧球形容器中的液面,所测气体的体积_________(填“偏大”、“偏小”或“无影响”)。
④记录滴定管的读数为b mL(已知:该实验条件下的气体摩尔体积为Vm L· mol-1),则Al4C3的质量分数为___________(用可能含a、b、x、y、Vm的代数式表示)。
⑤测量AlN质量分数的数据:首先关闭活塞K1,打开活塞K3,通过分液漏斗加入过量NaOH溶液,与装置B瓶内物质充分反应;反应完成后,___________________________(填该步应进行的操作),最后称得装置D的质量为z g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苹果醋是一种由苹果汁发酵而成的酸性饮品,具有解毒、降脂等药效。苹果酸是一种常见的有机酸,其结构简式为![]() 。
。
(1)苹果酸的分子式为___。
(2)1mol苹果酸与足量金属钠反应,能生成标准状况下的氢气___L。
(3)苹果酸可能发生的反应是___(填序号)。
A.与NaOH溶液反应
B.与石蕊试液作用
C.与乙酸在一定条件下发生酯化反应
D.与乙醇在一定条件下发生酯化反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com