



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 Ϊ������ˮ����İ�ɫ���壬
Ϊ������ˮ����İ�ɫ���壬 Ϊ������ˮ�����Ǻ�ɫ���塣
Ϊ������ˮ�����Ǻ�ɫ���塣 ��
��  ��Һ���������ɫ������ȫת��Ϊ��ɫ���塣
��Һ���������ɫ������ȫת��Ϊ��ɫ���塣 | ��ѧʽ | �� AgCl | �� AgBr | �� Ag2S | �� Ag2CrO4 |
| Ksp | 2.0��10��10 | 5.4��10��13 | 2.0��10��48 | 2.0��10��12 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��c(H+)��c(OH-)������ | B��c(H+)���� | C��c(OH-)��С | D��c(H+)��С |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��Va>Vbʱ��c(CH3COOH) + c(CH3COO-)�� c(K+�� |
| B��Va=Vbʱ��c(CH3COOH) + c(H+) = c(OH-�� |
| C��Va<Vbʱ��c(CH3COO-) �� c(K+���� c(OH-����(H+) |
| D��Va��Vb�����ʱ��c(K+��+ c(H+) ��c(OH-��+ c(CH3COO-) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��4����Һ��PH�Ĵ�С�Ǣۣ��ڣ��ܣ��� |
| B������4����Һϡ����ͬ�ı�����PH�仯�����Ǣ� |
| C�����ֱ����25 mL0.1 mol��L��1�����PH�����Ǣ� |
| D����4����Һ��PH��Ϊ9�������ʵ���Ũ�ȴ�С˳���Ǣۣ��٣��ڣ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
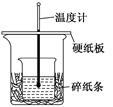
| A����ͼ������ʵ�������û��������ʧ |
| B��������60 mL 0.50 mol/L�����50 mL 0.55 mol/L��NaOH��Һ���з�Ӧ����������˵����Ӧ����� |
| C��ͼ��ʵ��װ��ȱ�ٻ��β�������� |
| D���ձ���������ֽ���������ǹ̶�С�ձ� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com