
【题目】已知AgCl的溶解平衡:AgCl(s)![]() Ag+(aq)+Cl-(aq),下列说法不正确的是( )
Ag+(aq)+Cl-(aq),下列说法不正确的是( )
A.除去溶液中Ag+加盐酸比硫酸盐好
B.加入H2O,溶液平衡不移动
C.用NaCl溶液代替蒸馏水洗涤AgCl,可以减少沉淀损失
D.反应2AgCl(s)+Na2S![]() Ag2S(s)+2NaCl说明溶解度:AgCl>Ag2S
Ag2S(s)+2NaCl说明溶解度:AgCl>Ag2S
 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案科目:高中化学 来源: 题型:
【题目】下表中对应关系正确的是( )
A | CH3CH3+Cl2 CH2=CH2+HCl→CH3CH2Cl | 均为取代反应 |
B | 由油脂得到甘油;由卤代烃制醇 | 均发生了水解反应 |
C | Cl2+2Br→2Cl+Br2;Zn+Cu2+→Zn2++Cu | 均为单质被还原的置换反应 |
D | 2Na2O2+2H2O→4NaOH+O2↑; 2F2+2H2O→4HF+ O2 | 均为水作还原剂的氧化还原反应 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如下图所示,装置Ⅰ为甲烷燃料电池(电解质溶液为KOH溶液),通过装置Ⅱ实现铁棒上镀铜。
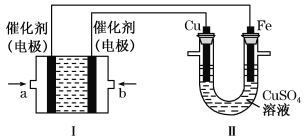
①a处应通入______(填“CH4”或“O2”),a处电极上发生的电极反应式是______________;
②电镀结束后,装置Ⅰ中溶液的pH _________ (填写“变大”“变小”或“不变”,下同),装置Ⅱ中Cu2+的物质的量浓度____________________;
③电镀结束后,装置Ⅰ溶液中的阴离子除了OH-以外还含有________________ ;
④在此过程中若完全反应,装置Ⅱ中阴极质量变化6.4 g,则装置Ⅰ中理论上消耗甲烷__________L(标准状况下)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚酯纤维(涤纶)是重要的衣服面料,以下是一种合成路线(部分反应条件略去)。
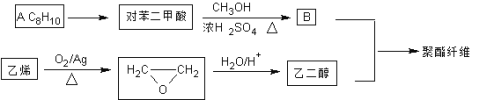
已知:酯与醇(或酚)可发生如下酯交换反应:![]()
(1)C8H10的系统命名为______________;它的同系物分子通式为________________。
(2)在其它催化剂作用下,乙烯与氧气反应的产物是____________(写结构简式)。
(3)若B过量,生成的聚酯纤维可表示为:![]() ,若乙二醇过量,则生成的聚酯纤维可表示为_______________________________。
,若乙二醇过量,则生成的聚酯纤维可表示为_______________________________。
(4)将废涤纶和甲醇在一定条件下反应,对聚合物进行降解,生成物是______________(填名称)。
(5)对苯二甲酸有多种芳香族同分异构体,写出一种满足以下条件的有机物的结构简式________。
①遇氯化铁溶液显紫色;②能发生银镜反应;③有三种不同化学环境的H原子。
(6)聚合物PC也由酯交换反应合成,其结构可表示为:![]() ,合成PC的2种单体中:醇(或酚)的结构简式为______________________,酯的名称为
,合成PC的2种单体中:醇(或酚)的结构简式为______________________,酯的名称为
_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工厂的电镀污泥中含有铜、铁等金属化合物。为实现资源的回收利用并有效防止环境污染,设计如下工艺流程:
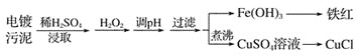
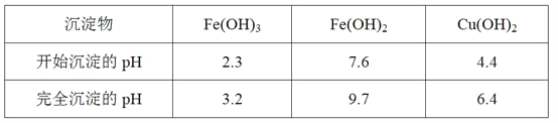
(1)酸浸后加入H2O2的目的是__,调pH的最适宜范围为__。
(2)调pH过程中加入的试剂最好是__。
A.NaOH B.CuO C.NH3·H2O D.Cu2(OH)2CO3
(3)煮沸CuSO4溶液的原因是__。向CuSO4溶液中加入一定量的NaCl、Na2SO3,可以生成白色的CuCl沉淀,写出该反应的化学方程式__。
(4)过滤后的沉淀表面通常附着有一些杂质离子,为得到纯净产物,需要进行洗涤,确定沉淀洗涤干净的操作及现象是__。
(5)称取所制备的CuCl样品0.2500g置于一定量的0.5mol﹒L-1FeCl3溶液中,待样品完全溶解后,加水20mL,用0.1000mol﹒L-1的Ce(SO4)2溶液滴定,到达终点时消耗Ce(SO4)2溶液25.00mL。有关的化学反应为Fe3++CuCl=Fe2++Cu2++Cl-,Ce4++Fe2+=Fe3++Ce3+。计算该CuCl样品的质量分数___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述相符的是

A.图I表示某吸热反应分别在有、无催化剂的情况下反应过程中的能量变化
B.图Ⅱ表示常温下,0.1000mol/LNaOH溶液滴定20.00mL、0.0100mol/LHCl溶液所得到的滴定曲线
C.图Ⅲ表示一定质量的冰醋酸加水稀释过程中,醋酸溶液电离程度:c < a < b
D.图Ⅳ表示反应4CO(g)+2NO2(g) ![]() N2(g)+4CO2(g),在其他条件不变的情况下改变起始物CO的物质的量,平衡时N2的体积分数变化情况,由图可知NO2的转化率c > b > a
N2(g)+4CO2(g),在其他条件不变的情况下改变起始物CO的物质的量,平衡时N2的体积分数变化情况,由图可知NO2的转化率c > b > a
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向100mL0.1mol/L的NaAlO2溶液中加入一定量的稀HNO3,将所得溶液加热、蒸干并灼烧直至质量不再变化,此时固体的质量为
A.1.09gB.1.20 gC.1.36gD.1.63g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,取浓度均为0.1 mol·L-1的醋酸溶液和氨水溶液各20 mL,分别用0.1 mol·L-1NaOH溶液、0.1 mol·L-1盐酸进行中和滴定,滴定过程中pH随滴加溶液的体积变化关系如右图所示。下列说法正确的是
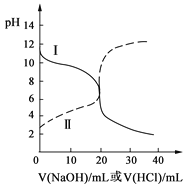
A.曲线Ⅰ:滴加溶液到10 mL时:c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
B.曲线Ⅰ:滴加溶液到20 mL时:c(Cl-)>c(NH4+)>c(H+)>c(OH-)
C.曲线Ⅱ:滴加溶液在10 mL~20 mL之间存在:c(NH4+)=c(Cl-)>c(OH-)=c(H+)
D.曲线Ⅱ:滴加溶液到10 mL时:c(CH3COO-)-c(CH3COOH)=2[c(H+)-c(OH-)]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮的氧化物(NOx)是大气污染物之一,工业上在一定温度和催化剂条件下用NH3将NOx还原生成N2,某同学在实验室中对NH3与NOx反应进行了探究。回答下列问题:
(1)氨气的制备

①氨气的发生装置可以选择上图中的________,反应的化学方程式为______________。
②预收集一瓶干燥的氨气,选择上图中的装置,其连接顺序为:发生装置→______(按气流方向,用小写字母表示)。
(2)氨气与二氧化氮的反应将上述收集到的NH3充入注射器X中,硬质玻璃管Y中加入少量催化剂,充入NO2(两端用夹子K1、K2夹好)。在一定温度下按图示装置进行实验。

操作步骤 | 实验现象 | 解释原因 |
打开K1,推动注射器活塞,使X中的气体缓慢通入Y管中 | ①Y管中_____________ | ②反应的化学方程式 ____________ |
将注射器活塞退回原处并固定,待装置恢复到室温 | Y管中有少量水珠 | 生成的气态水凝集 |
打开K2 | ③_______________ | ④______________ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com