
| A、溶液中肯定不存在的离子只有Fe3+ |
| B、Fe3+和Cu2+均能被铁粉还原 |
| C、Fe2+与SCN-能形成红色的物质 |
| D、滤渣中肯定不含有铜 |


科目:高中化学 来源: 题型:
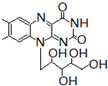 核黄素又称为维生素B2,可促进发育和细胞再生,有利于增进视力,减轻眼睛疲劳.核黄素分子的结构如图所示:已知:
核黄素又称为维生素B2,可促进发育和细胞再生,有利于增进视力,减轻眼睛疲劳.核黄素分子的结构如图所示:已知: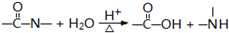
| A、该化合物的分子式为C17H22N4O6 |
| B、酸性条件下加热水解,有CO2生成 |
| C、该分子中有3个手性碳原子(与4个不同基团连接的碳原子叫手性碳原子) |
| D、能发生酯化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ① | ② | ③ | ④ | |
| 溶液 | 氨水 | 氢氧化钠溶液 | 醋酸 | 盐酸 |
| pH | 11 | 11 | 3 | 3 |
| A、在①、②中分别加入适量的氯化铵晶体后,①的pH减小,②的pH不变 |
| B、温度下降10℃,四种溶液的pH均不变 |
| C、分别加水稀释10倍,四种溶液的pH:①>②>③>④ |
| D、将①、④两种溶液等体积混合,所得溶液中:c(NH4+)>c(Cl-)>c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
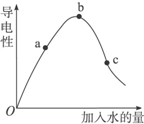 一定温度下,冰醋酸加水稀释过程中溶液的导电能力如图所示.请完成下列问题:
一定温度下,冰醋酸加水稀释过程中溶液的导电能力如图所示.请完成下列问题:| ①H2SO4溶液 HSO4-?H++SO42- | ②NaHSO4溶液 HSO4-?H++SO42- | ③醋酸溶液 CH3COOH?H++CH3COO- | ④盐酸 HCl=H++Cl- |
| 10% | 29% | 1.33% | 100% |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向氯水中加入碳酸钙粉末,能提高溶液中HClO的浓度 |
| B、氯水中含有7种微粒,其可以与AgNO3、FeBr2等多种物质反应 |
| C、蓝色石蕊试纸放入氯水中先变红后褪色 |
| D、氯水可以导电,说明氯气是电解质 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com