
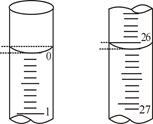
| �ζ����� | ������������/mL | 0.1000 mol/LNaOH��Һ�����/mL | ||
| �ζ�ǰ�̶� | �ζ���̶� | ��Һ���/mL | ||
| ��һ�� | 25.00 | 2.00 | 28.15 | 26.15 |
| �ڶ��� | 25.00 | 1.50 | 29.50 | 28.00 |
| ������ | 25.00 | 0.20 | 26.55 | 26.35 |


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��pH��7����Һ | B��c(H+)��c(OH��) ����Һ |
| C��pH��7����Һ | D��c(H+)��c(OH��) ����Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A����x��y����a+b��14����pH��7 | B����10x��y����a+b��13����pH��7 |
| C����ax��by����a+b��13����pH��7 | D����x��10y����a+b��14����pH��7 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��

A������Һ��pH= 3 3 | |
B����HA�������c(H+)ԼΪˮ�������c(H+)��108�� | C��Na2A��Һ�Լ��� |
D�������¶ȣ���Һ��pH���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A����ɫ | B����ɫ | C����ɫ | D����ɫ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�ʵ����
| A����ʽ�ζ���δ�ñ�������ϴ��ֱ��ע������� |
| B���ζ�ǰʢ��NaOH��Һ����ƿ������ˮϴ����û�и��� |
| C����ʽ�ζ����ڵζ�ǰ�����ݣ��ζ���������ʧ |
| D����ȡ�������ʱ����ʼ���Ӷ������ζ�����ʱ���Ӷ��� |

| �ζ� ���� | ����NaOH��Һ�����/mL | 0��100 mol/L��������/mL | ||
| �ζ�ǰ�̶� | �ζ���̶� | ��Һ���/mL | ||
| ��һ�� | 25��00 | 0��20 | 20��22 | |
| �ڶ��� | 25��00 | 0��56 | 24��54 | |
| ������ | 25��00 | 0��42 | 20��40 | |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A����������Һ��ˮϡ��1000����pH����3 |
| B����NaHCO3��Һ�У�c(Na+)=c(HCO3��)+c(H2CO3) |
| C��pH=8��Ba(OH)2��Һ��pH=8�İ�ˮ�У���ˮ�����c(OH��)��Ϊ1��10��8mo1��L��1 |
| D��pH=13��NaOH��Һ��pH=1�������Ϻ�һ����c(H+)=c(OH��) |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com