
【题目】一同学欲从量筒中取出部分液体,他先俯视凹液面的最低处,读数为50mL,倒出液体后,他又仰视凹液面的最低处,读数为10mL他实际倒出液体的体积为( )
A. 40mL B. 大于40mL C. 小于40mL D. 不一定
科目:高中化学 来源: 题型:
【题目】由A、B、C、D四种金属按下表中装置进行实验。
装置 |
|
|
|
现象 | 二价金属A不断溶解 | C的质量增加 | A上有气体产生 |
根据实验现象回答下列问题:
(1)装置甲中负极的电极反应式是__。
(2)装置乙中正极的电极反应式是__。
(3)装置丙中溶液的pH__(填“变大”、“变小”或“不变”)。
(4)四种金属活泼性由强到弱的顺序是__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如果n为第ⅠA族中X元素的原子序数,则原子序数为(n+2)的Y元素可能位于( )
①ⅡA ②ⅢA ③ⅣA ④ⅠB ⑤ⅡB ⑥ⅢB.
A.①④
B.②⑥
C.③⑤
D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】埋在地下的输油铁管道,在下列情况下,被腐蚀速率最慢的是
A.在含铁元素较多的酸性土壤 B.在潮湿疏松透气的土壤
C.在干燥致密不透气的土壤 D.在含碳颗粒较多,潮湿透气的中性土壤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】医用氯化钙可用于生产补钙、抗过敏和消炎等,以工业碳酸钙(含少量Na+、Al3+、Fe3+等杂质)生产医药级二水合氯化钙(CaCl2、2H2O的质量分数为97.0%~103.0%)的主要流程如下:
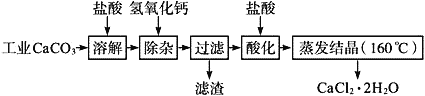
已知:
氢氧化物 | Fe(OH)3 | Al(OH)3 | Al(OH)3 | |
开始沉淀时的pH | 2.3 | 4.0 | 开始溶解时的pH | 7.8 |
完全沉淀时的pH | 3.7 | 5.2 | 完全溶解时的pH | 10.8 |
(1)CaCO3与盐酸反应的离子方程式___________。
(2)“除杂”操作是加入氢氧化钙,调节溶液的pH范围为________,目的是除去溶液中的少量Al3+、Fe2+。
(3)过滤时需用的比玻璃器有__________。
(4)“酸化”操作是加入盐酸,调节溶液的pH约为4.0,其目的有:①防止氢氧化钙吸收空气中的二氧化碳;②防止Ca2+在蒸发时水解;③_______。
(5)蒸发结晶要保持在160℃的原因是__________。
(6)测定样品中Cl-含量的方法是:称取0.750 0 gCaCl2·2H2O样品,溶解,在250 mL容量瓶中定容;量取25.00 mL待测溶液于锥形瓶中;用0.050 00 mol/L AgNO3溶液滴定至终点(用K2Cr2O2),消耗AgNO3溶液体积的平均值为20.39 mL。
①上述测定过程中需用溶液润洗的仪器有________。
②计算上述样品中CaCl2·2H2O的质量分数为_______。(保留四位有效数字)
③若用上述方法测定的样品中CaCl2·2H2O的质量分数偏高(测定过程中产生的误差可忽略),其可能原因有________;__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组为了制取并探究氨气性质,按下列装置(部分夹持装置已略去)进行实验。[制取氨气的反应原理:2NH4Cl+Ca(OH)2=CaCl2+2NH3↑+2H2O]

【实验探究】
(1)利用上述原理,实验室制取氨气应选用下图中 发生装置进行实验。
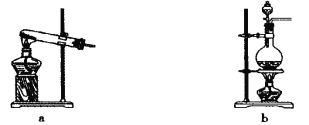
(2)B装置中的干燥剂可选用 (填“碱石灰”或“浓硫酸”)。
(3)用5.35 g NH4Cl固体与足量Ca(OH)2反应,最多可制得标准状况下氨气的体积为 L。(NH4Cl的摩尔质量为53.5 g·mol-1)
(4)气体通过C、D装置时,试纸颜色会发生变化的是 (填“C”或“D”)。
(5)当实验进行一段时间后,挤压E装置中的胶头滴管,滴入1~2滴浓盐酸,可观察到的现象是 。
(6)F装置中倒置漏斗的作用 。
【拓展应用】
(7)某同学用氨气和滴加酚酞的水做喷泉实验,根据烧瓶内产生红色喷泉的现象,说明氨气具有 性质(填序号)。
a.还原性 b.极易溶于水 c.与水反应生成碱性物质
(8)氨气的用途很广。如可用氨气处理二氧化氮: 8NH3 + 6NO2 =7N2 + 12H2O
该反应中氨气体现 (填“氧化性”或“还原性”)。
请你列举出氨气的另一种用途 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列除杂质的操作中不正确的是
A. 铁粉中混有铝粉:加入过量烧碱溶液充分反应后过滤
B. FeCl2溶液中混有FeCl3加入过量铁粉充分反应后过滤
C. Na2CO3固体中混有少量NaHCO3:加入适量NaOH溶液
D. AI(OH)3中混有Mg(OH)2:加入足量烧碱溶液后过滤,向滤液中通入过量CO2后过滤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E为原子序数依次增大的短周期元素,已知A、B、E 三种原子最外层共有10个电子,且这3种元素的最高价氧化物的水化物两两皆能发生反应生成盐和水,C元素的最外层电子数比次外层电子数少4,D元素原子次外层电子数比最外层电子数多3。
(1)写出对应的元素符号:C________,D_______
(2)用电子式表示A与E两元素形成化合物的过程:___________________________ ;
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com