
短周期元素X、Y、Z、W的原子序数依次增大,X的原子在元素周期表中原子半径最小,Y原子基态时最外层电子数是次外层的3倍,ZX2是一种储氢材料,W与Y属于同一主族。下列叙述正确的是
| A.原子半径:rW >rZ>rY |
| B.元素Y的简单气态氢化物的热稳定性比W的弱 |
| C.化合物从X2Y、ZY,、WY3中化学键的类型相同 |
| D.化合物ZWY4·7X2Y的水溶液显酸性 |
 补充习题江苏系列答案
补充习题江苏系列答案 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案科目:高中化学 来源: 题型:单选题
下列有关化学用语使用正确的是
A.NH4Br的电子式: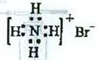 |
B.S2-的结构示意图: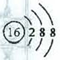 |
| C.乙酸的分子式:CH3COOH |
D.原子核内有18个中子的氯原子: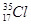 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
氧元素是地壳中含量最多的元素。下列说法正确的是
| A.16O2与18O3互为同位素 |
| B.氧元素与其它短周期非金属元素形成的氧化物均属于酸性氧化物 |
| C.O2变成O3以及16O变成18O的变化均属于化学变化 |
| D.氧与钠形成的稳定化合物中,阴、阳离子个数比均为1∶2 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
短周期元素X、Y、Z中,其中X、Y位于同一主族,Y、Z位于同一周期。X原子的最外层电子数是其电子层数的3倍,Z原子的核外电子数比Y原子少1个,下列比较正确的是
| A.原子半径:X>Y | B.元素非金属性:X>Y |
| C.气态氢化物的稳定性:Z>Y | D.最高价氧化物水化物的酸性:Z>Y |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
有A、B、C、D、E五种短周期元素,A是地壳中含量最多的元素,B元素有3种同位素B1、B2、B3,B3原子的质量数是B1的3倍,C是非金属性最强的元素,D和C可以形成DC型离子化合物,且离子的电子层结构相同,E元素原子的最外层电子数比内层电子总数少6个。下列说法正确的是 ( )
A.离子半径:D+>C—
B.EA2是光导纤维的主要成分
C.A和B可以形成原子个数比1:1的化合物
D.以上元素中形成的最高价氧化物对应的水化物酸性最强的是C
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
元素周期表和元素周期律可以指导人们进行规律性的推测和判断。下列说法不合理的是
| A.若X+和Y2-的核外电子层结构相同,则原子序数:X>Y |
| B.由水溶液的酸性:HCl>H2S,可推断出元素的非金属性:Cl>S |
| C.硅、锗都位于金属与非金属的交界处,都可以做半导体材料 |
| D.Cs和Ba分别位于第六周期IA和ⅡA族,碱性:CsOH >Ba(OH)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下图是部分短周期主族元素原子半径与原子序数的关系图。则下列说法正确的是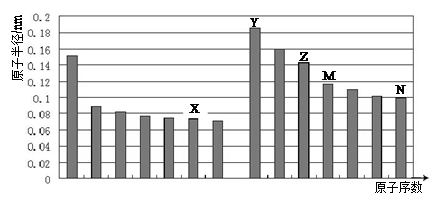
| A.Z、N两种元素的离子半径相比,前者较大 |
| B.X、N两种元素的气态氢化物的稳定性相比,前者较弱 |
| C.由X与M两种元素组成的化合物不能与任何酸反应,但能与强碱反应 |
| D.Z的氧化物能分别溶解于Y的氢氧化物和N的氢化物的水溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
短周期元素Q、R、T、W在元素周期表中的位置如右图所示,其中T所处的周期序数与主族序数相等,下列推断正确的是
| | Q | R | |
| T | | | W |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
X、Y、Z是原子序数依次递增的短周期元素,3种元素的原子核外电子数之和与Ca2+的核外电子数相等,X、Z分别得到一个电子后均形成稀有气体原子的稳定电子层结构。下列说法正确的是
| A.原子半径:Z>Y>X |
| B.Z与X形成化合物的沸点高于Z的同族元素与X形成化合物的沸点 |
| C.Na2Y2与水发生氧化还原反应时,Na2Y2只作氧化剂 |
| D.CaX2、CaY2和CaZ2等3种化合物中,阳离子与阴离子个数比均为1︰2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com