
( 9分)A、B都是短周期元素,原子最外层电子排布式分别为(n+1)sx、nsx+1npx+3。A与B可形成化合物D。D溶于水时有气体逸出,该气体能使带火星的木条复燃。请回答下列问题:
(1)比较电离能:I1(A)________I1(B)(填“>”或“<”,下同),比较电负性:A________B。
(2)通常A元素的化合价是________,对A元素呈现这种价态进行解释:
①用原子结构的观点进行解释: _______________________________________。
②用电离能的观点进行解释: ___________________________________________。
③写出D跟水反应的离子方程式:_______________________________________。
( 9分 ) (1)①< (1分) ②< (1分) (2)+1价(1分)
①钠原子失去一个电子后形成1s22s22p6式的原子轨道全充满的+1价阳离子。该离子结构体系能量低,极难再失去电子(2分)
②Na原子的第一电离能相对较小,第二电离能比第一电离能大很多倍。通常Na原子只能失去一个电子 (2分)③2Na2O2+2H2O===4Na++4OH-+O2↑(2分)
【解析】
试题分析:根据构造原理可知,s轨道最多容纳2个电子,所以x=1。D溶于水时有气体逸出,该气体能使带火星的木条复燃,所以D是过氧化钠,则n=2,所以A是钠,B是氧元素。
(1)非金属性越强,第一电离能越大,所以钠的第一电离能小于氧元素的。同样电负性也是钠的小于氧元素的。
(2)钠最外层电子数是1个,通常显+1价。
①由于钠原子失去1个电子后形成1s22s22p6式的原子轨道全充满的+1价阳离子。该离子结构体系能量低,极难再失去电子,所以通常显+1价。
②由于Na原子的第一电离能相对较小,而第二电离能比第一电离能大很多倍。通常Na原子只能失去一个电子,因此显+1价。
③过氧化钠溶于水生成氧气和氢氧化钠,反应的离子方程式是2Na2O2+2H2O===4Na++4OH-+O2↑。
考点:考查核外电子的排布、电离能及电负性的有关判断
点评:在判断原子核外电子的排布时,应该利用构造原理进行分析。另外本题的关键还在于能使带火星的木条复燃的气体是氧气,继而逐一分析即可。


 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案科目:高中化学 来源:2012-2013学年福建省厦门六中高二上学期期中考试化学试卷(带解析) 题型:填空题
( 9分)A、B都是短周期元素,原子最外层电子排布式分别为(n+1)sx、nsx+1npx+3。A与B可形成化合物D。D溶于水时有气体逸出,该气体能使带火星的木条复燃。请回答下列问题:
(1)比较电离能:I1(A)________I1(B)(填“>”或“<”,下同),比较电负性:A________B。
(2)通常A元素的化合价是________,对A元素呈现这种价态进行解释:
①用原子结构的观点进行解释: _______________________________________。
②用电离能的观点进行解释: ___________________________________________。
③写出D跟水反应的离子方程式:_______________________________________。
查看答案和解析>>
科目:高中化学 来源:2012年人教版高中化学必修一第四章 非金属及其化合物练习卷(解析版) 题型:填空题
(9分)A、B、C、D、E可能是NH4Cl、Ba(OH)2、KCl、K2SO4、(NH4)2SO4无色溶液中的一种,将它们两两混合时产生的现象是:
①A和B混合后产生白色沉淀,加热后无明显现象.
②B和C混合也产生白色沉淀,加热后有气体产生,气体使湿润的红色石蕊试纸变蓝.
③B和E混合后无沉淀,但加热后也产生使湿润的红色石蕊试纸变蓝的气体.
④D和任何一种溶液混合后,都无明显变化.根据上述现象,回答:
(1)A:________,B:________,C:________,D:___________,E:________(用化学式表示).
(2)写出有关反应的离子方程式:
A+B:________________________________________________________;
B+C:________________________________________________________;
B+E:_________________________________________________________.
查看答案和解析>>
科目:高中化学 来源:2010-2011学年湖北省武汉市江汉区黄冈市高三上学期期末考试(理综)化学部分 题型:填空题
(14分)物质A~E都是由下表中离子组成的,常温下各物质从1mL稀释到1000mL,pH的变化如图甲所示,其中A与D反应得到E。 请回答:
|
阳离子 |
NH4+、H+、Na+ |
|
阴离子 |
OH-、CH3COO-、Cl- |
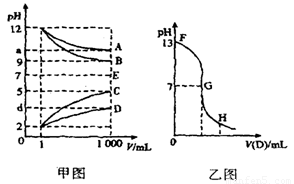
(1)根据pH的变化关系图甲,写出物质的化学式:B: ,D: 。
(2)图甲a>9的理由是
(3)另取浓度为C1的B溶液25mL,向其中逐滴滴加0.2mol/L的D溶液,滴定过程中溶液pH的变化曲线如乙图所示。
①C1为 ;
②G点溶液呈中性则滴加入D溶液的体积V 12.5mL(填>,<或=)
③常温下B、C溶液的pH分别是a、b且a+b=13则将B、C混和恰好完全反应时所消耗B、C溶液的体积比VB:VC=
查看答案和解析>>
科目:高中化学 来源: 题型:
(9分) A、B、C、D、E五种短周期元素,原子序数依次增大,A、E同主族,A元素的原子半径最小,B元素原子的最外层电子数是内层电子数的2倍,C元素原子的电子层数为n,最外层电子数为2n+l,A、B、C、E每种元素都能与D元素组成两种或两种以上的常见化合物。 回答下列问题:
(1)写出下列各元素的名称:C___________ E____________
(2)已知:BA3DA(g)+A2D(g)=BD2(g)+3A2(g) △H= +49.0kJ/mol
BA3DA(g)+1/2D2(g)=BD2(g)+2A2(g) △H = 一192.9kJ/mol
试写出:气态BA3DA完全燃烧生成气态A2D的热化学方程式(用推出的元素符号写)
(3)![]() 点燃不纯的A2气体可能会发生爆炸,为了防止意外,可连接一个安全装置。下图的装置能起到此作用的是___________。
点燃不纯的A2气体可能会发生爆炸,为了防止意外,可连接一个安全装置。下图的装置能起到此作用的是___________。
![]()

(4)由A、B、C、D四种元素可以组成多种既能与强酸反应又能与强碱反应的化合物。其中有一种在加热条件下能分解生成等物质的量的三种产物,该化合物是 ;另一种是人体必须的营养物质,它的相对分子质量为75,该化合物是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com