
【题目】1892年比利时人索尔维以NaCl、CO2、NH3、H2O为原料制得了纯净的Na2CO3,该法又称氨碱法,其主要生产流程如下。完成下列填空
(1) 写出反应①中产生碳酸氢钠的离子方程式_________________________________。
(2)NaHCO3在水中溶解度较小,以沉淀形式析出,则图中③的操作名称___________________。从绿色化学原料的充分利用的角度看,该方法有明显的缺陷(答一条即可)___________。
【答案】Na++NH3+CO2+H2O→NaHCO3↓+NH4+ 过滤 产物CaCl2没有利用上
【解析】
工业制碱的原理涉及反应:![]() ,
,![]() ,索尔维法用生成的氯化铵制备氨气,将氯化铵进行了循环利用,所以从理论上讲,是不需要补充氨的,但是在生产过程中,
,索尔维法用生成的氯化铵制备氨气,将氯化铵进行了循环利用,所以从理论上讲,是不需要补充氨的,但是在生产过程中,![]() 母液被弃去,氯化铵制备氨气生成了无用的氯化钙,这两点是索尔维法的缺陷。
母液被弃去,氯化铵制备氨气生成了无用的氯化钙,这两点是索尔维法的缺陷。
(1)根据流程图,反应①是向饱和氯化钠溶液中通入氨气和二氧化碳,离子方程式为:![]() ,
,
答案为:![]() ;
;
(2)![]() 在水中溶解度较小,以沉淀形式析出,故③操作为过滤,从绿色化学原料的充分利用的角度看,
在水中溶解度较小,以沉淀形式析出,故③操作为过滤,从绿色化学原料的充分利用的角度看,![]() 母液被弃去,氯化铵制备氨气生成了无用的氯化钙,这两点是索尔维法的缺陷,
母液被弃去,氯化铵制备氨气生成了无用的氯化钙,这两点是索尔维法的缺陷,
答案为:过滤;产物![]() 没有利用上
没有利用上


 阳光课堂课时优化作业系列答案
阳光课堂课时优化作业系列答案科目:高中化学 来源: 题型:
【题目】已知表中是某些有机物的模型图,根据要求回答下列问题:
有机物 | 甲 | 乙 | 丙 |
模型 |
|
|
|
(1)甲的分子式是___________________,其一氯代物有___________________种。
(2)写出乙与![]() 的
的![]() 溶液发生反应的化学方程式:______________________________________,该反应的反应类型是___________________。
溶液发生反应的化学方程式:______________________________________,该反应的反应类型是___________________。
(3)丙的摩尔质量为![]() ,则用苯制备该物质时的催化剂是___________________。
,则用苯制备该物质时的催化剂是___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2014年中国十大科技成果之一是:我国科学家成功实现甲烷在催化剂及无氧条件下,一步高效生产乙烯、芳烃和氢气等化学品,为天然气化工开发了一条革命性技术。以甲烷为原料合成部分化工产品流程如图(部分反应条件已略去):
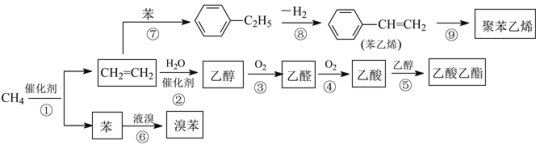
(1)乙酸分子中所含官能团名称为_____。
(2)聚苯乙烯的结构简式为_____。
(3)图中9步反应中只有两步属于取代反应,它们是_____(填序号)。
(4)写出下列反应的化学方程式(注明反应条件):
反应⑤为_____;
反应⑥为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 时,将
时,将![]() 溶液逐滴滴加到
溶液逐滴滴加到![]() 溶液中,所得溶液的
溶液中,所得溶液的![]() 与滴加
与滴加![]() 的体积关系如右图所示。下列指定溶液浓度关系说法正确的是
的体积关系如右图所示。下列指定溶液浓度关系说法正确的是
已知:![]() ,
,![]() 时
时![]() 的
的![]() ,
,![]() 。
。
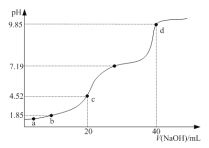
A.![]() 点所得溶液中:
点所得溶液中:![]()
B.![]() 点所得溶液中:
点所得溶液中:![]()
C.![]() 点所得溶液中:
点所得溶液中: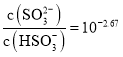
D.![]() 点所得溶液中:
点所得溶液中:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F为中学化学中的常见物质,且物质A由1~2种短周期元素组成,在一定条件下有如图转化关系,请完成下列问题:
![]()
(1)若常温下A为有色气体。
①当F是一种金属单质时,请写出一定浓度的B溶液和适量F反应生成C与气体E的离子方程式:_________________。
②当C为直线形分子时,E具有漂白性,物质F焰色反应呈黄色,则C的电子式为________________;D中所含化学键的类型为____________________。
(2)若A为淡黄色固体,D为白色难溶于水的物质,且A和D的相对分子质量相等,请用离子方程式表示F的水溶液呈酸性的原因:_________________。
(3)若A中一种元素原子的最外层电子数为内层电子总数的![]() ,将B和D分别溶于水,所得溶液按恰当比例混合,可得一种不含金属元素的盐溶液,请写出A与H2O反应的化学方程式:____________;B转化为C的化学方程式为______________。
,将B和D分别溶于水,所得溶液按恰当比例混合,可得一种不含金属元素的盐溶液,请写出A与H2O反应的化学方程式:____________;B转化为C的化学方程式为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国化学家侯德榜改革国外的纯碱生产工艺,创造了侯德榜制碱法又叫联碱法,该法是将合成氨工厂生产的NH3及副产品CO2,再与饱和食盐水反应.
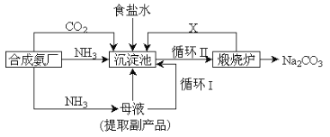
(1)该法与氨碱法比大大提高了原料利用率,主要表现在_______。
(2)碳酸氢钠分解产生的二氧化碳可循环使用,但必须要补充,补充的主要原因是_________,但实际生产中补充量超过理论上反应耗用量,可能的原因是______。
(3)氨碱法需补充的二氧化碳一定来自_________。那么联合制碱需补充的二氧化碳可能来自__________。
(4)侯德榜法在滤去碳酸氢钠的母液中通氨气并加入细小食盐颗粒,冷却析出副产品,通氨气的作用____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:①A的产量通常用来衡量一个国家的石油化工水平;
②![]() 。
。
现以A为主要原料合成化合物E,其合成路线如图所示。回答下列问题:
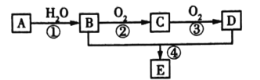
(1)写出下列物质的官能团名称:B_____;C______。
(2)反应④的化学方程式为_____________,反应类型是__________。
(3)某学习小组设计B的催化氧化的实验装置如图所示,试回答下列问题。
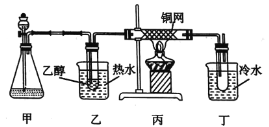
①甲的锥形瓶中盛放的固体药品可能为_______(填字母)。
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
②实验过程中,丙装置硬质玻璃管中发生反应的化学方程式为_____________。
③物质B的催化氧化产物与葡萄糖具有相同的特征反应,将所得的氧化产物与新制氢氧化铜悬浊液混合后加热,现象为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.写出下列反应的热化学方程式。
(1)CuCl(s)与O2反应生成CuCl2(s)和一种黑色固体。在25 ℃、101 kPa下,已知该反应每消耗1 mol CuCl(s),放热44.4 kJ,该反应的热化学方程式是_____________________。
(2)在1.01×105 Pa时,16 g S固体在足量的氧气中充分燃烧生成二氧化硫,放出148.5 kJ的热量,则S固体燃烧热的热化学方程式为________________________。
II.研究NOx、SO2、CO等大气污染气体的处理具有重要意义。
(3)处理含CO、SO2烟道气污染的一种方法是将其在催化剂作用下转化为单质S固体。已知:
①CO(g)+![]() O2(g)=CO2(g) ΔH=-283.0 kJ·mol-1
O2(g)=CO2(g) ΔH=-283.0 kJ·mol-1
②S(s)+O2(g)=SO2(g) ΔH=-296.0 kJ·mol-1
此反应的热化学方程式是_____________________。
(4)氮氧化物是造成光化学烟雾和臭氧层损耗的主要气体。已知:
CO(g)+NO2(g)=NO(g)+CO2(g) ΔH=-a kJ·mol-1(a>0)
2CO(g)+2NO(g)=N2(g)+2CO2(g) ΔH=-b kJ·mol-1(b>0)
若用标准状况下3.36 L CO还原NO2至N2(CO完全反应)的整个过程中转移电子的物质的量为________mol,放出的热量为______________kJ(用含有a和b的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是恒温下某化学反应的反应速率随反应时间变化的示意图。下列叙述与示意图不相符合的是
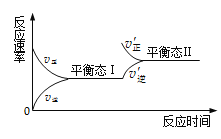
A.反应达平衡时,正反应速率和逆反应速率相等
B.该反应达到平衡Ⅰ后,增大反应物的浓度,平衡发生移动,达到平衡态Ⅱ
C.该反应达到平衡态Ⅰ后,减小反应物浓度,平衡发生移动,达到平衡态Ⅱ
D.同一种气体反应物在平衡态Ⅰ和平衡态Ⅱ时体积分数不相等
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com