
【题目】下列关于元素周期律和元素周期表的论述中正确的是( )。
A.同一主族的元素从上到下金属性逐渐减弱
B.元素周期表是元素周期律的具体表现形式
C.同一周期从左到右,元素原子半径逐渐增大
D.非金属元素的最高正化合价等于它的负化合价的绝对值
科目:高中化学 来源: 题型:
【题目】有4瓶常用溶液:①BaCl2溶液,②NaCl溶液,③Na2SO4溶液,④CuSO4溶液。不用其他试剂,可通过实验方法将它们一一鉴别开来,鉴别出来的先后顺序可能是( )
A.④①②③B.④②①③C.④①③②D.①④③②
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种三室微生物燃料电池污水净化系统原理如下图所示,图中含酚废水中有机物可用C6H6O表示,左、中、右室间分别以离子交换膜分隔。下列说法不正确的是( )

A. 左池的pH值降低
B. 右边为阴离子交换膜
C. 右池电极的反应式:2NO3-+10e-+12H+= N2↑+ 6H2O
D. 当消耗0.1molC6H6O,在标准状况下将产生0.28mol氮气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)为了验证Fe2+与Cu2+氧化性强弱,下列装置能达到实验目的的是______,写出正极的电极反应________。若构建原电池时两个电极的质量相等,当导线中通过0.05mol电子时,两个电极的质量差为________。
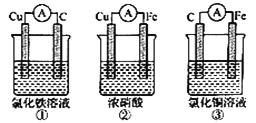
(2)将CH4设计成燃料电池,其利用率更高,装置如图所示(A、B为多孔碳棒)。

①实验测得OH-定问移向B电极,则_____处电极入口通甲烷(填A或B),其电极反应式为 ___________。
②当消耗甲院的体积为33.6L(标准状况下)时,假设电池的能量转化率为80%,则导线中转移电子的物质的量为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将纯锌片和纯铜片按图示方式插入同浓度的稀硫酸中一段时间,下列叙述正确的是

A. 两烧杯中锌片质量均减小,铜片质量均不变
B. 甲烧杯中锌片和铜片表面均产生气泡,乙烧杯中只有锌片表面产生气泡
C. 甲烧杯中铜片失去电子,乙烧杯中铜不参与化学反应
D. 当转移1mol电子时,甲烧杯中产生氢气比乙烧杯中产生的氢气多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度和压强下,在2 L的密闭容器中合成氨气:N2(g)+3H2(g)![]() 2NH3(g) 。在反应过程中反应物和生成物的物质的量随时间的变化如图所示。下列说法错误的是:
2NH3(g) 。在反应过程中反应物和生成物的物质的量随时间的变化如图所示。下列说法错误的是:
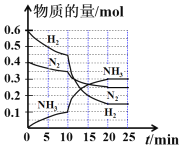
A. 0~10 min内,以NH3表示的平均反应速率为0.005 mol L-1 min-1
B. 10~20 min内,NH3浓度变化的原因可能是加入催化剂或缩小容器体积
C. 该反应在20 min时达到化学平衡状态
D. N2的平衡转化率与H2平衡转化率相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种钌(Ru)基配合物光敏染料敏化太阳能电池的原理及电池中发生的主要反应如图所示。下列说法正确的是

A. 镀铂导电玻璃的作用是传递I-
B. 电池工作时,光能转变为电能,X为电池的正极
C. 电池的电解质溶液中I-和I3-的浓度均不断减小
D. 电解质溶液中发生反应2Ru3++3I-═2Ru2++I3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现用传感技术测定喷泉实验中的压强变化来认识喷泉实验的原理。下列说法正确的是

A. 制取氨气时烧瓶中的固体常用CaO或CaCl2
B. 将湿润的蓝色石蕊试纸置于三颈瓶口,试纸变红,说明NH3已经集满
C. 关闭a,将单孔塞(插有吸入水的胶头滴管)塞紧颈口c,打开b,完成喷泉实验,电脑绘制三颈瓶内压强变化曲线如图2,则E点时喷泉最剧烈
D. 工业上,若出现液氨泄漏,喷稀盐酸比喷洒NaHCO3溶液处理效果好
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外小组在实验室用二氧化锰和浓盐酸共热制备氯气,并进行氯气性质的研究。
(1)该小组同学欲用下图所示仪器及试剂制备并收集纯净、干燥的氯气。
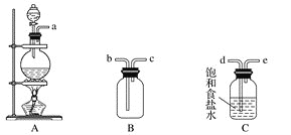
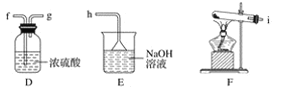
①用不到的仪器是________(填大写字母)
②将各仪器按先后顺序连接起来,应该是:___________(用导管口处的字母表示)。
③浓盐酸与二氧化锰反应的离子方程式_____________
④ C的作用___________,D的作用_______,E中倒置漏斗的作用是_________
(2)该小组同学设计如下所示装置探究氯气的氧化性。
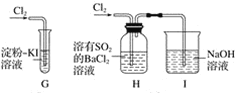
① 通少量Cl2时,G中的现象是_______,原因是_________(用化学方程式表示)
② H中的现象是__________________。
③ 烧杯中NaOH溶液的作用是______________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com