
分析 水溶液中或熔融状态下能够导电的化合物称为电解质,酸、碱、盐都是电解质;在上述两种情况下都不能导电的化合物称为非电解质,蔗糖、乙醇等都是非电解质.大多数的有机物都是非电解质;单质,混合物既不是电解质也不是非电解质;物质导电有两种原因,一是金属类有自由移动的电子能够导电,二是能够产生自由离子的溶液能够导电.
解答 解:①HCl气体不能导电,溶于水能导电,属于电解质;
②NH3不能导电,溶于水因为生成了一水合氨,所以导电,本身不能电离,属于非电解质;
③熔融的NaOH能导电,属于电解质;
④SO2不能导电,溶于水能导电是因为生成了亚硫酸,亚硫酸导电,二氧化硫是非电解质;
⑤Cu能导电,是金属单质,既不是电解质也不是非的电解质;
⑥氨水能导电,属于混合物,既不是电解质也不是非电解质;
⑦KNO3溶液能导电,属于混合物,既不是电解质也不是非电解质;
⑧液态醋酸不能导电,溶于水能导电,属于电解质;
⑨蔗糖不能导电,属于非电解质;
⑩硫酸钡固体不能导电,熔融状态下能导电,属于电解质,
故答案为:③⑤⑥⑦;①③⑧⑩;②④⑨.
点评 本题较简单,主要考查电解质的定义,熟悉常见的酸、碱、盐都属于电解质来解答,注意导电,要从导电实质的角度去分析给定物质是否具备导电性能.


科目:高中化学 来源: 题型:选择题
| A. | ①③⑤⑧ | B. | ②③④⑤⑥⑦ | C. | ③⑤⑧ | D. | ①②③④⑤⑥⑦⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若有9.8gH2SO4参加反应,则转移电子的物质的量为1mol | |
| B. | 该反应的化学方程式为:5PbO2+2MnSO4+2H2SO4═Pb(MnO4)2+4PbSO4+2H2O | |
| C. | Pb(MnO4)2既是氧化产物又是还原产物 | |
| D. | X是MnSO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
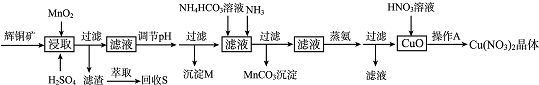
| 离子 | 开始沉淀的pH | 完全沉淀的pH |
| Fe3+ | 1.1 | 3.2 |
| Mn2+ | 8.3 | 9.8 |
| Cu2+ | 4.4 | 6.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2CO3溶液中:c(Na+)+c(H+)=c(HCO3-)+c(CO32-)+c(OH-) | |
| B. | 0.1 mol•L-1NH4Cl溶液中:c(Cl-)>c(H+)>c(NH4+)>c(OH-) | |
| C. | K2S溶液中:2c(K+)═c(H2S)+c(S2-)+c(HS-) | |
| D. | 相同浓度的CH3COOH和NaOH溶液等体积混合后,则:c(CH3COO-)+c(CH3COOH)═c(Na+) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 高温下,16.8g Fe与足量水蒸气完全反应失去电子数为0.8 NA | |
| B. | 12g NaHSO4固体中阴离子所带负电荷数为0.02 NA | |
| C. | 1 mol OD-含有的质子、中子、电子数均为9NA | |
| D. | 含4 NA个离子的固体Na2O2溶于水配成1L溶液,所得溶液中c(Na+)=2 mol•L-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com