
| A. | ①③⑤⑧ | B. | ②③④⑤⑥⑦ | C. | ③⑤⑧ | D. | ①②③④⑤⑥⑦⑧ |
分析 水溶液中或熔融状态下能够导电的化合物称为电解质,酸、碱、盐都是电解质.
解答 解:①NaCl溶液属于混合物既不是电解质也不是非电解质;
②干冰不能导电,属于非电解质;
③冰醋酸(纯净的醋酸)不能导电,但是溶于水能导电,属于电解质;
④铜是金属单质,既不是电解质也不是非电解质;
⑤BaSO4固体,熔融状态下能导电,属于电解质;
⑥蔗糖不能导电,属于非电解质;
⑦酒精不能导电,属于非电解质;
⑧熔融的KNO3,能导电,属于电解质,
故选C.
点评 本题较简单,主要考查电解质的定义,熟悉常见的酸、碱、盐都属于电解质来解答,注意导电,要从导电实质的角度去分析给定物质是否具备导电性能.


 赢在课堂名师课时计划系列答案
赢在课堂名师课时计划系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
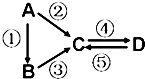 A、B、C、D均为中学化学常见的纯净物,A是单质.它们之间有如下的反应关系:
A、B、C、D均为中学化学常见的纯净物,A是单质.它们之间有如下的反应关系:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
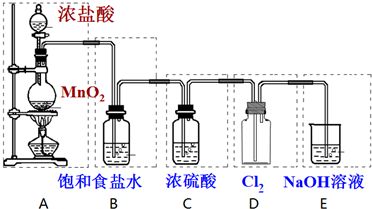
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 生石灰与水混合 | B. | 灼热的碳与CO2的反应 | ||
| C. | Ba(OH)2•8H2O与NH4Cl的反应 | D. | 锌和稀硫酸反应制取氢气 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验步骤 | 实验现象和结论 |
| 取一定量样品充分干燥,然后将样品加热分解,将产生的气体依次通过盛有无水硫酸铜的干燥管和盛有澄清石灰水的洗气瓶. | 无水硫酸铜变蓝色,澄清石灰水变浑浊 说明样品全部是2PbCO3•Pb(OH)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H+ | B. | SO42- | C. | OH- | D. | Na+ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com