
| t/min | 2 | 4 | 7 | 9 |
| n��Y��/mol | 0.12 | 0.11 | 0.10 | 0.10 |
| A�� | 0��2 min��ƽ������v��Z��=2.0��10-3 mol•L-1•min-1 | |
| B�� | �����������䣬�����¶ȣ���Ӧ�ﵽ��ƽ��ʱv��������v���棩 | |
| C�� | ���¶��´˷�Ӧ��ƽ�ⳣ��K=144 | |
| D�� | �����������䣬�ٳ���0.2 mol Z��ƽ��ʱX������������� |
���� A������v=$\frac{��c}{��t}$�����Y�����ʣ�����������֮�ȵ��ڻ�ѧ������֮�����Z�����ʣ�
B�����ݻ�ѧƽ��״̬�����������жϣ�
C����������ʽ������ƽ�ⳣ���Ķ�����м��㣻
D�����õ�Чƽ���˼�����жϣ�
��� �⣺A.0��2 min��ƽ������v��Z��=$\frac{��c}{��t}$=$\frac{\frac{0.16mol-0.12mol}{10L}}{2min}$mol/��L•min��=0.002mol/��L•min������������֮�ȵ��ڻ�ѧ������֮�ȿɵ�Z������Ϊ2��0.002mol/��L•min��=0.004mol/��L•min������A����
B�����ڸ÷�ӦΪ���ȷ�Ӧ�������¶�ʱ��ƽ�������ƶ������Ǵﵽƽ��״̬ʱ���淴Ӧ������ȣ���v���棩=v����������B����
C����������ʽ��
X��g��+Y��g��?2Z��g��
��ʼ��mol/L�� 0.016 0.016 0
ת����mol/L�� 0.006 0.006 0.012
ƽ�⣨mol/L��0.01 0.01 0.012
����ƽ�ⳣ��K=$\frac{0.01{2}^{2}}{0.01��0.01}$=1.44����C����
D�����轫0.2mol Z����һ�����н�����ԭƽ��ɵ�Чƽ�����ϵ���ٽ�����ϵ���뵽ԭ�����У����ڸ÷�Ӧǰ������������䣬����ѹǿ��ƽ����ƶ�û��Ӱ�죬���Լ����X������������䣬��D��ȷ��
��ѡD��
���� ������Ҫ�����˻�ѧ��Ӧ���ʵļ��㣬��Ŀ�Ѷ��еȣ��漰Ӱ��ƽ���ƶ������ء���ѧƽ�ⳣ���ļ��㡢��Чƽ���֪ʶ����ȷ��ѧƽ�⼰��Ӱ������Ϊ���ؼ���ע�����յ�Чƽ��֪ʶ��Ӧ�÷���������������ѧ���ķ�����������ѧ����������


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | �Ͼ���ʾ��������գ�����ҪĿ����Ϊ����ȡ���еĹ��ؽ��� | |
| B�� | ������ˮ�������ĵ�����������ֲ��Ӫ���أ����ᵼ��ˮ����Ⱦ | |
| C�� | ������̼�ͼ���Ȼᵼ�¡�����ЧӦ�����Ӷ�����ȫ���ů | |
| D�� | ����������������صĽ�ͨ���⣬������һ�ֽ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
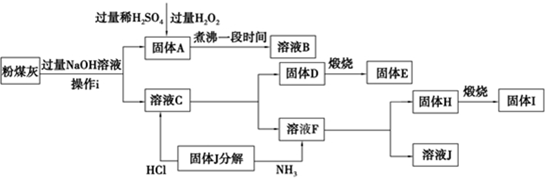
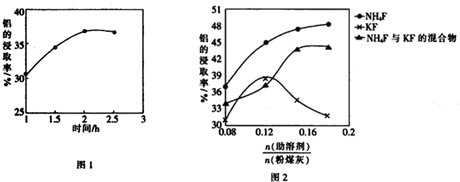
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �������ӣ�����������Ų���ȫ��ͬ�����仯ѧ����һ����ͬ | |
| B�� | ���ӻ������У�һ�����ڽ���Ԫ�غͷǽ���Ԫ�� | |
| C�� | ͬʱ�������Ӽ����ۼ��Ļ����һ�������ӻ�����������ǹ��ۻ����� | |
| D�� | ��ʧ���ӵ�ԭ�ӣ���õ��ӵ�����һ��ǿ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | NH3 | B�� | H2O | C�� | Ca2+ | D�� | CO |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
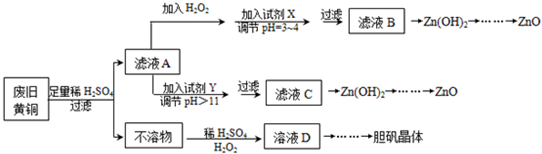
| Fe3+ | Fe2+ | Zn2+ | |
| ��ʼ������pH | 1.1 | 5.8 | |
| ������ȫ��pH | 3.0 | 8.8 | 8.9 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ͭ��ˮ��ͷ���Ӵ��ĸ���ˮ��������ʴ | |
| B�� | ������̼�����顢���������������ЧӦ������ | |
| C�� | �ڹ�ҵ�����У����Ƴ��ڽϵ��¶Ⱥ�ѹǿ����ʹ��ӦѸ�ٽ��еĴ��������ܺõĽ���Ч����������ʮ�˴�����ġ���ɫ��չ������ | |
| D�� | ʯ���ѽ⡢ú����������ˮ��þ��������ѧ�仯 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | HCl�TH++Cl- | B�� | NH3•H2O�TNH4++OH- | ||
| C�� | CaCl2=Ca2++2Cl- | D�� | CH3COOH?CH3COO-+H+ |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com